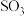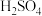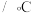按要求回答下列问题:
(1)CH4是_______ 形分子,是_______ 分子(填“极性”“非极性”)。
(2)①基态原子的N层有1个未成对电子,M层未成对电子数最多的元素的价电子排布式为_______ 。
②最外层电子数是次外层电子数3倍的元素的轨道表示式为_______ 。
③Cu原子的结构示意图为_______ 。
(3)某元素+3价离子的电子排布式为1s22s22p63s23p63d3,该元素在周期表中的_______ 区。
(4)已知下列四种酸①CH3CBr2COOH②CH3CF2COOH③CH3CH2COOH④CH3COOH酸性由弱到强的顺序为_______ 。
(1)CH4是
(2)①基态原子的N层有1个未成对电子,M层未成对电子数最多的元素的价电子排布式为
②最外层电子数是次外层电子数3倍的元素的轨道表示式为
③Cu原子的结构示意图为
(3)某元素+3价离子的电子排布式为1s22s22p63s23p63d3,该元素在周期表中的
(4)已知下列四种酸①CH3CBr2COOH②CH3CF2COOH③CH3CH2COOH④CH3COOH酸性由弱到强的顺序为
更新时间:2024-05-04 16:46:18
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】在分析化学的电位法中,甘汞电极常做参比电极,它是由金属汞及其难溶盐Hg2Cl2和KCl溶液组成的电极。Hg2Cl2(甘汞)毒性较小,而HgCl2(升汞)有剧毒。
(1)K元素的基态原子的电子填充于_____ 个不同的能级。
(2)Hg的价层电子排布式为5d106s2,Hg元素位于元素周期表的_______ 区。
(3)Hg2Cl2在400~500℃时升华,由此推测Hg2Cl2的晶体类型为____ 。
(4)KCl和NaCl相比,____ 的熔点更高,原因是________ 。
(5)把NH4Cl和HgCl2按一定比例混合,在密封管中加热时,生成某种晶体,其晶胞如图所示。用X-射线衍射法测得该晶体的晶胞为长方体(晶胞参数a=b =419pm、c=794pm),每个NH4+可视为被8个Cl-围绕,距离为335pm,Cl-与Cl-尽可能远离。
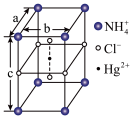
①该晶体的化学式为________ 。
②晶体中Cl-的空间环境_____________ (填“相同”或“不相同”)。用题中数据说明理由_______________
③设阿伏加 德罗常数的值为NA,则该晶体的密度为_______ g/cm3(列出计算表达式)。
(1)K元素的基态原子的电子填充于
(2)Hg的价层电子排布式为5d106s2,Hg元素位于元素周期表的
(3)Hg2Cl2在400~500℃时升华,由此推测Hg2Cl2的晶体类型为
(4)KCl和NaCl相比,
(5)把NH4Cl和HgCl2按一定比例混合,在密封管中加热时,生成某种晶体,其晶胞如图所示。用X-射线衍射法测得该晶体的晶胞为长方体(晶胞参数a=b =419pm、c=794pm),每个NH4+可视为被8个Cl-围绕,距离为335pm,Cl-与Cl-尽可能远离。

①该晶体的化学式为
②晶体中Cl-的空间环境
③设阿伏加 德罗常数的值为NA,则该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】下图是s能级和p能级的原子轨道图。试回答下列问题:
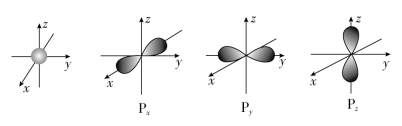
(1)s电子的原子轨道呈___________ 形,每个s能级有___________ 个原子轨道;p电子的原子轨道呈____ 形,每个p能级有___________ 个原子轨道。
(2)元素X的原子最外层电子排布式为nsnnpn+2,原子中能量最高的是___________ 电子,其电子云在空间有3个互相___________ (填“垂直”或“平行”)的伸展方向。元素X的名称是___________ ,它的氢化物中原子个数为1:1的化合物中,其σ键类型为___________ 。
(3)元素Y的原子最外层电子排布式为nsn-1npn+2,Y的元素符号为___________ ,原子的核外电子排布式为___________ 。

(1)s电子的原子轨道呈
(2)元素X的原子最外层电子排布式为nsnnpn+2,原子中能量最高的是
(3)元素Y的原子最外层电子排布式为nsn-1npn+2,Y的元素符号为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D、E、F、G、H是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如下表:
请用化学用语填空:
(1) A元素在元素周期表中的位置________ ;A、B、C三种元素的第一电离能由大到小的排序为_____ (用元素符号填写);
(2) B元素与宇宙中含量最丰富的元素形成的最简单化合物的分子构型为____ ,B元素所形成的单质分子中σ键与π键数目之比为____ 。
(3) G元素的低价阳离子的离子结构示意图是________ ,F元素原子的外围电子排布图是________ ,H元素的基态原子核外电子排布式是________ 。
(4) D元素的单质及其常见化合物的焰色反应主要利用了原子光谱中的______ (A.原子吸收光谱B.原子发射光谱)
(5) 上述元素属于p区的是_______ (用元素符号填写);
| 元素 | 相关信息 |
| A | 原子核外有6种不同运动状态的电子 |
| C | 基态原子中s电子总数与p电子总数相等 |
| D | 原子半径在同周期元素中最大 |
| E | 基态原子最外层电子排布式为3s23p1 |
| F | 基态原子的最外层p轨道有两个电子的自旋方向与其他电子的自旋方向相反 |
| G | 基态原子核外有7个能级且能量最高的能级上有6个电子 |
| H | 是我国使用最早的合金中的最主要元素 |
(1) A元素在元素周期表中的位置
(2) B元素与宇宙中含量最丰富的元素形成的最简单化合物的分子构型为
(3) G元素的低价阳离子的离子结构示意图是
(4) D元素的单质及其常见化合物的焰色反应主要利用了原子光谱中的
(5) 上述元素属于p区的是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】中国科学报报道钙钛矿太阳能电池在柔性可穿戴电子设备等方面具有独特的优势和巨大的用潜力。钛酸钙晶胞俯视投影图如下:
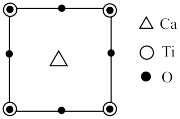
已知:晶胞中只含有一个钙原子,钙原子与钛原子之间的最近距离为xnm。
回答下列问题::
(1)基态 的核外价电子排布图为
的核外价电子排布图为___________ ,Al原子核外电子的空间运动状态有___________ 种
(2)Ti的四卤化物熔点如下表所示, 熔点高于其他三种卤化物,自
熔点高于其他三种卤化物,自 至
至 熔点依高,原因是
熔点依高,原因是___________ 。
(3)钛酸钙的组成元素的电负性大小顺序是___________ 。
(4)如图晶胞结构的化学式为___________ ; 、
、 的配位数分别为
的配位数分别为___________ 。
(5)晶体密度为___________  (列出计算式)。
(列出计算式)。

已知:晶胞中只含有一个钙原子,钙原子与钛原子之间的最近距离为xnm。
回答下列问题::
(1)基态
 的核外价电子排布图为
的核外价电子排布图为(2)Ti的四卤化物熔点如下表所示,
 熔点高于其他三种卤化物,自
熔点高于其他三种卤化物,自 至
至 熔点依高,原因是
熔点依高,原因是| 化合物 |  |  |  |  |
| 熔点/℃ | 377 | -24.12 | 38.3 | 155 |
(3)钛酸钙的组成元素的电负性大小顺序是
(4)如图晶胞结构的化学式为
 、
、 的配位数分别为
的配位数分别为(5)晶体密度为
 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】前四周期原子序数依次增大的元素A、B、C、D、E中,A的基态原子核外3个能级上有电子,且每个能级上的电子数相等,B原子核外电子有7种不同的运动状态,C元素原子核外的M层中只有2对成对电子,D+与C2-的电子数相等,E元素位于元素周期表的ds区,且基态原子价电层电子均已成对。
回答下列问题:
(1)E2+的外围电子排布图为________________ 。
(2)五种元素中电负性最小的是________ (填元素符号),CAB-离子中,A原子的杂化方式是________ 。
(3)AB-、D+和E2+三种离子组成的化学物质D2E(AB)4,该化合物中存在一个复杂离子,该离子的化学式为________ ,配位体是________ 。
(4)C和E两种元素组成的一种化合物的晶胞如图所示。
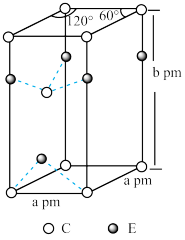
①该化合物的化学式为________ ,E的配位数为________ ,C采取________ (填“简单立方”、“体心立方”、“六方最密”或“面心立方最密”)堆积;
②列式表示该晶体的密度:________ g·cm-3。(NA表示阿伏伽德罗常数的值)
回答下列问题:
(1)E2+的外围电子排布图为
(2)五种元素中电负性最小的是
(3)AB-、D+和E2+三种离子组成的化学物质D2E(AB)4,该化合物中存在一个复杂离子,该离子的化学式为
(4)C和E两种元素组成的一种化合物的晶胞如图所示。

①该化合物的化学式为
②列式表示该晶体的密度:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】硫及其化合物有许多用途,相关物质的物理常数如下表所示:
回答下列问题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为____________________________ ,基态S原子电子占据最高能级的电子云轮廓图为________ 形。
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是__ 。
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为__________________ 。
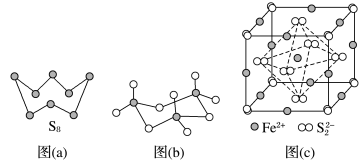
(4)气态三氧化硫以单分子形式存在,其分子的立体构型为________ 形,其中共价键的类型有________ 种;固体三氧化硫中存在如图(b)所示的三聚分子,该分子中S原子的杂化轨道类型为________ 。
(5)FeS2晶体的晶胞如图(c)所示。晶胞边长为anm、FeS2相对式量为M、阿伏伽德罗常数的值为NA,其晶体密度的计算表达式为______________________________ g·cm-3;晶胞中Fe2+位于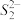 所形成的正八面体的体心,该正八面体的边长为
所形成的正八面体的体心,该正八面体的边长为________ nm。
|
|
|
|
|
| |
熔点 | -85.5 | 115.2 |
(分解) | -75.5 | 16.8 | 10.3 |
沸点 | -60.3 | 444.6 | -10.0 | 45.0 | 337.0 |
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为

(4)气态三氧化硫以单分子形式存在,其分子的立体构型为
(5)FeS2晶体的晶胞如图(c)所示。晶胞边长为anm、FeS2相对式量为M、阿伏伽德罗常数的值为NA,其晶体密度的计算表达式为
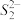 所形成的正八面体的体心,该正八面体的边长为
所形成的正八面体的体心,该正八面体的边长为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】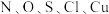 五种元素的单质及其化合物在现代工业生产中有着广泛应用。请回答下列问题:
五种元素的单质及其化合物在现代工业生产中有着广泛应用。请回答下列问题:
(1)第一电离能:N_______ (填“>”或“<”,下同)O,电负性:O_______ S。
(2) 极易溶于水的原因是
极易溶于水的原因是_______ ; 属于
属于_______ (填“极性”或“非极性”)分子,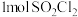 含有
含有 的键为
的键为_______  。
。
(3) 的空间构型是
的空间构型是_______ , 的中心原子的杂化方式为
的中心原子的杂化方式为_______ 。
(4)与 互为等电子体的微粒有
互为等电子体的微粒有_______ (任写两种)。
(5) 与
与 形成化合物的晶胞如图所示。
形成化合物的晶胞如图所示。
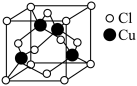
该晶体的化学式为_______ .已知该晶体中 原子和
原子和 原子之间的最短距离为
原子之间的最短距离为 ,且恰好为体对角线的
,且恰好为体对角线的 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则该晶体的密度为
,则该晶体的密度为_______ (只写计算式) 。
。
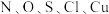 五种元素的单质及其化合物在现代工业生产中有着广泛应用。请回答下列问题:
五种元素的单质及其化合物在现代工业生产中有着广泛应用。请回答下列问题:(1)第一电离能:N
(2)
 极易溶于水的原因是
极易溶于水的原因是 属于
属于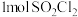 含有
含有 的键为
的键为 。
。(3)
 的空间构型是
的空间构型是 的中心原子的杂化方式为
的中心原子的杂化方式为(4)与
 互为等电子体的微粒有
互为等电子体的微粒有(5)
 与
与 形成化合物的晶胞如图所示。
形成化合物的晶胞如图所示。
该晶体的化学式为
 原子和
原子和 原子之间的最短距离为
原子之间的最短距离为 ,且恰好为体对角线的
,且恰好为体对角线的 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则该晶体的密度为
,则该晶体的密度为 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】下表为长式周期表的一部分,其中的编号代表对应的元素。
请回答下列问题:
(1)③和①形成的一种5核10电子分子,其立体构型为_______ ,中心原子杂化方式为_______ ,属于_______ 分子(填“极性”或“非极性”)。
(2)元素③和⑦的最高价氧化物对应水化物中酸性较强的是:_______ (填化学式),元素⑥的电负性_______ 元素⑦(选填“>”、“=”、“<”=)的电负性。
(3)根据元素周期表分区,元素⑨位于_______ 区,其基态原子电子排布式为_______ 。
(4)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的离子方程式_______ 。
(5)⑩的离子与4个H2O分子形成的阳离子中含的化学键有_______ 。
| ① | |||||||||||||||||
| ② | ③ | ||||||||||||||||
| ④ | ⑤ | ⑥ | ⑦ | ||||||||||||||
| ⑧ | ⑨ | ⑩ |
请回答下列问题:
(1)③和①形成的一种5核10电子分子,其立体构型为
(2)元素③和⑦的最高价氧化物对应水化物中酸性较强的是:
(3)根据元素周期表分区,元素⑨位于
(4)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的离子方程式
(5)⑩的离子与4个H2O分子形成的阳离子中含的化学键有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】二硫化硒(SeS2)具有抗真菌、抗皮脂溢出作用,常用作洗发香波中的去屑剂。
(1)二硫化硒(SeS2)具有抗真菌、抗皮脂溢出作用,常用作洗发香波中的去屑剂。硒与硫在元素周期表中的相对位置如图所示。

硒在元素周期表中的位置是___________ ;硒原子核外有___________ 个未成对电子;硒化氢的电子式为___________ 。
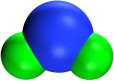
(2)已知SeS2分子比例模型如所示,推测SeS2为___________ 分子(填“极性”或“非极性”)。
(3)SeS2中硫元素的化合价为负价,请从原子结构角度解释原因:___________ 。
工业上提取硒的过程如下:
第一步(未配平):X + Se + H2SO4 → Na2SO4 + H2SeO3 + ClO2↑+ H2O
已知该反应中氧化产物与还原产物的物质的量之比为1:4。
第二步:向H2SeO3溶液中通入SO2,可析出固体Se。
(4)第一步中X的化学式为___________ 。每溶解1 mol Se,转移电子数为___________ 个。
(5)写出第二步反应的化学方程式___________ ;该反应中被氧化的元素是___________ 。
(1)二硫化硒(SeS2)具有抗真菌、抗皮脂溢出作用,常用作洗发香波中的去屑剂。硒与硫在元素周期表中的相对位置如图所示。

硒在元素周期表中的位置是
(2)已知SeS2分子比例模型如所示,推测SeS2为

(3)SeS2中硫元素的化合价为负价,请从原子结构角度解释原因:
工业上提取硒的过程如下:
第一步(未配平):X + Se + H2SO4 → Na2SO4 + H2SeO3 + ClO2↑+ H2O
已知该反应中氧化产物与还原产物的物质的量之比为1:4。
第二步:向H2SeO3溶液中通入SO2,可析出固体Se。
(4)第一步中X的化学式为
(5)写出第二步反应的化学方程式
您最近一年使用:0次