硒是动物和人体所必需的微量元素之一,也是一种重要的工业原料。河南焦作的山药富含硒(Se),有抗癌、抗衰老等重要功能。请回答下列问题。
(1)34Se的原子结构示意图为___________ ,其在周期表中的位置为______ 。
(2)氧、硫、硒位于同一主族,其性质具有一定的递变性。
①下列说法正确的是___________ (填标号)。
A.还原性:S2->Se2-
B.浓硒酸不可能具有强氧化性、吸水性
C.稳定性:H2Se>H2S>H2O
D.氧化性:O2>Se
②SO2通入SeO2的水溶液中会生成不溶于水的Se,该反应的化学方程式为___________ ;Se能与浓硫酸反应生成SO2和SeO2,则浓硫酸、SO2和SeO2三者中,氧化性最弱的为___________ 。
(1)34Se的原子结构示意图为
(2)氧、硫、硒位于同一主族,其性质具有一定的递变性。
①下列说法正确的是
A.还原性:S2->Se2-
B.浓硒酸不可能具有强氧化性、吸水性
C.稳定性:H2Se>H2S>H2O
D.氧化性:O2>Se
②SO2通入SeO2的水溶液中会生成不溶于水的Se,该反应的化学方程式为
更新时间:2024-05-07 16:25:57
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1)制印刷电路时常用氯化铁溶液作为“腐蚀液”。铜被氯化铁溶液腐蚀的方程式为:2FeCl3+Cu=2FeCl2+CuCl2;氯化铁溶液也能与铁反应:2FeCl3+Fe=3FeCl2;当向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,烧杯底部可能出现的情况是___ (多选)
A.有铜无铁B.有铁无铜C.有铁有铜D.无铁无铜
请把铜被氯化铁溶液腐蚀的化学方程式改写为离子方程式______ :
(2)某河道两旁有甲乙两厂。它们排放的工业废水中,共含有K+、Ag+、Fe3+、C1-、OH-、NO 六种离子。若测得甲厂的废水明显呈碱性,则可推知乙厂废水中所含的三种离子是
六种离子。若测得甲厂的废水明显呈碱性,则可推知乙厂废水中所含的三种离子是_______ 。
A.有铜无铁B.有铁无铜C.有铁有铜D.无铁无铜
请把铜被氯化铁溶液腐蚀的化学方程式改写为离子方程式
(2)某河道两旁有甲乙两厂。它们排放的工业废水中,共含有K+、Ag+、Fe3+、C1-、OH-、NO
 六种离子。若测得甲厂的废水明显呈碱性,则可推知乙厂废水中所含的三种离子是
六种离子。若测得甲厂的废水明显呈碱性,则可推知乙厂废水中所含的三种离子是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】CdSnAs2是一种高迁移率的新型热电材料,回答下列问题:
(1)Sn为ⅣA族元素,单质Sn与干燥Cl2反应生成SnCl4。常温常压下SnCl4为无色液体,SnCl4空间构型为_______ ,其固体的晶体类型为_______ 。
(2)NH3、PH3、AsH3的沸点由高到低的顺序为_______ ,(填化学式,下同)还原性由强到弱的顺序为_______ ,键角由大到小的顺序为_______ 。
(1)Sn为ⅣA族元素,单质Sn与干燥Cl2反应生成SnCl4。常温常压下SnCl4为无色液体,SnCl4空间构型为
(2)NH3、PH3、AsH3的沸点由高到低的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1)根据反应的难易(反应条件)比较下列物质的氧化性强弱
①2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
②MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
可判断氧化性:KMnO4_______ MnO2。
(2)根据变价元素被氧化或被还原的程度比较下列物质的氧化性强弱
①2Fe+3Cl2 2FeCl3
2FeCl3
②Fe+S FeS
FeS
可判断氧化性:氯气_______ 硫。
(3)由(1)、(2)可知,根据反应条件、氧化产物的价态高低来比较物质的氧化性、还原性强弱时,应注意什么,结论是什么_______ 。
(1)根据反应的难易(反应条件)比较下列物质的氧化性强弱
①2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
②MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O可判断氧化性:KMnO4
(2)根据变价元素被氧化或被还原的程度比较下列物质的氧化性强弱
①2Fe+3Cl2
 2FeCl3
2FeCl3②Fe+S
 FeS
FeS可判断氧化性:氯气
(3)由(1)、(2)可知,根据反应条件、氧化产物的价态高低来比较物质的氧化性、还原性强弱时,应注意什么,结论是什么
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】如下图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(气体体积在同温同压下测定)。试回答问题:
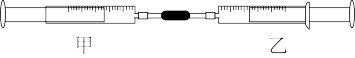
(1)实验1中发生反应的离子方程式为:___________ 。
(2)实验2反应后甲针筒内有少量的残留气体,正确的处理方法是将其通入___________ 溶液中。
(3)实验3中能看见有白烟产生并生成一种气体(空气主要成分之一),该化学反应方程式___________ ,写出检验所得白色固体中阳离子的操作方法:___________ ,充分反应后甲针筒内剩余气体成分为___________ (填化学式)。

| 实验序号 | 甲针筒内物质 | 乙针筒内物质 |
| 1 | 溴水 | SO2 |
| 2 | H2S | SO2 |
| 3 | 15mLCl2 | 35mLNH3 |
(2)实验2反应后甲针筒内有少量的残留气体,正确的处理方法是将其通入
(3)实验3中能看见有白烟产生并生成一种气体(空气主要成分之一),该化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】以下是依据一定的分类标准,对某些物质与水反应情况进行分类的分类图。请根据你所学知识,按要求填空。

(1)上述第一级分类标准(分成A、B组)的依据为___ 。
(2)C组中某一物质常温能与冷水反应,其离子方程式为___ 。
(3)D组中与水反应时氧化剂和还原剂物质的量之比为1:1的物质有____ 。
(4)F组中某一物质的水溶液呈弱碱性,用电离方程式表示呈弱碱性的原因:___ 。
(5)E组中某一物质的水溶液可使酸性KMnO4溶液褪色,用离子方程式表示褪色的原因:___ 。

(1)上述第一级分类标准(分成A、B组)的依据为
(2)C组中某一物质常温能与冷水反应,其离子方程式为
(3)D组中与水反应时氧化剂和还原剂物质的量之比为1:1的物质有
(4)F组中某一物质的水溶液呈弱碱性,用电离方程式表示呈弱碱性的原因:
(5)E组中某一物质的水溶液可使酸性KMnO4溶液褪色,用离子方程式表示褪色的原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】卤族元素包括氟、氯、溴、碘、砹等元素,位于元素周期表中第ⅦA族。
(1)画出下列卤族元素的原子结构示意图:①氟________ ;②氯________ ③溴________ ;④碘_________ 。
(2)比较卤族元素的原子结构:
①它们在结构上的相同点是____________ ;
②它们在结构上的不同点是_____________ 。
(3)卤族元素原子结构的变化规律是_______________ 。
(1)画出下列卤族元素的原子结构示意图:①氟
(2)比较卤族元素的原子结构:
①它们在结构上的相同点是
②它们在结构上的不同点是
(3)卤族元素原子结构的变化规律是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系,如图是元素周期表的一部分,回答下列问题:
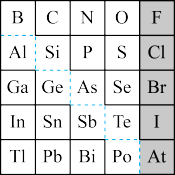
(1)元素Ga在元素周期表中的位置为:___ 。
(2)Sn的最高正价为___ ,Cl的最高价氧化物对应水化物的化学式为___ 。
(3)根据元素周期律,推断
①阴影部分元素形成的氢化物中热稳定性最高的是___ 。(写化学式)
②原子半径比较:N___ Si(填“>”、“<”、“=”或“无法比较”)。

(1)元素Ga在元素周期表中的位置为:
(2)Sn的最高正价为
(3)根据元素周期律,推断
①阴影部分元素形成的氢化物中热稳定性最高的是
②原子半径比较:N
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氟和氯是两种典型的卤族元素。回答下列问题:
(1)氟与氯化学性质相似,写出NaF的电子式:___________ 。根据元素周期律知识,写出氢气和氟气反应的化学方程式(标出反应条件):___________ 。
(2)氧元素的非金属性___________ (填“强于”或“弱于”)氯元素,你的理由是___________ 。根据HF的___________ (选填编号)大于H2O,可推断氟元素的非金属性强于氧元素。
A.酸性 B.熔沸点 C.稳定性 D.键的极性
(3)不同卤素原子之间形成的化合物叫做卤素互化物,如ClF、ICl、BrF3等。ClF是___________ 化合物(填“离子”或“共价”),它遇水发生复分解反应,试写出该反应的化学方程式:___________ 。
(4)盐酸(氢氯酸)和氢氟酸都是一元酸。某温度下,相同pH的盐酸和氢氟酸溶液分别加水稀释,溶液的pH随溶液体积变化的曲线如下图所示。据图判断:
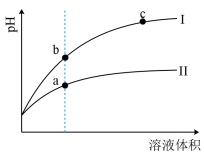
①盐酸稀释时的pH变化曲线为___________ (填“Ⅰ”或“Ⅱ”),溶液的导电性b___________ c(填“>”、“<”或“=”)。
②比较两种溶液中水电离的[H+]:a点___________ b点(填“>”、“<”或“=”)。从电离平衡移动原理解释原因:___________ 。
(1)氟与氯化学性质相似,写出NaF的电子式:
(2)氧元素的非金属性
A.酸性 B.熔沸点 C.稳定性 D.键的极性
(3)不同卤素原子之间形成的化合物叫做卤素互化物,如ClF、ICl、BrF3等。ClF是
(4)盐酸(氢氯酸)和氢氟酸都是一元酸。某温度下,相同pH的盐酸和氢氟酸溶液分别加水稀释,溶液的pH随溶液体积变化的曲线如下图所示。据图判断:

①盐酸稀释时的pH变化曲线为
②比较两种溶液中水电离的[H+]:a点
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】黑火药爆炸时发生的反应:S+2KNO3+3C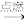 K2S+3CO2↑+N2↑
K2S+3CO2↑+N2↑
(1)上述反应涉及的元素中,非金属性最强的是___________ ,S在周期表中的位置是___________ 。
(2)氮元素对应的气态氢化物是___________ ,其水溶液显___________ 性,写出一水合氨的电离方程式___________ 。
(3)硫元素在自然界主要以硫酸盐的形式存在。写出检验SO 的方法:
的方法:___________
(4)氧、硫的非金属性强弱可通过比较这两种元素___________ (选填编号)
a.原子的得电子的能力b.含氧酸的酸性c.气态氢化物的酸性d.单质的熔沸点
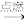 K2S+3CO2↑+N2↑
K2S+3CO2↑+N2↑(1)上述反应涉及的元素中,非金属性最强的是
(2)氮元素对应的气态氢化物是
(3)硫元素在自然界主要以硫酸盐的形式存在。写出检验SO
 的方法:
的方法:(4)氧、硫的非金属性强弱可通过比较这两种元素
a.原子的得电子的能力b.含氧酸的酸性c.气态氢化物的酸性d.单质的熔沸点
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】锶(Sr)位于元素周期表的第5周期IIA族。碳酸锶(SrCO3)是制取锶的原料,用天青石固体(主要成分SrSO4,难溶于水)和Na2CO3溶液混合浸泡可制取碳酸锶。完成下列填空:
(1)在上述反应体系中出现的几种短周期元素,原子半径最大的是______ 。非金属性最强的是______ 。
(2)反应体系中出现的非金属元素可形成二硫化碳(CS2),其分子构型是直线型分子,写出该分子的电子式______ ,该分子为______ (选填“极性”、“非极性”)分子。
(3)已知:锶的原子序数为38,某锶原子的质量数为88,写出能包含这些信息的一种化学符号______ 。写出锶原子的最外层电子排布式______ 。下列关于锶及其化合物的叙述中,错误的是______ 。
a.锶的金属性比镁强 b.氢氧化锶呈两性
c.锶在化合物中呈+2价 d.锶在自然界中以游离态存在
(4)请用溶解平衡移动原理解释工业上可以天青石制取碳酸锶的原因______ 。
钡位于元素周期表第六周期IIA族。工业上制备单质钡的原理如下:2Al+4BaO 3Ba↑+BaO+Al2O3。
3Ba↑+BaO+Al2O3。
(5)常温下Al的金属性比Ba的金属性______ (选填“强”“弱”)。利用上述方法可制取Ba的主要原因是______ 。
a.高温时Al的活泼性大于Ba b.高温有利于BaO分解
c.高温时BaO·Al2O3比Al2O3稳定 d.Ba的沸点比Al的低
(1)在上述反应体系中出现的几种短周期元素,原子半径最大的是
(2)反应体系中出现的非金属元素可形成二硫化碳(CS2),其分子构型是直线型分子,写出该分子的电子式
(3)已知:锶的原子序数为38,某锶原子的质量数为88,写出能包含这些信息的一种化学符号
a.锶的金属性比镁强 b.氢氧化锶呈两性
c.锶在化合物中呈+2价 d.锶在自然界中以游离态存在
(4)请用溶解平衡移动原理解释工业上可以天青石制取碳酸锶的原因
钡位于元素周期表第六周期IIA族。工业上制备单质钡的原理如下:2Al+4BaO
 3Ba↑+BaO+Al2O3。
3Ba↑+BaO+Al2O3。(5)常温下Al的金属性比Ba的金属性
a.高温时Al的活泼性大于Ba b.高温有利于BaO分解
c.高温时BaO·Al2O3比Al2O3稳定 d.Ba的沸点比Al的低
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】硫、硒及其化合物在生产、生活中用途广泛。
I.请根据如图所示价一类二维图,回答下列问题:
(1)Y是引发酸雨的主要污染物,请用离子方程式表示硫酸型酸雨露置于空气中一段时间后溶液酸性变化的原因:___________ 。
(2)若将Y气体通入X水溶液中直至过量,下列表示溶液的pH随通入Y气体体积变化的示意图正确的是___________ (填序号)。
① ②
②
③ ④
④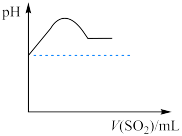
已知:Y对应酸: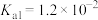 ,X对应酸
,X对应酸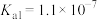 。
。
(3)W的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为___________ 。
(4)欲制备Na2S2O3(硫代硫酸钠),从氧化还原反应角度分析合理的是___________(填序号)。
Ⅱ.为更好地满足吃货们的心愿,丰富舌尖上的营养和美味,很多食物添加了食品添加剂。国家卫健委发布公告称,富硒酵母、二氧化硅、硫黄等6种食品添加剂新品种安全性已通过审查。回答下列问题:
(5)富硒酵母是一种新型添加剂,下列有关硒元素说法正确的是_______ (填字母)。
A.沸点高低:H2Se>H2S>H2O B.硒的非金属性比氧弱,但比溴强
C.热稳定性:H2Se>H2S>H2O D.酸性:HClO3>H2SO4>H2SeO4
E.还原性:Se2->S2-
(6)食品添加剂含有短周期元素A、B、C、D、E、F,其最高正化合价或最低负化合价与原子序数的关系如图所示:
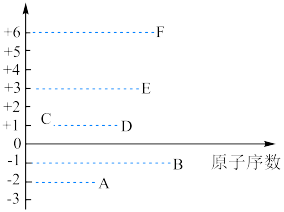
①A、B、C、D、E、F元素形成的简单离子中半径最大的是_______ (用离子符号表示)。
②以下说法不正确的是___________ (填字母)。
A.BA2可用于自来水的消毒
B.A、C形成的一种化合物常用作氧化剂和漂白剂,加热氧化效果更好
C.E、F与A形成的化合物均能与NaOH溶液反应
D.实验室中用CS2洗涤残留在试管壁上的F单质,利用了F单质的还原性
I.请根据如图所示价一类二维图,回答下列问题:

(1)Y是引发酸雨的主要污染物,请用离子方程式表示硫酸型酸雨露置于空气中一段时间后溶液酸性变化的原因:
(2)若将Y气体通入X水溶液中直至过量,下列表示溶液的pH随通入Y气体体积变化的示意图正确的是
①
 ②
②
③
 ④
④
已知:Y对应酸:
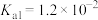 ,X对应酸
,X对应酸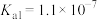 。
。(3)W的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为
(4)欲制备Na2S2O3(硫代硫酸钠),从氧化还原反应角度分析合理的是___________(填序号)。
A. | B. |
C. | D.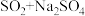 |
Ⅱ.为更好地满足吃货们的心愿,丰富舌尖上的营养和美味,很多食物添加了食品添加剂。国家卫健委发布公告称,富硒酵母、二氧化硅、硫黄等6种食品添加剂新品种安全性已通过审查。回答下列问题:
(5)富硒酵母是一种新型添加剂,下列有关硒元素说法正确的是
A.沸点高低:H2Se>H2S>H2O B.硒的非金属性比氧弱,但比溴强
C.热稳定性:H2Se>H2S>H2O D.酸性:HClO3>H2SO4>H2SeO4
E.还原性:Se2->S2-
(6)食品添加剂含有短周期元素A、B、C、D、E、F,其最高正化合价或最低负化合价与原子序数的关系如图所示:

①A、B、C、D、E、F元素形成的简单离子中半径最大的是
②以下说法不正确的是
A.BA2可用于自来水的消毒
B.A、C形成的一种化合物常用作氧化剂和漂白剂,加热氧化效果更好
C.E、F与A形成的化合物均能与NaOH溶液反应
D.实验室中用CS2洗涤残留在试管壁上的F单质,利用了F单质的还原性
您最近一年使用:0次



