工业废弃物铬钒渣中含有价格相对较高且稀缺的钒(V)、铬(Cr)元素,铬钒渣中铬、钒均以低价含氧酸盐(不溶于水,也不溶于碱性溶液)形式存在,杂质的成分主要为 、
、 、
、 以及磷的化合物。一种从铬钒渣中分离提取铬和钒的流程如图所示:
以及磷的化合物。一种从铬钒渣中分离提取铬和钒的流程如图所示: 与
与 固体能发生反应。
固体能发生反应。
②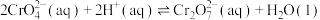 。
。
③25℃时, ,
, ;当溶液中离子浓度小于
;当溶液中离子浓度小于 时,可以认为完全沉淀。
时,可以认为完全沉淀。
(1)“煅烧”时为加快反应速率,可采取的措施为___________ ;“煅烧”时铬元素被氧化为相应的最高价含氧酸盐,则该最高价含氧酸盐中铬元素的化合价为___________ 价。
(2)写出“煅烧”时 与
与 固体反应的化学方程式:
固体反应的化学方程式:___________ 。
(3)试分析,将“浸取”步骤与“沉淀”步骤合并对产品纯度的影响:___________ 。
(4)“还原”时,发生反应的n(氧化剂)∶n(还原剂)=___________ 。
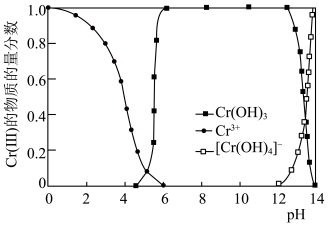
(5)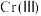 的存在形态的物质的量分数随溶液pH的分布如图。25℃时,通过调节pH使废水中的
的存在形态的物质的量分数随溶液pH的分布如图。25℃时,通过调节pH使废水中的 转化为
转化为 ,溶液中剩余
,溶液中剩余 的浓度小于
的浓度小于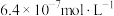 ,则调节pH的范围为
,则调节pH的范围为___________ {已知:25℃时,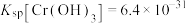 }。
}。 具有两性,溶解在NaOH溶液中得到
具有两性,溶解在NaOH溶液中得到 ,写出该反应的离子方程式:
,写出该反应的离子方程式:___________ ; 在
在 时,转化为
时,转化为 ,向含
,向含 的溶液中加入氨水可得到微溶于水的
的溶液中加入氨水可得到微溶于水的 ,
, 受热最终会分解生成钒的余化物,取234g
受热最终会分解生成钒的余化物,取234g 焙烧,焙烧过程中剩余固体的质量m随温度的变化曲线如图,则b的化学式为
焙烧,焙烧过程中剩余固体的质量m随温度的变化曲线如图,则b的化学式为___________ 。
 、
、 、
、 以及磷的化合物。一种从铬钒渣中分离提取铬和钒的流程如图所示:
以及磷的化合物。一种从铬钒渣中分离提取铬和钒的流程如图所示: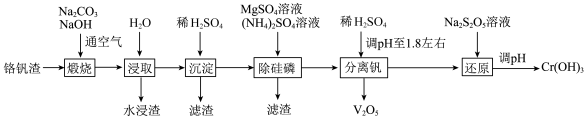
 与
与 固体能发生反应。
固体能发生反应。②
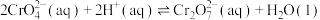 。
。③25℃时,
 ,
, ;当溶液中离子浓度小于
;当溶液中离子浓度小于 时,可以认为完全沉淀。
时,可以认为完全沉淀。(1)“煅烧”时为加快反应速率,可采取的措施为
(2)写出“煅烧”时
 与
与 固体反应的化学方程式:
固体反应的化学方程式:(3)试分析,将“浸取”步骤与“沉淀”步骤合并对产品纯度的影响:
(4)“还原”时,发生反应的n(氧化剂)∶n(还原剂)=
(5)
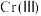 的存在形态的物质的量分数随溶液pH的分布如图。25℃时,通过调节pH使废水中的
的存在形态的物质的量分数随溶液pH的分布如图。25℃时,通过调节pH使废水中的 转化为
转化为 ,溶液中剩余
,溶液中剩余 的浓度小于
的浓度小于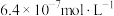 ,则调节pH的范围为
,则调节pH的范围为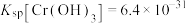 }。
}。
 具有两性,溶解在NaOH溶液中得到
具有两性,溶解在NaOH溶液中得到 ,写出该反应的离子方程式:
,写出该反应的离子方程式: 在
在 时,转化为
时,转化为 ,向含
,向含 的溶液中加入氨水可得到微溶于水的
的溶液中加入氨水可得到微溶于水的 ,
, 受热最终会分解生成钒的余化物,取234g
受热最终会分解生成钒的余化物,取234g 焙烧,焙烧过程中剩余固体的质量m随温度的变化曲线如图,则b的化学式为
焙烧,焙烧过程中剩余固体的质量m随温度的变化曲线如图,则b的化学式为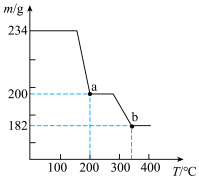
更新时间:2024-05-08 13:08:25
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
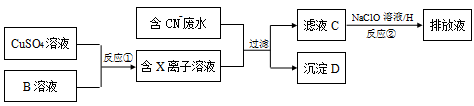
【推荐1】电镀工业中往往产生大量的有毒废水,必须严格处理后才可以排放。含CN-废水在排放前的处理过程如下:
已知:9.0g 沉淀 D 在氧气中灼烧后,产生 8.0g 黑色固体,生成的气体通过足量澄清石灰水时,产生 10.0g 白色沉淀,最后得到的混合气体除去氧气后,还剩余标准状况下密度为 1.25g/L 的单质气体 1.12L。
(1)溶液B具有性质_______________ (填“氧化性”或“还原性”)。
(2)写出沉淀 D 在氧气中灼烧发生的化学方程式___________________________________ 。
(3)滤液 C 中还含有微量的CN-离子,通过反应②,可将其转化为对环境无害的物质,试用离子方程式表示该原理_________________________________ 。
已知:9.0g 沉淀 D 在氧气中灼烧后,产生 8.0g 黑色固体,生成的气体通过足量澄清石灰水时,产生 10.0g 白色沉淀,最后得到的混合气体除去氧气后,还剩余标准状况下密度为 1.25g/L 的单质气体 1.12L。
(1)溶液B具有性质
(2)写出沉淀 D 在氧气中灼烧发生的化学方程式
(3)滤液 C 中还含有微量的CN-离子,通过反应②,可将其转化为对环境无害的物质,试用离子方程式表示该原理
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
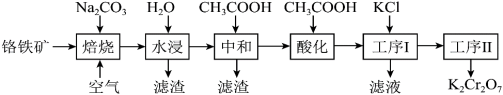
【推荐2】重铬酸钾(K2Cr2O7)是一种重要的化工原料,可用于制铬矾、火柴、铬颜料,并供鞣革、电镀、有机合成等。工业上以铬铁矿[主要成分为Fe(CrO2)2,质量分数为67.2%,杂质主要为硅、铁、铝的氧化物]为原料制备重铬酸钾的工艺流程如图所示:
①焙烧时Fe(CrO2)2中的Fe元素转化为NaFeO2,Cr元素转化为Na2CrO4;铝的氧化物转化为NaAlO2。
②Fe(CrO2)2的摩尔质量为224g/mol,K2Cr2O7的摩尔质量为294g/mol。
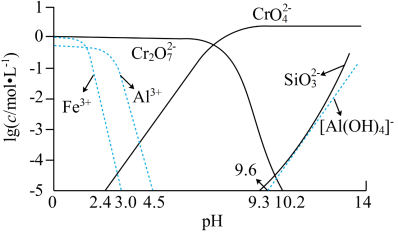
③矿物中相关元素可溶性组分物质的量浓度c(mol•L-1)的对数值与pH的关系如图所示。
请回答下列问题:
(1)写出“焙烧”过程中发生的主要反应的化学方程式:______ 。
(2)“水浸”所得滤渣1的主要成分是Fe(OH)3,写出生成此滤渣的离子方程式:_______ 。
(3)在“中和”步骤中加冰醋酸调节pH约等于7,中和后滤渣2的主要成分是_______ (填化学式)。
(4)“酸化”时加冰醋酸调节pH约等于5,写出酸化过程中发生反应的离子方程式:______ 。
(5)工序I经过滤、洗涤后获得粗产品,经工序Ⅱ得到661.5kg产品,则工序Ⅱ的操作方法是_______ ,生产过程的产率为______ 。
(6)测定产品中K2Cr2O7含量:称取样品2.50g配成250mL溶液,取25.00mL于锥形瓶中,加入足量稀硫酸和几滴指示剂,用0.1000mol•L-1(NH4)2Fe(SO4)2标准液进行滴定。三次实验消耗(NH4)2Fe(SO4)2标准液的平均体积为25.00mL。则样品中K2Cr2O7的纯度为_______ 。(滴定过程中发生的反应为Cr2O +Fe2++H+→Cr3++Fe3++H2O)
+Fe2++H+→Cr3++Fe3++H2O)
①焙烧时Fe(CrO2)2中的Fe元素转化为NaFeO2,Cr元素转化为Na2CrO4;铝的氧化物转化为NaAlO2。
②Fe(CrO2)2的摩尔质量为224g/mol,K2Cr2O7的摩尔质量为294g/mol。
③矿物中相关元素可溶性组分物质的量浓度c(mol•L-1)的对数值与pH的关系如图所示。
请回答下列问题:
(1)写出“焙烧”过程中发生的主要反应的化学方程式:
(2)“水浸”所得滤渣1的主要成分是Fe(OH)3,写出生成此滤渣的离子方程式:
(3)在“中和”步骤中加冰醋酸调节pH约等于7,中和后滤渣2的主要成分是
(4)“酸化”时加冰醋酸调节pH约等于5,写出酸化过程中发生反应的离子方程式:
(5)工序I经过滤、洗涤后获得粗产品,经工序Ⅱ得到661.5kg产品,则工序Ⅱ的操作方法是
(6)测定产品中K2Cr2O7含量:称取样品2.50g配成250mL溶液,取25.00mL于锥形瓶中,加入足量稀硫酸和几滴指示剂,用0.1000mol•L-1(NH4)2Fe(SO4)2标准液进行滴定。三次实验消耗(NH4)2Fe(SO4)2标准液的平均体积为25.00mL。则样品中K2Cr2O7的纯度为
 +Fe2++H+→Cr3++Fe3++H2O)
+Fe2++H+→Cr3++Fe3++H2O)
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
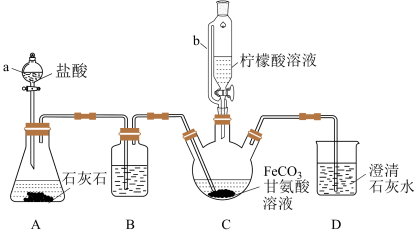
【推荐3】甘氨酸亚铁[(H2NCH2COO)2Fe]是新一代畜禽饲料补铁添加剂。某实验小组以碳酸亚铁和甘氨酸反应制备甘氨酸亚铁的装置如下(夹持和加热仪器略去):
已知:①反应原理为2H2NCH2COOH+FeCO3 (H2NCH2COO)2Fe+CO2↑+H2O。
(H2NCH2COO)2Fe+CO2↑+H2O。
②甘氨酸易溶于水,微溶于乙醇;甘氨酸亚铁易溶于水,难溶于乙醇。
③柠檬酸易溶于水和乙醇,具有较强的还原性和酸性。
实验过程:I.装置C中盛有过量的FeCO3和200mL 1.0 mol·L-1甘氨酸溶液。实验时,先打开仪器a的活塞,待装置C中的空气排净后,加热并不断搅拌;然后向三颈烧瓶中滴加柠檬酸溶液。
II.反应结束后过滤,将滤液进行蒸发浓缩;加入无水乙醇,过滤、洗涤并干燥。
(1)装置B中的试剂为_______ 。
(2)装置A制备CO2的用途是_______ 。
(3)向FeSO4溶液中加入NH4HCO3溶液可制得FeCO3,该反应的离子方程式为_______ 。
(4)过程I加入柠檬酸溶液促进FeCO3溶解并调节溶液pH,溶液pH与甘氨酸亚铁产率的关系如图所示。

①pH过低或过高均导致产率下降,pH过高导致产率下降的原因是_______ 。
②柠檬酸溶液除了起酸性作用外,还有的作用是_______ 。
(5)过程II中加入无水乙醇的目的是_______ 。
(6)本实验制得15.3 g甘氨酸亚铁(Mr=204g/mol),则其产率是_______ %。

已知:①反应原理为2H2NCH2COOH+FeCO3
 (H2NCH2COO)2Fe+CO2↑+H2O。
(H2NCH2COO)2Fe+CO2↑+H2O。②甘氨酸易溶于水,微溶于乙醇;甘氨酸亚铁易溶于水,难溶于乙醇。
③柠檬酸易溶于水和乙醇,具有较强的还原性和酸性。
实验过程:I.装置C中盛有过量的FeCO3和200mL 1.0 mol·L-1甘氨酸溶液。实验时,先打开仪器a的活塞,待装置C中的空气排净后,加热并不断搅拌;然后向三颈烧瓶中滴加柠檬酸溶液。
II.反应结束后过滤,将滤液进行蒸发浓缩;加入无水乙醇,过滤、洗涤并干燥。
(1)装置B中的试剂为
(2)装置A制备CO2的用途是
(3)向FeSO4溶液中加入NH4HCO3溶液可制得FeCO3,该反应的离子方程式为
(4)过程I加入柠檬酸溶液促进FeCO3溶解并调节溶液pH,溶液pH与甘氨酸亚铁产率的关系如图所示。

①pH过低或过高均导致产率下降,pH过高导致产率下降的原因是
②柠檬酸溶液除了起酸性作用外,还有的作用是
(5)过程II中加入无水乙醇的目的是
(6)本实验制得15.3 g甘氨酸亚铁(Mr=204g/mol),则其产率是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】铁粉可用于处理水中污染物。铁粉的氧化物层可以导电。
(1)富铁矿石经破碎、筛分到微米级后,在氢气氛围下 高温还原1小时可以制备微米级铁粉。请写出磁铁矿与氢气反应制备铁的化学方程式:
高温还原1小时可以制备微米级铁粉。请写出磁铁矿与氢气反应制备铁的化学方程式:___________ 。
(2)采用 溶液还原铁盐,可以制备纳米级的铁粉,并生成
溶液还原铁盐,可以制备纳米级的铁粉,并生成 。
。
① 中
中 离子的空间构型为
离子的空间构型为___________ 。
②由 每生成
每生成 ,需要
,需要 物质的量是
物质的量是___________  。
。
(3)利用纳米铁粉可以有效处理废水中的 和
和 ,去除机理如图1所示。
,去除机理如图1所示。
①纳米铁粉去除污水中 和
和 机理不同,请解释原因并简述两者的区别
机理不同,请解释原因并简述两者的区别___________ 。


②由图2可知,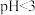 时,随
时,随 减小,
减小, 和
和 去除率减小的原因是
去除率减小的原因是___________ 。
(1)富铁矿石经破碎、筛分到微米级后,在氢气氛围下
 高温还原1小时可以制备微米级铁粉。请写出磁铁矿与氢气反应制备铁的化学方程式:
高温还原1小时可以制备微米级铁粉。请写出磁铁矿与氢气反应制备铁的化学方程式:(2)采用
 溶液还原铁盐,可以制备纳米级的铁粉,并生成
溶液还原铁盐,可以制备纳米级的铁粉,并生成 。
。①
 中
中 离子的空间构型为
离子的空间构型为②由
 每生成
每生成 ,需要
,需要 物质的量是
物质的量是 。
。(3)利用纳米铁粉可以有效处理废水中的
 和
和 ,去除机理如图1所示。
,去除机理如图1所示。①纳米铁粉去除污水中
 和
和 机理不同,请解释原因并简述两者的区别
机理不同,请解释原因并简述两者的区别

②由图2可知,
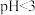 时,随
时,随 减小,
减小, 和
和 去除率减小的原因是
去除率减小的原因是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】实验室用酸性蚀刻废液(含Cu2+、H+、CuC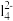 、Cl-等)和碱性蚀刻废液[N
、Cl-等)和碱性蚀刻废液[N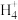 、Cu(NH3
、Cu(NH3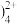 、NH3·H2O等]制备CuI(白色固体)的实验流程如下:
、NH3·H2O等]制备CuI(白色固体)的实验流程如下:

(1)步骤Ⅰ中发生了多个反应,其中Cu(NH3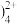 与盐酸反应生成Cu(OH)Cl的离子方程式为
与盐酸反应生成Cu(OH)Cl的离子方程式为______ 。
(2)步骤Ⅳ需控制pH为1~2,80 ℃下进行,合适的加热方式是______ 。
(3)步骤Ⅴ的具体步骤是蒸发浓缩、______ 、____ 。
(4)步骤Ⅵ在下列装置(夹持及加热装置已省略)中进行。
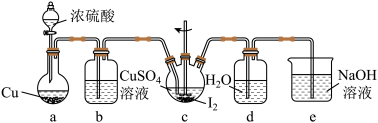
①装置a中盛装浓硫酸的仪器的名称是____ ,圆底烧瓶中发生反应的化学方程式为____ 。
②用装置d中的溶液洗涤制得的CuI的目的是____ ,然后再用无水乙醇洗涤的目的是____ 。
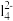 、Cl-等)和碱性蚀刻废液[N
、Cl-等)和碱性蚀刻废液[N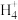 、Cu(NH3
、Cu(NH3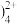 、NH3·H2O等]制备CuI(白色固体)的实验流程如下:
、NH3·H2O等]制备CuI(白色固体)的实验流程如下:
(1)步骤Ⅰ中发生了多个反应,其中Cu(NH3
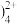 与盐酸反应生成Cu(OH)Cl的离子方程式为
与盐酸反应生成Cu(OH)Cl的离子方程式为(2)步骤Ⅳ需控制pH为1~2,80 ℃下进行,合适的加热方式是
(3)步骤Ⅴ的具体步骤是蒸发浓缩、
(4)步骤Ⅵ在下列装置(夹持及加热装置已省略)中进行。

①装置a中盛装浓硫酸的仪器的名称是
②用装置d中的溶液洗涤制得的CuI的目的是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】工业上利用硫铁矿烧渣(主要成分为 、FeO、
、FeO、 等)为原料制备高档颜料铁红(
等)为原料制备高档颜料铁红( ),具体生产流程如下:
),具体生产流程如下:
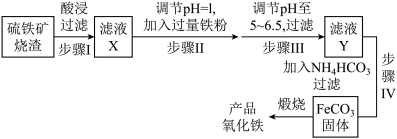
试回答下列问题:
(1)滤液X中含有的金属阳离子是_______ (填离子符号)。
(2)①步骤Ⅱ加入过量铁粉的目的是将_______ 。
②步骤Ⅲ中可选用_______ (填字母)调节溶液的pH。
a.次氯酸钙 b.氨水 c.氢氧化钠溶液 d.高锰酸钾溶液
(3)①步骤Ⅳ加入 时的离子方程式:
时的离子方程式:_______ 。
②步骤Ⅳ的反应温度一般需控制在35℃以下,其目的是_______ 。
③步骤Ⅳ中 沉淀完全后,溶液中含有少量
沉淀完全后,溶液中含有少量 ,检验
,检验 的方法是
的方法是_______ 。
(4)在空气中煅烧 生成产品氧化铁的化学方程式为
生成产品氧化铁的化学方程式为_______ 。
 、FeO、
、FeO、 等)为原料制备高档颜料铁红(
等)为原料制备高档颜料铁红( ),具体生产流程如下:
),具体生产流程如下:
试回答下列问题:
(1)滤液X中含有的金属阳离子是
(2)①步骤Ⅱ加入过量铁粉的目的是将
②步骤Ⅲ中可选用
a.次氯酸钙 b.氨水 c.氢氧化钠溶液 d.高锰酸钾溶液
(3)①步骤Ⅳ加入
 时的离子方程式:
时的离子方程式:②步骤Ⅳ的反应温度一般需控制在35℃以下,其目的是
③步骤Ⅳ中
 沉淀完全后,溶液中含有少量
沉淀完全后,溶液中含有少量 ,检验
,检验 的方法是
的方法是(4)在空气中煅烧
 生成产品氧化铁的化学方程式为
生成产品氧化铁的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
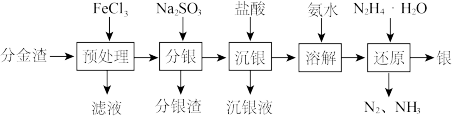
【推荐1】从分金渣(主要成分为AgCl、 、
、 、
、 )中获取高纯银的流程如图所示:
)中获取高纯银的流程如图所示:
已知:在上述反应的温度下 ,
,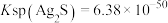
(1)“预处理”加入 溶液将
溶液将 转化为AgCl,反应的化学方程式为
转化为AgCl,反应的化学方程式为___________ 。
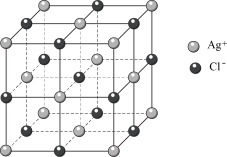
(2)氯化银的晶胞如图, 周围最近且等距离的
周围最近且等距离的 数目为
数目为___________ 。
(3)已知: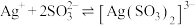 ,
,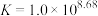 ,“分银”时,AgCl与
,“分银”时,AgCl与 反应生成
反应生成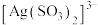 ,该反应的平衡常数
,该反应的平衡常数
___________ 。
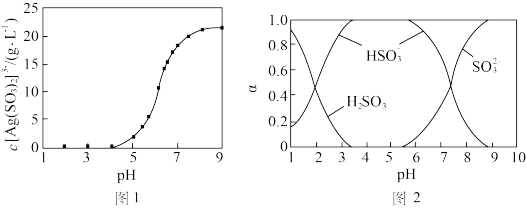
(4)“分银”时,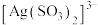 的浓度与溶液pH的关系如图1;
的浓度与溶液pH的关系如图1; 及其与
及其与 形成的微粒的浓度分数
形成的微粒的浓度分数 随溶液pH变化的关系如图2。“分银”时,终点pH需控制的范围及原因为
随溶液pH变化的关系如图2。“分银”时,终点pH需控制的范围及原因为___________ 。
(5)“还原”时发生反应的离子方程式为___________ 。
(6)已如 (白色),测定所制银样品纯度的过程为(杂质不反应):
(白色),测定所制银样品纯度的过程为(杂质不反应):
①称取制备的银样品1.0800g,加适量稀硝酸溶解,定容到100mL容量瓶中。
②准确量取25.00mL溶液于锥形瓶中,酸化后滴入几滴 溶液作指示剂,再用
溶液作指示剂,再用 标准溶液滴定,滴定终点时溶液变为血红色。
标准溶液滴定,滴定终点时溶液变为血红色。
③重复②的操作2次,所用 标准溶液的平均体积为24.00mL。
标准溶液的平均体积为24.00mL。
计算样品中银的质量分数(写出计算过程)___________ 。
 、
、 、
、 )中获取高纯银的流程如图所示:
)中获取高纯银的流程如图所示:
已知:在上述反应的温度下
 ,
,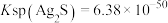
(1)“预处理”加入
 溶液将
溶液将 转化为AgCl,反应的化学方程式为
转化为AgCl,反应的化学方程式为(2)氯化银的晶胞如图,
 周围最近且等距离的
周围最近且等距离的 数目为
数目为
(3)已知:
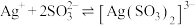 ,
,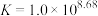 ,“分银”时,AgCl与
,“分银”时,AgCl与 反应生成
反应生成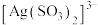 ,该反应的平衡常数
,该反应的平衡常数
(4)“分银”时,
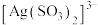 的浓度与溶液pH的关系如图1;
的浓度与溶液pH的关系如图1; 及其与
及其与 形成的微粒的浓度分数
形成的微粒的浓度分数 随溶液pH变化的关系如图2。“分银”时,终点pH需控制的范围及原因为
随溶液pH变化的关系如图2。“分银”时,终点pH需控制的范围及原因为
(5)“还原”时发生反应的离子方程式为
(6)已如
 (白色),测定所制银样品纯度的过程为(杂质不反应):
(白色),测定所制银样品纯度的过程为(杂质不反应):①称取制备的银样品1.0800g,加适量稀硝酸溶解,定容到100mL容量瓶中。
②准确量取25.00mL溶液于锥形瓶中,酸化后滴入几滴
 溶液作指示剂,再用
溶液作指示剂,再用 标准溶液滴定,滴定终点时溶液变为血红色。
标准溶液滴定,滴定终点时溶液变为血红色。③重复②的操作2次,所用
 标准溶液的平均体积为24.00mL。
标准溶液的平均体积为24.00mL。计算样品中银的质量分数(写出计算过程)
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】三氧化二钴(Co2O3)主要用作颜料、釉料、磁性材料、催化剂和氧化剂等。用某工业含钴废料(主要成分为Co2O3,含有少量PbO、NiO、FeO、SiO2) 制备Co2O3和Ni(OH)2的流程如下。

回答下列问题:
(1)滤渣2的主要成分是___________ (填化学式);检验其中阳离子可选用的化学试剂为___________ 。
(2)实验室中进行操作X用到的硅酸盐仪器除酒精灯外还有___________ 、___________ ;萃取分离用到的仪器是___________ 。
(3)“酸浸”时不使用盐酸酸化的原因___________ 。
(4)“酸浸”时H2O2的作用是___________ 。
(5)“沉镍”时发生反应的离子方程式为___________ ;此步骤需加热,温度不能太高也不能太低的原因是___________ 。

回答下列问题:
(1)滤渣2的主要成分是
(2)实验室中进行操作X用到的硅酸盐仪器除酒精灯外还有
(3)“酸浸”时不使用盐酸酸化的原因
(4)“酸浸”时H2O2的作用是
(5)“沉镍”时发生反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】硫铁矿(含 )是一种重要的化学矿物原料,也是工业制硫酸的主要原料,其煅烧过程及产物存在如下转化关系:
)是一种重要的化学矿物原料,也是工业制硫酸的主要原料,其煅烧过程及产物存在如下转化关系:
(1)硫铁矿 中
中 元素的化合价为
元素的化合价为_______________ 。
(2)为了使反应Ⅰ燃烧得更充分,可以采用的措施是_______________ 。(任写一条)
(3)将 通入新制碘水中,发现溶液褪色,发生反应的离子方程式为
通入新制碘水中,发现溶液褪色,发生反应的离子方程式为_______________ 。
(4)下列关于 的说法不正确的是_______________。
的说法不正确的是_______________。
(5)工业上为了防止污染,可以利用氧化亚铁硫杆菌(T.f)对硫铁矿进行催化脱硫,该过程如图所示: ,转移的电子的物质的量为
,转移的电子的物质的量为_______________ 。
②脱硫过程中产生的 在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式
在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式_______________ 。
③在 和
和 的混合液中,可用于检验
的混合液中,可用于检验 的试剂是
的试剂是_______________ 。
a.酸性高锰酸钾溶液 b.硫氰化钾溶液
c.先加入硫氰化钾溶液,再加入过氧化氢 d.氢氧化钠溶液
 )是一种重要的化学矿物原料,也是工业制硫酸的主要原料,其煅烧过程及产物存在如下转化关系:
)是一种重要的化学矿物原料,也是工业制硫酸的主要原料,其煅烧过程及产物存在如下转化关系:
(1)硫铁矿
 中
中 元素的化合价为
元素的化合价为(2)为了使反应Ⅰ燃烧得更充分,可以采用的措施是
(3)将
 通入新制碘水中,发现溶液褪色,发生反应的离子方程式为
通入新制碘水中,发现溶液褪色,发生反应的离子方程式为(4)下列关于
 的说法不正确的是_______________。
的说法不正确的是_______________。| A.浓硫酸有强氧化性,稀硫酸没有氧化性 |
| B.常温下,浓硫酸与铁不反应,故可用铁罐车储运浓硫酸 |
C.浓硫酸具有吸水性,可用于干燥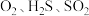 等气体 等气体 |
| D.蔗糖中滴入浓硫酸,可观察到蔗糖由白变黑、体积膨胀并有刺激性气味气体产生,该过程中浓硫酸体现了脱水性和强氧化性 |
(5)工业上为了防止污染,可以利用氧化亚铁硫杆菌(T.f)对硫铁矿进行催化脱硫,该过程如图所示:
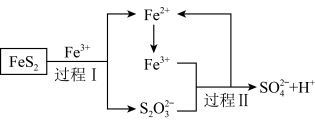
 ,转移的电子的物质的量为
,转移的电子的物质的量为②脱硫过程中产生的
 在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式
在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式③在
 和
和 的混合液中,可用于检验
的混合液中,可用于检验 的试剂是
的试剂是a.酸性高锰酸钾溶液 b.硫氰化钾溶液
c.先加入硫氰化钾溶液,再加入过氧化氢 d.氢氧化钠溶液
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
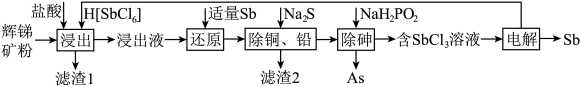
【推荐1】锑(Sb)及其化合物在工业上有许多用途。以辉锑矿(主要成分为Sb2S3,还含有PbS、As2S3、CuO、SiO2等)为原料制备金属锑的工艺流程如图所示:
①浸出液中除了含有少量H[SbCl6]、盐酸外,主要含有SbCl3、PbCl2、AsCl3、CuCl2等;
②常温下:Ksp(CuS)=1.27×10-36,Ksp(PbS)=9.04×10-29;
③溶液中离子浓度小于等于1.0×10-5mol·L-1时,认为该离子沉淀完全。
(1)“浸出”过程中,几乎没有有毒的H2S气体生成,则“浸出”时,Sb2S3发生反应的化学方程式为_____________ ,滤渣的主要成分是______ 。浸出液必须保持强酸性,否则锑元素会以SbOCl形式混入滤渣1中使产率降低,原因是_____________ (用离子方程式表示)。
(2)“还原”时,被Sb还原的物质为___________ (填化学式)。
(3)常温下,“除铜、铅”时,Cu2+和Pb2+均沉淀完全,此时溶液中的c(S2-)不低于__ ;所加Na2S也不宜过多,原因是______ 。
(4)“除砷”时反应的化学方程式为_________ 。
(5)“电解”时,被氧化的Sb元素与被还原的Sb元素的质量之比为____________ 。
①浸出液中除了含有少量H[SbCl6]、盐酸外,主要含有SbCl3、PbCl2、AsCl3、CuCl2等;
②常温下:Ksp(CuS)=1.27×10-36,Ksp(PbS)=9.04×10-29;
③溶液中离子浓度小于等于1.0×10-5mol·L-1时,认为该离子沉淀完全。
(1)“浸出”过程中,几乎没有有毒的H2S气体生成,则“浸出”时,Sb2S3发生反应的化学方程式为
(2)“还原”时,被Sb还原的物质为
(3)常温下,“除铜、铅”时,Cu2+和Pb2+均沉淀完全,此时溶液中的c(S2-)不低于
(4)“除砷”时反应的化学方程式为
(5)“电解”时,被氧化的Sb元素与被还原的Sb元素的质量之比为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
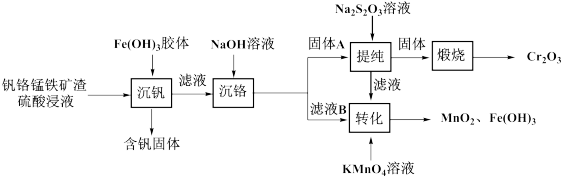
【推荐2】从钒铬锰铁矿渣(主要成分为 、
、 、
、 、
、 )中提
)中提 的一种工艺流程如下:
的一种工艺流程如下:
已知: 开始沉淀的
开始沉淀的 为6.3;
为6.3; 较大时,二价锰
较大时,二价锰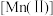 在空气中易被氧化。
在空气中易被氧化。
回答下列问题:
(1) 的电子式为
的电子式为___________ 。
(2)常温下,各种形态五价钒粒子总浓度的对数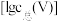 与
与 关系如图一、已知钒铬锰铁矿渣中
关系如图一、已知钒铬锰铁矿渣中 ,“沉钒”过程控制
,“沉钒”过程控制 ,则与胶体共沉降的五价钒粒子的存在形态为
,则与胶体共沉降的五价钒粒子的存在形态为___________ 。(填化学式)

(3)某温度下, Cr(Ⅲ)、Mn(Ⅱ)的沉淀率与 关系如图二、“沉铬”过程最佳
关系如图二、“沉铬”过程最佳 为
为___________ 。此时,滤液B中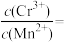
___________ 。 [已知:该温度下,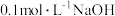 溶液的
溶液的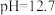 ,
, ,
,
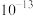 ]
]
(4)“提纯”过程中 的作用为
的作用为___________ 。
(5)“转化”过程中:
①除去 的离子方程式为___________
的离子方程式为___________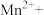 ___________
___________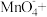 _____
_____ ______
______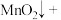 ___________
___________ (配平该方程式)
(配平该方程式) ____ 。
②写出除去 的离子方程式
的离子方程式____ (产物之一为 )。
)。
 、
、 、
、 、
、 )中提
)中提 的一种工艺流程如下:
的一种工艺流程如下:
已知:
 开始沉淀的
开始沉淀的 为6.3;
为6.3; 较大时,二价锰
较大时,二价锰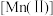 在空气中易被氧化。
在空气中易被氧化。回答下列问题:
(1)
 的电子式为
的电子式为(2)常温下,各种形态五价钒粒子总浓度的对数
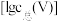 与
与 关系如图一、已知钒铬锰铁矿渣中
关系如图一、已知钒铬锰铁矿渣中 ,“沉钒”过程控制
,“沉钒”过程控制 ,则与胶体共沉降的五价钒粒子的存在形态为
,则与胶体共沉降的五价钒粒子的存在形态为
(3)某温度下, Cr(Ⅲ)、Mn(Ⅱ)的沉淀率与
 关系如图二、“沉铬”过程最佳
关系如图二、“沉铬”过程最佳 为
为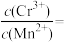
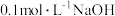 溶液的
溶液的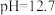 ,
, ,
,
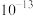 ]
](4)“提纯”过程中
 的作用为
的作用为(5)“转化”过程中:
①除去
 的离子方程式为___________
的离子方程式为___________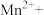 ___________
___________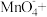 _____
_____ ______
______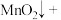 ___________
___________ (配平该方程式)
(配平该方程式) ②写出除去
 的离子方程式
的离子方程式 )。
)。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】 是生产含钼催化剂的重要原料,能溶于氨水和强碱。以钼精矿(主要成分是
是生产含钼催化剂的重要原料,能溶于氨水和强碱。以钼精矿(主要成分是 ,还含有
,还含有 、
、 、
、 、
、 等杂质)为原料制备
等杂质)为原料制备 的工艺流程如图所示:
的工艺流程如图所示: 和
和 发生反应;
发生反应; 元素转化为
元素转化为 、
、 、
、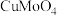 ;
;
②“氨浸”时, 元素以
元素以 的形式进入滤液1中,而
的形式进入滤液1中,而 元素进入滤渣1中;
元素进入滤渣1中;
③ 。
。
回答下列问题:
(1)尾气的成分有 和
和_______ (填化学式)。
(2)“滤渣1”的主要成分是 和
和_______ (填化学式)。
(3)写出“除杂”时反应的离子方程式_______ 。除杂后测得溶液中 ,列式计算并判断
,列式计算并判断 是否沉淀完全
是否沉淀完全_______ 。
(4)“酸沉”时加入 的作用是
的作用是_______ 。
(5)写出四钼酸铵[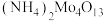 ]发生“焙解”的化学方程式
]发生“焙解”的化学方程式_______ 。
(6) 的结构和
的结构和 相似,如图
相似,如图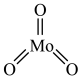 ,易升华,则
,易升华,则 晶体类型为
晶体类型为_______ 。 晶体有多种晶胞,正交相
晶体有多种晶胞,正交相 具有独特的层状结构,层与层之间的作用力为范德华力,根据结构和作用力预测正交相
具有独特的层状结构,层与层之间的作用力为范德华力,根据结构和作用力预测正交相 晶体在日常生活中可用作
晶体在日常生活中可用作_______ 。
(7)工业上还可以在碱性环境下用 溶液和
溶液和 反应制备钼酸盐,同时生成副产品硫酸盐,写出该反应的离子方程式
反应制备钼酸盐,同时生成副产品硫酸盐,写出该反应的离子方程式_______ 。
 是生产含钼催化剂的重要原料,能溶于氨水和强碱。以钼精矿(主要成分是
是生产含钼催化剂的重要原料,能溶于氨水和强碱。以钼精矿(主要成分是 ,还含有
,还含有 、
、 、
、 、
、 等杂质)为原料制备
等杂质)为原料制备 的工艺流程如图所示:
的工艺流程如图所示: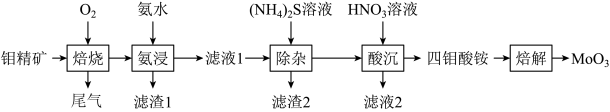
 和
和 发生反应;
发生反应; 元素转化为
元素转化为 、
、 、
、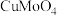 ;
;②“氨浸”时,
 元素以
元素以 的形式进入滤液1中,而
的形式进入滤液1中,而 元素进入滤渣1中;
元素进入滤渣1中;③
 。
。回答下列问题:
(1)尾气的成分有
 和
和(2)“滤渣1”的主要成分是
 和
和(3)写出“除杂”时反应的离子方程式
 ,列式计算并判断
,列式计算并判断 是否沉淀完全
是否沉淀完全(4)“酸沉”时加入
 的作用是
的作用是(5)写出四钼酸铵[
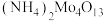 ]发生“焙解”的化学方程式
]发生“焙解”的化学方程式(6)
 的结构和
的结构和 相似,如图
相似,如图 ,易升华,则
,易升华,则 晶体类型为
晶体类型为 晶体有多种晶胞,正交相
晶体有多种晶胞,正交相 具有独特的层状结构,层与层之间的作用力为范德华力,根据结构和作用力预测正交相
具有独特的层状结构,层与层之间的作用力为范德华力,根据结构和作用力预测正交相 晶体在日常生活中可用作
晶体在日常生活中可用作(7)工业上还可以在碱性环境下用
 溶液和
溶液和 反应制备钼酸盐,同时生成副产品硫酸盐,写出该反应的离子方程式
反应制备钼酸盐,同时生成副产品硫酸盐,写出该反应的离子方程式
您最近一年使用:0次



