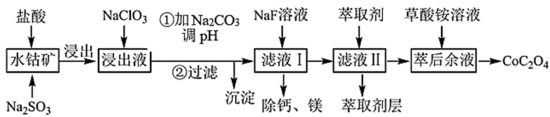
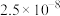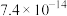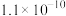利用水钴矿(主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO等)制取草酸钴的工艺流程如下:
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(1)为增大水钴矿的浸取效率,可采取的措施为______ 。(任写一条)
(2)向浸出液中加入NaClO3对应的离子反应方程式为______ ,制取NaClO3可以将氯气通入到热的浓氢氧化钠溶液,该反应的离子方程式为______ ;实验需要制取21.3克NaClO3,需要的氯气由电解食盐水生成,若不考虑反应过程中的损失,则同时生成的氢气的体积为______ (标准状况)。
(3)向浸出液中加入碳酸钠后析出的沉淀是______ ,至少调节pH为______ 。
(4)滤液Ⅱ中加入萃取剂的目的是______ 。
(5)“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀。已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10。当加入过量NaF后,所得滤液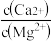 =
=______ 。
(6)取15gCoC2O4样品灼烧(CoC2O4=CoO+CO+CO2,假设杂质不参与变化),将分解产生的气体收集起来得到标况下体积为4.48L的气体,则CoC2O4的纯度为_______ 。
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)为增大水钴矿的浸取效率,可采取的措施为
(2)向浸出液中加入NaClO3对应的离子反应方程式为
(3)向浸出液中加入碳酸钠后析出的沉淀是
(4)滤液Ⅱ中加入萃取剂的目的是
(5)“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀。已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10。当加入过量NaF后,所得滤液
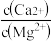 =
=(6)取15gCoC2O4样品灼烧(CoC2O4=CoO+CO+CO2,假设杂质不参与变化),将分解产生的气体收集起来得到标况下体积为4.48L的气体,则CoC2O4的纯度为
更新时间:2024-05-09 14:43:01
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室制取硝基苯常规方法为:在大试管中将浓硝酸和浓硫酸按体积比2:3混合,摇匀、冷却后滴入苯,水浴加热至55℃~60℃,即可制得硝基苯。将该实验进行改进,以N2O5为绿色硝化剂制取硝基苯的反应原理、实验装置及实验步骤如下:
反应方程式: +N2O5
+N2O5
 +HNO3
+HNO3

实验步骤:
Ⅰ.将100mL浓度为0.108g•mL-1N2O5的CH2Cl2溶液加入到装有高选择性分子筛催化剂(NaY)的反应器中。
Ⅱ.在搅拌状态下,将一定量的苯用恒压滴液漏斗滴加至反应器中,使苯与N2O5物质的量之比达到1:1.1,并控制反应温度在15℃以下。
Ⅲ.滴加完毕后继续搅拌一段时间,将反应器中的液体倒入饱和NaHCO3溶液中,分液得到粗产品。
Ⅳ.将粗产品进一步纯化得到硝基苯9.84g。
回答下列问题:
(1)常规法制取硝基苯的化学方程式为___ 。
(2)准确配制100mL浓度为0.108g•mL-1的N2O5的CH2Cl2溶液用到的玻璃仪器有烧杯、玻璃棒、__ 、___ 。
(3)“步骤Ⅲ”中饱和碳酸氢钠溶液的作用是___ 。
(4)“步骤Ⅳ”中“进一步纯化”的方法是___ 。
(5)若忽略提纯过程中硝基苯的损耗,N2O5的转化率为___ 。
反应方程式:
 +N2O5
+N2O5
 +HNO3
+HNO3
实验步骤:
Ⅰ.将100mL浓度为0.108g•mL-1N2O5的CH2Cl2溶液加入到装有高选择性分子筛催化剂(NaY)的反应器中。
Ⅱ.在搅拌状态下,将一定量的苯用恒压滴液漏斗滴加至反应器中,使苯与N2O5物质的量之比达到1:1.1,并控制反应温度在15℃以下。
Ⅲ.滴加完毕后继续搅拌一段时间,将反应器中的液体倒入饱和NaHCO3溶液中,分液得到粗产品。
Ⅳ.将粗产品进一步纯化得到硝基苯9.84g。
回答下列问题:
(1)常规法制取硝基苯的化学方程式为
(2)准确配制100mL浓度为0.108g•mL-1的N2O5的CH2Cl2溶液用到的玻璃仪器有烧杯、玻璃棒、
(3)“步骤Ⅲ”中饱和碳酸氢钠溶液的作用是
(4)“步骤Ⅳ”中“进一步纯化”的方法是
(5)若忽略提纯过程中硝基苯的损耗,N2O5的转化率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】二氧化碳是碳循环中的重要一员,具有广泛的应用价值。
(1)二氧化碳是植物生长必需的物质。草莓大棚中可通过燃烧木炭提供所需的二氧化碳,该反应的化学方程式是_______ 。
(2)实验室制备二氧化碳时,利用下列仪器组装发生装置。
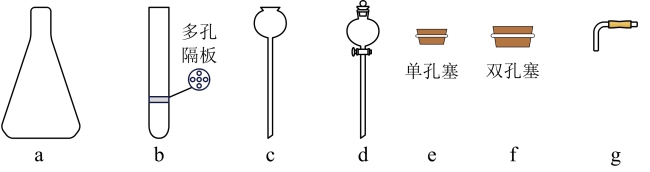
I.实验室制取二氧化碳的方程式为_______ 。
II.选择上述bcfg连接_______ (填“能”或“不能”)实现控制反应的发生与停止。
III.选择上图中a和_______ 组合发生装置,可以使反应平稳进行。
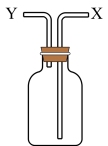
IV.可用下图装置收集CO2时,空气从_______ (填“x”或“y”)排出;验满的方法是_______ 。
(3)工业上利用煅烧大石灰石或酒精(C2H5OH)发酵制二氧化碳。酒精燃烧的方程式为:C2H5OH+3O2 2CO2+3H2O,若消耗1.5mol氧气,可产生二氧化碳
2CO2+3H2O,若消耗1.5mol氧气,可产生二氧化碳_______ g;实验室不用该反应制取二氧化碳的原因是_______ 。
(1)二氧化碳是植物生长必需的物质。草莓大棚中可通过燃烧木炭提供所需的二氧化碳,该反应的化学方程式是
(2)实验室制备二氧化碳时,利用下列仪器组装发生装置。

I.实验室制取二氧化碳的方程式为
II.选择上述bcfg连接
III.选择上图中a和
IV.可用下图装置收集CO2时,空气从

(3)工业上利用煅烧大石灰石或酒精(C2H5OH)发酵制二氧化碳。酒精燃烧的方程式为:C2H5OH+3O2
 2CO2+3H2O,若消耗1.5mol氧气,可产生二氧化碳
2CO2+3H2O,若消耗1.5mol氧气,可产生二氧化碳
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】实验室利用如图所示装置制取并收集氯气。

(1)仪器A的名称为_______
(2)写出B中反应的化学方程式:_______ ,假设理论上有0.5 mol的HCl被氧化,可产生标准状况下的气体体积为_______ L(不考虑损耗)。
(3)次氯酸钠是家用“84”消毒剂的有效成分,写出制取“84”消毒剂的离子方程式:_______ ;假设尾气吸收装置中的NaOH完全与氯气反应得200 mL混合溶液。为了测定有成分的浓度(假设其他成分不参与反应),某兴趣小组进行了如下实验:
①取20 mL溶液,调pH至溶液呈酸性,加入 溶液,充分反应的离子方程式:
溶液,充分反应的离子方程式: (未配平)。
(未配平)。
②向上述反应后的溶液中滴加 溶液20.00 mL,恰好完全反应(此条件下
溶液20.00 mL,恰好完全反应(此条件下 不参与反应)的离子方程式:
不参与反应)的离子方程式: (未配平)。
(未配平)。
则次氯酸钠的物质的量浓度为_______ 。

(1)仪器A的名称为
(2)写出B中反应的化学方程式:
(3)次氯酸钠是家用“84”消毒剂的有效成分,写出制取“84”消毒剂的离子方程式:
①取20 mL溶液,调pH至溶液呈酸性,加入
 溶液,充分反应的离子方程式:
溶液,充分反应的离子方程式: (未配平)。
(未配平)。②向上述反应后的溶液中滴加
 溶液20.00 mL,恰好完全反应(此条件下
溶液20.00 mL,恰好完全反应(此条件下 不参与反应)的离子方程式:
不参与反应)的离子方程式: (未配平)。
(未配平)。则次氯酸钠的物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】实验室常用如下装置制取溴乙烷。在圆底烧瓶中加入溴化钠、浓H2SO4、乙醇和适量的水,加热可收集到溴乙烷。所涉及的有关物质的物理性质见下表:

(1)写出用此法制备溴乙烷的化学方程式:
① NaBr + H2SO4 NaHSO4 + HBr;
NaHSO4 + HBr;
②_______ 。
(2)浓H2SO4在本实验中的作用是_______ ,其用量(物质的量)应_______ (填“大”“小”或“等”)于NaBr的用量。
(3)反应物中加入适量水,除了溶解NaBr使反应物接触更充分外,还可以_______ (任写一条)。
(4)下列最适宜作为溴乙烷收集装置的是_______ (选填编号)。
(5)制得的粗溴乙烷中会含有少量杂质Br2而呈黄色,可先用NaHSO3溶液洗涤,再水洗干燥后蒸馏。洗涤过程用到的主要玻璃仪器是_______ 。完成NaHSO3溶液洗涤时发生反应的离子方程式并标明电子转移方向和数目:_______ 。□HSO + □Br2 + □_______ → □SO
+ □Br2 + □_______ → □SO + □Br- + □H+
+ □Br- + □H+
能否改用氢氧化钠溶液洗涤粗溴乙烷?_______ (填“可以”或“不可以”),原因是_______ 。

| 乙醇 | 溴乙烷 | |
| 沸点(℃) | 78 | 38.4 |
| 密度(g/cm3) | 0.79 | 1.45 |
| 水溶性 | 互溶 | 不溶 |
① NaBr + H2SO4
 NaHSO4 + HBr;
NaHSO4 + HBr;②
(2)浓H2SO4在本实验中的作用是
(3)反应物中加入适量水,除了溶解NaBr使反应物接触更充分外,还可以
(4)下列最适宜作为溴乙烷收集装置的是
 |  |  |  |
| a | b | c | d |
 + □Br2 + □_______ → □SO
+ □Br2 + □_______ → □SO + □Br- + □H+
+ □Br- + □H+能否改用氢氧化钠溶液洗涤粗溴乙烷?
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】高铁酸钾( )是一种新型高效的水处理剂,在碱性溶液中较稳定。工业上有干法与湿法两种制备高铁酸钾的方法。
)是一种新型高效的水处理剂,在碱性溶液中较稳定。工业上有干法与湿法两种制备高铁酸钾的方法。
(1)高铁酸钾( )具有
)具有___________ 性,可以用于杀菌消毒,其在消毒后可形成 胶体,常用于处理饮用水。
胶体,常用于处理饮用水。
(2)干法制备高铁酸钾( )时先制备高铁酸钠(
)时先制备高铁酸钠( ),制备过程中发生的反应为
),制备过程中发生的反应为 ,该反应中氧化剂是
,该反应中氧化剂是___________ (填化学式)。每生成 转移电子的物质的量为
转移电子的物质的量为___________ mol。
(3)湿法制备高铁酸钾的流程如下图
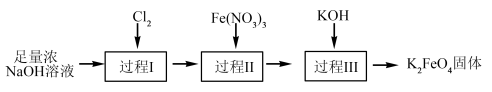
①过程Ⅱ为碱性条件下制备高铁酸钠( )。补全过程Ⅱ中发生反应的离子方程式,并用单线桥表示电子转移的情况:
)。补全过程Ⅱ中发生反应的离子方程式,并用单线桥表示电子转移的情况:___________ 。
______ ______
______ ______=______
______=______ ______
______ ______
______
②过程Ⅲ的反应能够发生的原因是___________ 。
③湿法制备 时,不同的温度下,不同质量浓度的
时,不同的温度下,不同质量浓度的 对
对 生成率有不同影响,由图可知工业生产中最佳条件(温度和
生成率有不同影响,由图可知工业生产中最佳条件(温度和 的质量浓度)为
的质量浓度)为___________ (填选项符号)。
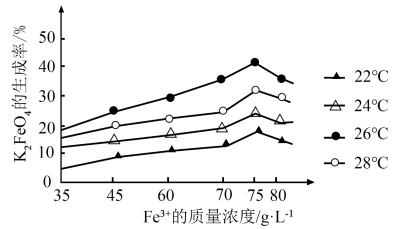
a.24℃,75g∙L-1 b.26℃,75g∙L-1 c.28℃,75g∙L-1 d.22℃,80g∙L-1
 )是一种新型高效的水处理剂,在碱性溶液中较稳定。工业上有干法与湿法两种制备高铁酸钾的方法。
)是一种新型高效的水处理剂,在碱性溶液中较稳定。工业上有干法与湿法两种制备高铁酸钾的方法。(1)高铁酸钾(
 )具有
)具有 胶体,常用于处理饮用水。
胶体,常用于处理饮用水。(2)干法制备高铁酸钾(
 )时先制备高铁酸钠(
)时先制备高铁酸钠( ),制备过程中发生的反应为
),制备过程中发生的反应为 ,该反应中氧化剂是
,该反应中氧化剂是 转移电子的物质的量为
转移电子的物质的量为(3)湿法制备高铁酸钾的流程如下图

①过程Ⅱ为碱性条件下制备高铁酸钠(
 )。补全过程Ⅱ中发生反应的离子方程式,并用单线桥表示电子转移的情况:
)。补全过程Ⅱ中发生反应的离子方程式,并用单线桥表示电子转移的情况:______
 ______
______ ______=______
______=______ ______
______ ______
______②过程Ⅲ的反应能够发生的原因是
③湿法制备
 时,不同的温度下,不同质量浓度的
时,不同的温度下,不同质量浓度的 对
对 生成率有不同影响,由图可知工业生产中最佳条件(温度和
生成率有不同影响,由图可知工业生产中最佳条件(温度和 的质量浓度)为
的质量浓度)为
a.24℃,75g∙L-1 b.26℃,75g∙L-1 c.28℃,75g∙L-1 d.22℃,80g∙L-1
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】工厂烟气(主要污染物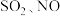 )直接排放会造成空气污染,需处理后才能排放。
)直接排放会造成空气污染,需处理后才能排放。
(1) 氧化。
氧化。 氧化过程中部分反应的能量变化如图所示。
氧化过程中部分反应的能量变化如图所示。

已知 ,则反应
,则反应
___________  。
。
(2)“纳米零价铁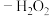 ”体系可将烟气中难溶的
”体系可将烟气中难溶的 氧化为可溶的
氧化为可溶的 。在一定温度下,将
。在一定温度下,将 溶液和
溶液和 溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的
溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的 氧化。
氧化。
① 催化
催化 分解产生
分解产生 ,
, 将
将 氧化为
氧化为 的机理如图所示,Y的化学式为
的机理如图所示,Y的化学式为_____ 。

② 与
与 反应生成
反应生成 的化学方程式为
的化学方程式为___________ 。
③纳米零价铁的作用是___________ 。
④ 脱除率随温度的变化如图所示。温度高于120℃时,
脱除率随温度的变化如图所示。温度高于120℃时, 脱除率随温度升高呈现下降趋势的主要原因是
脱除率随温度升高呈现下降趋势的主要原因是___________ 。

(3) 和
和 等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
① 的处理。
的处理。 是硝酸生产中氨催化氧化的副产物,用特种催化剂能使
是硝酸生产中氨催化氧化的副产物,用特种催化剂能使 分解。
分解。 与
与 在加热和催化剂作用下生成
在加热和催化剂作用下生成 的化学方程式为
的化学方程式为___________ 。
② 和
和 的处理。已除去
的处理。已除去 的硝酸尾气可用
的硝酸尾气可用 溶液吸收,主要反应:
溶液吸收,主要反应:

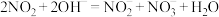
下列措施能提高尾气中 和
和 去除率的有
去除率的有___________ (填字母)。
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量 溶液
溶液
(4) 的氧化吸收。用
的氧化吸收。用 溶液吸收硝酸尾气,可提高尾气中
溶液吸收硝酸尾气,可提高尾气中 的去除率。其他条件相同,
的去除率。其他条件相同, 转化为
转化为 的转化率随
的转化率随 溶液初始
溶液初始 (用稀盐酸调节)的变化如图所示。
(用稀盐酸调节)的变化如图所示。

①在酸性 溶液中,
溶液中, 氧化
氧化 生成
生成 和
和 ,其离子方程式为
,其离子方程式为___________ 。
② 溶液的初始
溶液的初始 越小,
越小, 转化率越高。其原因是
转化率越高。其原因是___________ 。
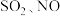 )直接排放会造成空气污染,需处理后才能排放。
)直接排放会造成空气污染,需处理后才能排放。(1)
 氧化。
氧化。 氧化过程中部分反应的能量变化如图所示。
氧化过程中部分反应的能量变化如图所示。
已知
 ,则反应
,则反应
 。
。(2)“纳米零价铁
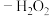 ”体系可将烟气中难溶的
”体系可将烟气中难溶的 氧化为可溶的
氧化为可溶的 。在一定温度下,将
。在一定温度下,将 溶液和
溶液和 溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的
溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的 氧化。
氧化。①
 催化
催化 分解产生
分解产生 ,
, 将
将 氧化为
氧化为 的机理如图所示,Y的化学式为
的机理如图所示,Y的化学式为
②
 与
与 反应生成
反应生成 的化学方程式为
的化学方程式为③纳米零价铁的作用是
④
 脱除率随温度的变化如图所示。温度高于120℃时,
脱除率随温度的变化如图所示。温度高于120℃时, 脱除率随温度升高呈现下降趋势的主要原因是
脱除率随温度升高呈现下降趋势的主要原因是
(3)
 和
和 等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。①
 的处理。
的处理。 是硝酸生产中氨催化氧化的副产物,用特种催化剂能使
是硝酸生产中氨催化氧化的副产物,用特种催化剂能使 分解。
分解。 与
与 在加热和催化剂作用下生成
在加热和催化剂作用下生成 的化学方程式为
的化学方程式为②
 和
和 的处理。已除去
的处理。已除去 的硝酸尾气可用
的硝酸尾气可用 溶液吸收,主要反应:
溶液吸收,主要反应:
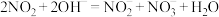
下列措施能提高尾气中
 和
和 去除率的有
去除率的有A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量
 溶液
溶液(4)
 的氧化吸收。用
的氧化吸收。用 溶液吸收硝酸尾气,可提高尾气中
溶液吸收硝酸尾气,可提高尾气中 的去除率。其他条件相同,
的去除率。其他条件相同, 转化为
转化为 的转化率随
的转化率随 溶液初始
溶液初始 (用稀盐酸调节)的变化如图所示。
(用稀盐酸调节)的变化如图所示。
①在酸性
 溶液中,
溶液中, 氧化
氧化 生成
生成 和
和 ,其离子方程式为
,其离子方程式为②
 溶液的初始
溶液的初始 越小,
越小, 转化率越高。其原因是
转化率越高。其原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】废旧铅蓄电池的铅膏中主要含有 、
、 、
、 和
和 ,还有少量
,还有少量 、
、 、
、 的盐或氧化物等,通过下图流程实现铅的回收。
的盐或氧化物等,通过下图流程实现铅的回收。

一些难溶电解质的溶度积常数如下表:
(1)在“脱硫”中 转化反应的离子方程式为
转化反应的离子方程式为___________ ,用沉淀溶解平衡原理解释选择 的原因
的原因_________ 。
(2)在“脱硫”中,加入 不能使铅膏中
不能使铅膏中 完全转化,原因是
完全转化,原因是_______ 。
 、
、 、
、 和
和 ,还有少量
,还有少量 、
、 、
、 的盐或氧化物等,通过下图流程实现铅的回收。
的盐或氧化物等,通过下图流程实现铅的回收。
一些难溶电解质的溶度积常数如下表:
难溶电解质 |
|
|
|
|
|
|
|
|
|
(1)在“脱硫”中
 转化反应的离子方程式为
转化反应的离子方程式为 的原因
的原因(2)在“脱硫”中,加入
 不能使铅膏中
不能使铅膏中 完全转化,原因是
完全转化,原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】湿法炼锌综合回收系统的萃余液中含有 、
、 、
、 ,还含有
,还含有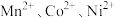 、
、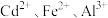 等,一种将萃余液中有价离子分步分离、富集回收的工艺流程如下:
等,一种将萃余液中有价离子分步分离、富集回收的工艺流程如下:

(1)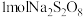 中过氧键的数目为
中过氧键的数目为___________  (设
(设 为阿伏加德罗常数的值);其氧化
为阿伏加德罗常数的值);其氧化 的离子方程式为
的离子方程式为___________ 。
(2)常温下,部分难溶化合物的溶度积相关数据如下表所示:
“调 ”时,应控制
”时,应控制 的范围为
的范围为___________ 。(已知溶液中 ;当溶液中某离子浓度
;当溶液中某离子浓度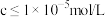 时,可视为沉淀完全)
时,可视为沉淀完全)
(3)“除镉”时所得“滤渣2”主要成分为___________ (写化学式)。
(4)“沉锌”时有气体生成,则生成碱式碳酸锌的离子方程式为___________ 。
(5)“沉锌”所得滤液经处理可得 溶液,已知
溶液,已知 的溶解度随温度变化如图1所示,由该溶液制备芒硝
的溶解度随温度变化如图1所示,由该溶液制备芒硝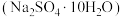 的操作为
的操作为___________ 、过滤、洗涤、干燥。
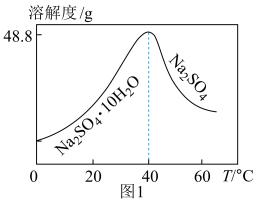
(6)一种 的立方晶胞结构如图2所示,已知晶胞参数为
的立方晶胞结构如图2所示,已知晶胞参数为 ,密度为
,密度为 ,则NA=
,则NA=________ mol-1(用含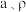 的计算表达式表示)。
的计算表达式表示)。

 、
、 、
、 ,还含有
,还含有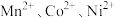 、
、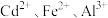 等,一种将萃余液中有价离子分步分离、富集回收的工艺流程如下:
等,一种将萃余液中有价离子分步分离、富集回收的工艺流程如下:
(1)
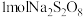 中过氧键的数目为
中过氧键的数目为 (设
(设 为阿伏加德罗常数的值);其氧化
为阿伏加德罗常数的值);其氧化 的离子方程式为
的离子方程式为(2)常温下,部分难溶化合物的溶度积相关数据如下表所示:
| 化合物 |  |  |  |
 近似值 近似值 | 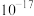 | 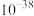 |  |
 ”时,应控制
”时,应控制 的范围为
的范围为 ;当溶液中某离子浓度
;当溶液中某离子浓度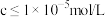 时,可视为沉淀完全)
时,可视为沉淀完全)(3)“除镉”时所得“滤渣2”主要成分为
(4)“沉锌”时有气体生成,则生成碱式碳酸锌的离子方程式为
(5)“沉锌”所得滤液经处理可得
 溶液,已知
溶液,已知 的溶解度随温度变化如图1所示,由该溶液制备芒硝
的溶解度随温度变化如图1所示,由该溶液制备芒硝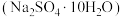 的操作为
的操作为
(6)一种
 的立方晶胞结构如图2所示,已知晶胞参数为
的立方晶胞结构如图2所示,已知晶胞参数为 ,密度为
,密度为 ,则NA=
,则NA=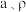 的计算表达式表示)。
的计算表达式表示)。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】菱镁矿的主要成分为MgCO3还含少量SiO2、Fe2O3和Al2O3。工业上利用菱镁矿冶炼镁的路径有两种,具体工业流程如下图。

回答下列问题:
(1)“煅烧”时,需将菱镁矿破碎,并将热空气从底部吹入,这两种操作的优点为___________ 。
(2)工艺I中所得“废渣”中含钙成分有___________ (填化学式)。
(3)工艺II中“浸出”操作中溶解氧化镁的离子方程式为___________ 。
(4)“沉镁”操作中温度不宜过高,原因为___________ 。
(5)“沉镁”过程中当镁离子沉淀完全时,溶液中c(NH ):c(NH3·H2O)至少为
):c(NH3·H2O)至少为___________ (填计算结果)。(已知Kb(NH3·H2O)=1.6×10-5;Ksp[Mg(OH)2]=1.0×10-11;当溶液中离子浓度小于1.0×10-5×mol·L-1时,认为该离子沉淀完全。)
(6)“操作”具体是指___________ 。
(7)“熔融电解”时阳极的电极反应式为___________ 。

回答下列问题:
(1)“煅烧”时,需将菱镁矿破碎,并将热空气从底部吹入,这两种操作的优点为
(2)工艺I中所得“废渣”中含钙成分有
(3)工艺II中“浸出”操作中溶解氧化镁的离子方程式为
(4)“沉镁”操作中温度不宜过高,原因为
(5)“沉镁”过程中当镁离子沉淀完全时,溶液中c(NH
 ):c(NH3·H2O)至少为
):c(NH3·H2O)至少为(6)“操作”具体是指
(7)“熔融电解”时阳极的电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】过氧化钙晶体﹝CaO2·8H2O﹞较稳定,呈白色,微溶于水,广泛应用于环境杀菌、消毒, 也在食品、牙膏、化妆品等制造中用作添加剂,还可以作为鱼池增氧剂。现以贝壳为原料制备CaO2流程如下:

(1)将过氧化钙晶体与溶液分离的方法是_____ 。
(2)我国制碱工业的先驱侯德榜先生为纯碱和氮肥工业技术的发展做出了杰出的贡献。其制备 原料有气体 X、氨气、精制饱和食盐水,过程主要是先制得小苏打,再过滤并加热分解小苏打制得纯碱。
①实验过程中应该先向精制饱和食盐水中通入_____ ,其原因是_____ 。
②请写出制备纯碱第一步发生的化学方程式_____ 。
(3)反应Y 不能在较高温度下进行的原因是_____ ; 已知该反应是化合反应,则反应 Y 的化学方程式是___________________ ;获得的过氧化钙晶体中常含有 Ca(OH)2 杂质,原因是_________ 。
(4)现设计如下实验测定制得的过氧化钙晶体[CaO2·8H2O]中 CaO2 的质量分数:称取晶体样品25 g,加热到 220℃充分分解,其产物含有参与反应 Y 的固体物质和能使带火星木条复燃的气体等(此时所得气体混合物的总质量为1.6 g)(已知杂质不发生变化),则该晶体样品中 CaO2 的质量分数是_____ 。

(1)将过氧化钙晶体与溶液分离的方法是
(2)我国制碱工业的先驱侯德榜先生为纯碱和氮肥工业技术的发展做出了杰出的贡献。其制备 原料有气体 X、氨气、精制饱和食盐水,过程主要是先制得小苏打,再过滤并加热分解小苏打制得纯碱。
①实验过程中应该先向精制饱和食盐水中通入
②请写出制备纯碱第一步发生的化学方程式
(3)反应Y 不能在较高温度下进行的原因是
(4)现设计如下实验测定制得的过氧化钙晶体[CaO2·8H2O]中 CaO2 的质量分数:称取晶体样品25 g,加热到 220℃充分分解,其产物含有参与反应 Y 的固体物质和能使带火星木条复燃的气体等(此时所得气体混合物的总质量为1.6 g)(已知杂质不发生变化),则该晶体样品中 CaO2 的质量分数是
您最近一年使用:0次
【推荐2】由黏土(主要成分Al2O3·2SiO2·2H2O,含少量Fe2O3、CaO、MgO等杂质)与磷肥生产的含氟废气生产冰晶石Na3AlF6的工艺流程如下:
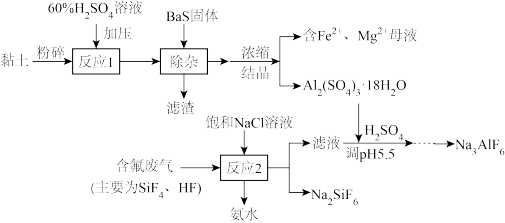
请回答下列问题:
(1) 冰晶石在电解Al2O3制铝中的作用是______ ,需定期更换石墨______ (填“阳”或“阴”)极。
(2) 不用98%硫酸进行“反应1”的可能原因是______ 。
A.不易发生离子反应,造成浸出率下降
B.反应速率太快太剧烈,造成了操作危险
C.产生较多酸性废液,也提高了原料成本
(3) 保持其他条件不变,反应1的铝浸出率在不同温度下随时间变化如图所示。“反应1”的最佳温度与时间分别是______ ℃、______ min。

(4) “除杂”步骤产生的“滤渣”中含有BaSO4、CaSO4、S等难溶物,写出产生S的离子方程式______ 。
(5) 若按“黏土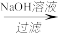 滤液
滤液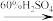 溶液
溶液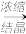 ”来制备Al2(SO4)3·18H2O,该方案的原料利用率比原方案更
”来制备Al2(SO4)3·18H2O,该方案的原料利用率比原方案更______ (填“高”或“低”)。
(6) “反应2”所得“滤液”中含氟物质主要为______ (写化学式)。
(7) 已知Ka(HF)= 6.4×10-4,Al3++ 6F- AlF
AlF 的K=1.0×1019,欲使平衡时c(AlF
的K=1.0×1019,欲使平衡时c(AlF )/c(Al3+)≥10,且调节并维持滤液pH=5.5,则其中HF平衡浓度应不低于
)/c(Al3+)≥10,且调节并维持滤液pH=5.5,则其中HF平衡浓度应不低于______ mol/L(保留2位有效数字,100.5≈ 3.2)。

请回答下列问题:
(1) 冰晶石在电解Al2O3制铝中的作用是
(2) 不用98%硫酸进行“反应1”的可能原因是
A.不易发生离子反应,造成浸出率下降
B.反应速率太快太剧烈,造成了操作危险
C.产生较多酸性废液,也提高了原料成本
(3) 保持其他条件不变,反应1的铝浸出率在不同温度下随时间变化如图所示。“反应1”的最佳温度与时间分别是

(4) “除杂”步骤产生的“滤渣”中含有BaSO4、CaSO4、S等难溶物,写出产生S的离子方程式
(5) 若按“黏土
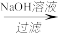 滤液
滤液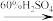 溶液
溶液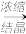 ”来制备Al2(SO4)3·18H2O,该方案的原料利用率比原方案更
”来制备Al2(SO4)3·18H2O,该方案的原料利用率比原方案更(6) “反应2”所得“滤液”中含氟物质主要为
(7) 已知Ka(HF)= 6.4×10-4,Al3++ 6F-
 AlF
AlF 的K=1.0×1019,欲使平衡时c(AlF
的K=1.0×1019,欲使平衡时c(AlF )/c(Al3+)≥10,且调节并维持滤液pH=5.5,则其中HF平衡浓度应不低于
)/c(Al3+)≥10,且调节并维持滤液pH=5.5,则其中HF平衡浓度应不低于
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】海水中含有丰富的自然资源,溶解着大量的 、
、 、
、 、
、 、
、 元素,其化合物在工农业生产中用途广泛,从海水中提取液溴的同时制取
元素,其化合物在工农业生产中用途广泛,从海水中提取液溴的同时制取 晶体的流程如下:
晶体的流程如下:
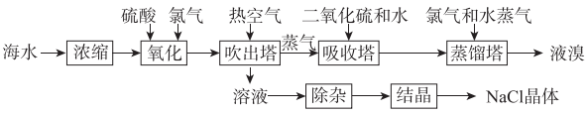
回答下列问题:
(1)“浓缩”的目的是___________ (任答1条即可)。
(2)流程中可用热空气吹出溴的原因为___________ (填选项字母)。
A.溴的氧化性较强 B.溴的熔点较低 C.溴的挥发性较强 D.溴在水中的溶解度较低
(3)上述流程中涉及的氧化还原反应有___________ 个。
(4)“吸收塔”中发生反应的离子方程式为___________ 。
(5)根据除杂原理,在表中填写“除杂”时依次添加的试剂及其预期除去的离子。
(6)制取 晶体的“结晶”操作为
晶体的“结晶”操作为___________ 。
 、
、 、
、 、
、 、
、 元素,其化合物在工农业生产中用途广泛,从海水中提取液溴的同时制取
元素,其化合物在工农业生产中用途广泛,从海水中提取液溴的同时制取 晶体的流程如下:
晶体的流程如下:
回答下列问题:
(1)“浓缩”的目的是
(2)流程中可用热空气吹出溴的原因为
A.溴的氧化性较强 B.溴的熔点较低 C.溴的挥发性较强 D.溴在水中的溶解度较低
(3)上述流程中涉及的氧化还原反应有
(4)“吸收塔”中发生反应的离子方程式为
(5)根据除杂原理,在表中填写“除杂”时依次添加的试剂及其预期除去的离子。
| 实验步骤 | 试剂 | 预期除去的离子 |
| 步骤1 |  |  |
| 步骤2 | ① | ② |
| 步骤3 |  | ③ |
| 步骤4 | ④ |  |
(6)制取
 晶体的“结晶”操作为
晶体的“结晶”操作为
您最近一年使用:0次