利用管状透氧膜反应器实现乙醇-水重整制氢,具有无需额外热源、氧气可协助消除积碳等优点。其主要反应为:
反应Ⅰ: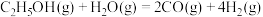
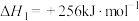
反应Ⅱ:
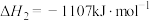
反应Ⅲ:
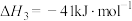
反应Ⅳ:

一定温度下,将一定比例的 、
、 、Ar气体通过装有催化剂的管状透氧膜反应器。经计算机仿真模拟,控制
、Ar气体通过装有催化剂的管状透氧膜反应器。经计算机仿真模拟,控制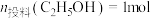 ,平衡时氢醇比
,平衡时氢醇比 随水醇比
随水醇比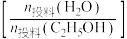 、膜管长度的变化如题13图所示。若仅考虑上述反应,下列说法正确的是
、膜管长度的变化如题13图所示。若仅考虑上述反应,下列说法正确的是
反应Ⅰ:
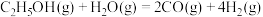
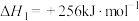
反应Ⅱ:

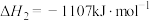
反应Ⅲ:

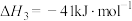
反应Ⅳ:


一定温度下,将一定比例的
 、
、 、Ar气体通过装有催化剂的管状透氧膜反应器。经计算机仿真模拟,控制
、Ar气体通过装有催化剂的管状透氧膜反应器。经计算机仿真模拟,控制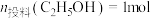 ,平衡时氢醇比
,平衡时氢醇比 随水醇比
随水醇比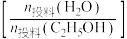 、膜管长度的变化如题13图所示。若仅考虑上述反应,下列说法正确的是
、膜管长度的变化如题13图所示。若仅考虑上述反应,下列说法正确的是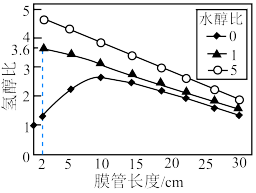
A.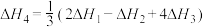 |
B.水醇比为0时,管长度超过10cm后氢醇比下降的原因可能为 氧化 氧化 |
C.水醇比为1、管长度为2cm,若 、 、 转化率为100%且 转化率为100%且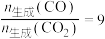 ,则管状透氧膜透过氧气0.1mol ,则管状透氧膜透过氧气0.1mol |
| D.实际生产中,水醇比越大、管长度越短,氢气产率越高 |
2024·江苏南京·二模 查看更多[2]
更新时间:2024-05-23 15:58:34
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】已知以下的热化学反应方程式:
Fe2O3(s)+1/3CO(g) = 2/3Fe3O4(s)+1/3CO2(g) ΔH=-15.73 kJ/mol
Fe3O4(s)+CO(g) = 3FeO(s)+CO2(g) ΔH=+640.4 kJ/mol
Fe2O3(s)+3CO(g) = 2Fe(s)+3CO2(g) ΔH=-24.8 kJ/mol
则42 g CO气体还原足量FeO固体得到Fe固体和CO2气体时对应的ΔH约为
Fe2O3(s)+1/3CO(g) = 2/3Fe3O4(s)+1/3CO2(g) ΔH=-15.73 kJ/mol
Fe3O4(s)+CO(g) = 3FeO(s)+CO2(g) ΔH=+640.4 kJ/mol
Fe2O3(s)+3CO(g) = 2Fe(s)+3CO2(g) ΔH=-24.8 kJ/mol
则42 g CO气体还原足量FeO固体得到Fe固体和CO2气体时对应的ΔH约为
| A.-327 kJ/mol | B.+327 kJ/mol | C.-218 kJ/mol | D.+218 kJ/mol |
您最近一年使用:0次
【推荐2】N2O和CO是环境污染性气体,可在Pt2O+表面转化为无害气体,其反应为:N2O(g)+CO(g) CO2(g)+N2(g) ΔH,有关化学反应的物质变化过程如图1,能量变化过程如图2。下列说法正确的是
CO2(g)+N2(g) ΔH,有关化学反应的物质变化过程如图1,能量变化过程如图2。下列说法正确的是

 CO2(g)+N2(g) ΔH,有关化学反应的物质变化过程如图1,能量变化过程如图2。下列说法正确的是
CO2(g)+N2(g) ΔH,有关化学反应的物质变化过程如图1,能量变化过程如图2。下列说法正确的是
| A.由图1可知:ΔH1=ΔH+ΔH2 |
| B.由图2 可知:ΔH=-226 kJ/mol |
| C.由图2可知:反应①的反应速率比反应②快 |
| D.为了实现转化需不断向反应器中补充Pt2O+和Pt2O2+ |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下。已知N2(g)+3H2(g) 2NH3(g)ΔH=-92.4 kJ·mol-1.下列说法正确的是( )
2NH3(g)ΔH=-92.4 kJ·mol-1.下列说法正确的是( )
 2NH3(g)ΔH=-92.4 kJ·mol-1.下列说法正确的是( )
2NH3(g)ΔH=-92.4 kJ·mol-1.下列说法正确的是( )| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1 mol N2、3 mol H2 | 2 mol NH3 | 4 mol NH3 |
| NH3的浓度 | c1 | c2 | c3 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | α1 | α2 | α3 |
| A.2c1 = c3 | B.a+b = 92.4 | C.2p2 = p3 | D.α1+α3 = 1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】容积均为1L的甲、乙两个恒容容器中,分别充入2molA、2molB和1molA、1molB,相同条件下,发生下列反应:A(g)+B(g) xC(g) △H<0。测得两容器中c(A)随时间t的变化如图所示,下列说法不正确的是
xC(g) △H<0。测得两容器中c(A)随时间t的变化如图所示,下列说法不正确的是
 xC(g) △H<0。测得两容器中c(A)随时间t的变化如图所示,下列说法不正确的是
xC(g) △H<0。测得两容器中c(A)随时间t的变化如图所示,下列说法不正确的是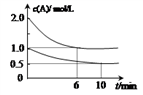
| A.x=1 |
| B.此条件下,该反应的平衡常数K=4 |
| C.给乙容器升温可缩短反应达平衡的时间但不能提高平衡转化率 |
| D.甲和乙中B的平衡转化率相等 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】下图是不同物质在密闭容器中反应的有关图像,下列对有关图像的叙述正确的是
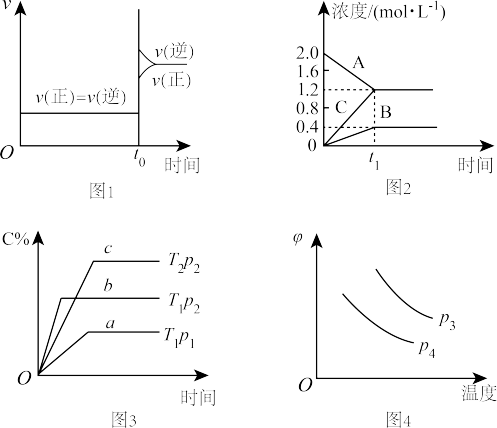

A.图1:对 达到平衡后,在 达到平衡后,在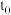 时刻充入了一定的HI,平衡逆向移动 时刻充入了一定的HI,平衡逆向移动 |
B.图2:该图像表示的方程式为3A B+2C B+2C |
C.图3:对 ,图中 ,图中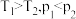 |
D.图4:对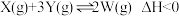 ,φ可表示X的百分含量 ,φ可表示X的百分含量 |
您最近一年使用:0次

 可作大型船舶的绿色燃料。工业上用
可作大型船舶的绿色燃料。工业上用 制备
制备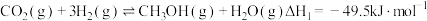

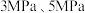 下,将
下,将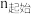
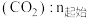
 的混合气体置于密闭容器中,若仅考虑上述反应,不同温度下反应体系达到平衡时,
的混合气体置于密闭容器中,若仅考虑上述反应,不同温度下反应体系达到平衡时, 、产物选择性
、产物选择性 的变化如图所示。
的变化如图所示。 或
或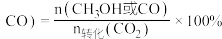 。下列说法不正确的是
。下列说法不正确的是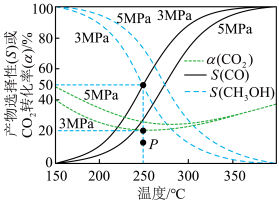
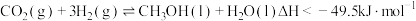
 后,不同压强下
后,不同压强下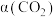 接近相等的原因为制备过程以反应1为主
接近相等的原因为制备过程以反应1为主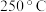 时,反应2的平衡常数
时,反应2的平衡常数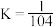
 下,
下,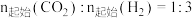 的混合气体在催化下反应一段时间
的混合气体在催化下反应一段时间 点的值,延长反应时间
点的值,延长反应时间


