五元环状化合物咪唑和噻吩都是平面分子,它们的结构简式如图所示。已知处于同一平面的多原子分子中如有相互平行的p轨道,p轨道电子在多个原子间运动形成不局限在两个原子之间的 型化学键,称为离域
型化学键,称为离域 键,表示为
键,表示为 ,m是成键原子数,n是成键电子数。下列说法错误的是
,m是成键原子数,n是成键电子数。下列说法错误的是
 型化学键,称为离域
型化学键,称为离域 键,表示为
键,表示为 ,m是成键原子数,n是成键电子数。下列说法错误的是
,m是成键原子数,n是成键电子数。下列说法错误的是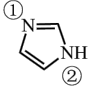 和
和
| A.沸点:咪唑>噻吩 |
B.咪唑和噻吩中均存在 型离域 型离域 键 键 |
C.噻吩中S原子的杂化方式为 杂化 杂化 |
| D.咪唑能够与金属离子形成配位键,其中②号N原子提供孤电子对 |
更新时间:2024-05-12 11:04:27
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】关于有机物 ,下列叙述不正确的是
,下列叙述不正确的是
 ,下列叙述不正确的是
,下列叙述不正确的是| A.碳原子的杂化类型有两种 |
| B.分子中最多有10个碳原子共平面 |
| C.分子式为C12H15Cl |
| D.能发生氧化、取代、加聚、消去反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】“ ”表示相关元素的原子中除去最外层电子的剩余部分,“。”表示氢原子,小黑点“·”表示没有形成共价键的最外层电子,短线表示共价键。关于下述几种分子的说法正确的是
”表示相关元素的原子中除去最外层电子的剩余部分,“。”表示氢原子,小黑点“·”表示没有形成共价键的最外层电子,短线表示共价键。关于下述几种分子的说法正确的是

 ”表示相关元素的原子中除去最外层电子的剩余部分,“。”表示氢原子,小黑点“·”表示没有形成共价键的最外层电子,短线表示共价键。关于下述几种分子的说法正确的是
”表示相关元素的原子中除去最外层电子的剩余部分,“。”表示氢原子,小黑点“·”表示没有形成共价键的最外层电子,短线表示共价键。关于下述几种分子的说法正确的是
| A.分子中,中心原子采用sp3杂化的只有①③ |
| B.①分子为正四面体结构,④分子为平面形 |
| C.②分子中σ键:π键=2:1 |
| D.四种分子的键角大小顺序为②>③>①>④ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
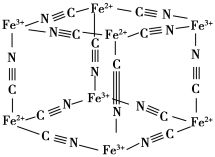
【推荐1】普鲁士蓝的晶体结构如图所示(每两个立方体中,一个 在其中一个立方体中心,另一个无
在其中一个立方体中心,另一个无 ,
, 未标出),下列说法不正确的是
未标出),下列说法不正确的是
 在其中一个立方体中心,另一个无
在其中一个立方体中心,另一个无 ,
, 未标出),下列说法不正确的是
未标出),下列说法不正确的是
A.化学式可以表示为 |
B.每一个立方体中平均含有6个 键 键 |
| C.普鲁士蓝属于配位化合物 |
D.每个 周围与之距离最近且相等的 周围与之距离最近且相等的 有12个 有12个 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】向含 的废水中加入铁粉和
的废水中加入铁粉和 可制备
可制备 ,发生反应:
,发生反应: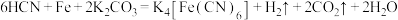 ,下列说法错误的是
,下列说法错误的是
 的废水中加入铁粉和
的废水中加入铁粉和 可制备
可制备 ,发生反应:
,发生反应: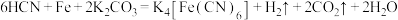 ,下列说法错误的是
,下列说法错误的是A.依据反应可知:还原性: |
| B.基态碳原子和基态氮原子的未成对电子之比为2∶3 |
| C.生成的配合物中存在离子键、配位键、极性键、非极性键 |
| D.生成的配合物的中心离子是Fe2+,配位数是6 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列化学用语的表达正确的是
A.邻羟基苯甲醛分子内氢键示意图: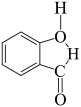 |
B.丙炔的球棍模型: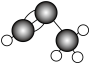 |
C. 过程中形成的是吸收光谱 过程中形成的是吸收光谱 |
D.Si原子电子排布式可能为: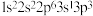 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列物质的性质与氢键无关的是( )
| A.冰的密度比水的密度小 | B.氨气极易溶于水 |
| C.AsH3的沸点比PH3的高 | D.溶解度:邻羟基苯甲醛<对羟基苯甲醛 |
您最近一年使用:0次


 中的N—H配位键说法正确的是
中的N—H配位键说法正确的是

