副族元素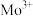 、
、 等元素较
等元素较 更易形成配合物,但是二环己烷并—18—冠(醚)—6在高锰酸钾溶液
更易形成配合物,但是二环己烷并—18—冠(醚)—6在高锰酸钾溶液_______ ;锰在周期表中的_______ 区。
(2)“超分子”中各元素(除H外)电负性由大到小的顺序为_______ 。
(3)副族元素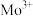 、
、 等元素比
等元素比 更易形成配合物,其原因是
更易形成配合物,其原因是_______ ; 与配体
与配体 形成共价键,提供孤电子对的原子是
形成共价键,提供孤电子对的原子是_______ (填元素符号),其中配体中C原子的杂化方式为_______ , 结合1个O和1个
结合1个O和1个 得到一种常见微粒,其空间构型为
得到一种常见微粒,其空间构型为_______ 。
(4)冠醚能够提升高锰酸钾氧化己烯的速率的原因是_______ 。
(5)氮化钼晶胞结构如图所示,N原子填充Mo围成的八面体空隙中,填充率为100%。_______ ;
② 的熔点
的熔点_______ (填“>”、“<”或“=”) ;
;
③若该八面体边长为 ,则晶胞的密度为
,则晶胞的密度为
_______  (
( 表示啊伏伽德罗常数)。
表示啊伏伽德罗常数)。
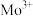 、
、 等元素较
等元素较 更易形成配合物,但是二环己烷并—18—冠(醚)—6在高锰酸钾溶液
更易形成配合物,但是二环己烷并—18—冠(醚)—6在高锰酸钾溶液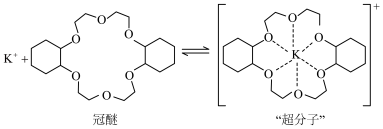
(2)“超分子”中各元素(除H外)电负性由大到小的顺序为
(3)副族元素
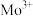 、
、 等元素比
等元素比 更易形成配合物,其原因是
更易形成配合物,其原因是 与配体
与配体 形成共价键,提供孤电子对的原子是
形成共价键,提供孤电子对的原子是 结合1个O和1个
结合1个O和1个 得到一种常见微粒,其空间构型为
得到一种常见微粒,其空间构型为(4)冠醚能够提升高锰酸钾氧化己烯的速率的原因是
(5)氮化钼晶胞结构如图所示,N原子填充Mo围成的八面体空隙中,填充率为100%。

②
 的熔点
的熔点 ;
;③若该八面体边长为
 ,则晶胞的密度为
,则晶胞的密度为
 (
( 表示啊伏伽德罗常数)。
表示啊伏伽德罗常数)。
2024·四川眉山·三模 查看更多[2]
更新时间:2024-05-20 09:05:16
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】山东大学晶体材料国家重点实验室成功生长出全球最大KDP晶体(名称:磷酸二氢钾,化学式:KH2PO4),常用于超级激光器项目。
(1)下列K原子的价电子排布图表示的状态中,能量最高和最低的分别为___ 、___ (填标号)
A. B.
B. C.
C. D.
D.
(2)KDP晶体中非ⅠA族元素电负性由大到小的顺序为___ 。
(3)①H3PO4( ),从结构角度解释其为弱弱的原因
),从结构角度解释其为弱弱的原因___ 。
②KDP晶体中 中心原子的杂化方式为
中心原子的杂化方式为___ 。
③五个磷酸分子的羟基之间脱去四个水分子形成五聚磷酸,1mol五聚磷酸中P-O单键的物质的量为___ mol。
(4)KDP晶体中K+与H2PO 的位置关系如图所示。
的位置关系如图所示。

①H2PO 的配位数为
的配位数为___ 。
②若KDP晶胞体积为Vnm3,且每mol晶胞含nmolKH2PO4,则KDP晶胞的密度为___ g·cm-3。(用含V、n的式子表示,NA为阿伏加 德罗常数的值)。
(1)下列K原子的价电子排布图表示的状态中,能量最高和最低的分别为
A.
 B.
B. C.
C. D.
D.
(2)KDP晶体中非ⅠA族元素电负性由大到小的顺序为
(3)①H3PO4(
 ),从结构角度解释其为弱弱的原因
),从结构角度解释其为弱弱的原因②KDP晶体中
 中心原子的杂化方式为
中心原子的杂化方式为③五个磷酸分子的羟基之间脱去四个水分子形成五聚磷酸,1mol五聚磷酸中P-O单键的物质的量为
(4)KDP晶体中K+与H2PO
 的位置关系如图所示。
的位置关系如图所示。
①H2PO
 的配位数为
的配位数为②若KDP晶胞体积为Vnm3,且每mol晶胞含nmolKH2PO4,则KDP晶胞的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】据媒体报道,某公司日前研发出比当前广泛使用的锂电池成本更低、寿命更长、充电速度更快的钠离子电池。该电池的负极材料为Na2Co2TeO6(制备原料为Na2CO3、Co3O4和TeO2),电解液为NaClO4的碳酸丙烯酯溶液。回答下列问题:
(1)Co属于元素周期表中_______ 区元素,其基态原子的价电子排布图为_______ ,和Co同周期的元素中,基态原子具有1个未成对电子的元素有_______ 种。
(2)基态Na原子中,核外电子的空间运动状态有_______ 种,其占据的最高能级电子云轮廓图形状为_______ 。
(3)C、O、Cl的电负性由大到小的顺序为_______ (用“>”连接,下同)。用离子符号表示NaClO4中三种元素所对应的简单离子半径由大到小的顺序为_______ 。第一电离能介于B、N之间的第二周期元素有_______ 种。
(4)O的简单氢化物的沸点比下一周期同主族元素的简单氢化物沸点高,其原因是_______ 。
(5)等电子体是指价电子数和原子数相同的分子、离子或原子团。
①下列各组不互为等电子体的是_______ 。
A.PO 与ClO
与ClO B.CO
B.CO 与NO
与NO C.N2与CN-D.NO2与CS2
C.N2与CN-D.NO2与CS2
②互为等电子体的分子或离子具有相似的化学键特征,请写出CO的结构式_______ 。
(1)Co属于元素周期表中
(2)基态Na原子中,核外电子的空间运动状态有
(3)C、O、Cl的电负性由大到小的顺序为
(4)O的简单氢化物的沸点比下一周期同主族元素的简单氢化物沸点高,其原因是
(5)等电子体是指价电子数和原子数相同的分子、离子或原子团。
①下列各组不互为等电子体的是
A.PO
 与ClO
与ClO B.CO
B.CO 与NO
与NO C.N2与CN-D.NO2与CS2
C.N2与CN-D.NO2与CS2②互为等电子体的分子或离子具有相似的化学键特征,请写出CO的结构式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】钡的单质和化合物在生产生活中有重要的应用。请回答下列问题:
(1)钡元素是第6周期的碱土金属元素,其基态原子的外围电子轨道表示式为_______ 。
(2)钡元素在自然界中主要以重晶石形式存在,其成分为BaSO4,其中所含三种元素的电负性从大到小的顺序是_______ ,SO 的空间构型是
的空间构型是_______ ,中心原子S的杂化方式是_______ 。
(3)部分碱土金属氧化物的熔点如下表所示:
由表中数据可知,该族元素氧化物熔点的变化规律是_______ ,产生这种规律的原因是_______ 。
(4)氯化钡的玻恩哈伯循环如下图所示:

①由图可知,Cl-Cl的键能为_______ 。
②元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1),则氯元素的第一电子亲和能E1=_______ 。
(5)已知氟化钡的晶胞符合萤石结构(见下图)。

①若将M和N两点的原子分数坐标分别定义为(0,0,0)和(0, ,
, ),则下列坐标为F-分数坐标的是
),则下列坐标为F-分数坐标的是_______ 。
A.(0, ,
, ) B.(
) B.( ,
, ,
, ) C.(
) C.( ,
, ,
, ) D.(
) D.( ,
, ,
, )
)
②若晶胞中两个相邻且距离最近的Ba2+的核间距为apm,则氟化钡的密度ρ=_______ g·cm-3(列出计算式,不必化简)。
(1)钡元素是第6周期的碱土金属元素,其基态原子的外围电子轨道表示式为
(2)钡元素在自然界中主要以重晶石形式存在,其成分为BaSO4,其中所含三种元素的电负性从大到小的顺序是
 的空间构型是
的空间构型是(3)部分碱土金属氧化物的熔点如下表所示:
| 碱土金属氧化物 | MgO | CaO | SrO | BaO |
| 熔点/°C | 2800 | 2576 | 2430 | 1923 |
由表中数据可知,该族元素氧化物熔点的变化规律是
(4)氯化钡的玻恩哈伯循环如下图所示:

①由图可知,Cl-Cl的键能为
②元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1),则氯元素的第一电子亲和能E1=
(5)已知氟化钡的晶胞符合萤石结构(见下图)。

①若将M和N两点的原子分数坐标分别定义为(0,0,0)和(0,
 ,
, ),则下列坐标为F-分数坐标的是
),则下列坐标为F-分数坐标的是A.(0,
 ,
, ) B.(
) B.( ,
, ,
, ) C.(
) C.( ,
, ,
, ) D.(
) D.( ,
, ,
, )
)②若晶胞中两个相邻且距离最近的Ba2+的核间距为apm,则氟化钡的密度ρ=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】自然界中存在大量金属元素,其中钠、镁、铝、铁、铜等在工农业生产中有着广泛的应用。
(1)请写出 的基态原子的核外电子排布式:
的基态原子的核外电子排布式:___________ 。
(2)金属元素A的原子只有3个电子层,其第一至第四电离能(单位: )如下:
)如下:
则A原子的价层电子排布式为___________ 。
(3)合成氨工业中,原料气( 及少量
及少量 的混合气)在进入合成塔前常用醋酸二氨合铜溶液来吸收原料气中的
的混合气)在进入合成塔前常用醋酸二氨合铜溶液来吸收原料气中的 ,其反应是(
,其反应是( 代表
代表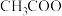 );
); (醋酸羧基三氨合铜)。
(醋酸羧基三氨合铜)。
配合物[Cu(NH3)3CO]Ac中心原子的配位数为___________ 。
(4) 、
、 等颗粒物及扬尘等易引起雾霾。其中
等颗粒物及扬尘等易引起雾霾。其中 的空间结构是
的空间结构是_______ 。
(5) 和
和 都属于离子晶体,
都属于离子晶体, 的熔点为
的熔点为 ,
, 的熔点高达
的熔点高达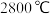 。造成两种晶体熔点差距的主要原因是
。造成两种晶体熔点差距的主要原因是___________ 。
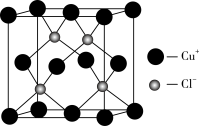
(6)铜的化合物种类很多,如图是氯化亚铜的晶胞结构,已知晶胞的棱长为 ,则氯化亚铜密度的计算式为
,则氯化亚铜密度的计算式为
___________  。
。
(1)请写出
 的基态原子的核外电子排布式:
的基态原子的核外电子排布式:(2)金属元素A的原子只有3个电子层,其第一至第四电离能(单位:
 )如下:
)如下: |  |  |  |
| 738 | 1451 | 7733 | 10540 |
则A原子的价层电子排布式为
(3)合成氨工业中,原料气(
 及少量
及少量 的混合气)在进入合成塔前常用醋酸二氨合铜溶液来吸收原料气中的
的混合气)在进入合成塔前常用醋酸二氨合铜溶液来吸收原料气中的 ,其反应是(
,其反应是( 代表
代表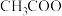 );
); (醋酸羧基三氨合铜)。
(醋酸羧基三氨合铜)。配合物[Cu(NH3)3CO]Ac中心原子的配位数为
(4)
 、
、 等颗粒物及扬尘等易引起雾霾。其中
等颗粒物及扬尘等易引起雾霾。其中 的空间结构是
的空间结构是(5)
 和
和 都属于离子晶体,
都属于离子晶体, 的熔点为
的熔点为 ,
, 的熔点高达
的熔点高达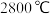 。造成两种晶体熔点差距的主要原因是
。造成两种晶体熔点差距的主要原因是(6)铜的化合物种类很多,如图是氯化亚铜的晶胞结构,已知晶胞的棱长为
 ,则氯化亚铜密度的计算式为
,则氯化亚铜密度的计算式为
 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】碳及其化合物广泛存在于自然界中。回答下列问题:
(1)在基态14C原子中,核外存在______ 对自旋相反的电子。
(2)碳在形成化合物时,其键型以共价键为主,原因是__________ 。
(3)CS2分子中,共价键的类型有________ ,C原子的杂化轨道类型是______ ,写出两个与CS2具有相同空间构型和键合形式的分子或离子_______ 。
(4)碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:

①在石墨烯晶体中,每个C原子连接_____ 个六元环,每个六元环占有___ 个C原子。
②在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接_____ 个六元环,六元环中最多有______ 个C原子在同一平面。
(1)在基态14C原子中,核外存在
(2)碳在形成化合物时,其键型以共价键为主,原因是
(3)CS2分子中,共价键的类型有
(4)碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:

①在石墨烯晶体中,每个C原子连接
②在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】深入认识物质的结构有助于进一步开发物质的用途。
(1) 的空间构型为
的空间构型为_______ 中心原子S的杂化方式为_______ 。
(2)从结构的角度解释: MgCO3 热分解温度低于CaCO3热分解温度的原因是_______ 。
(3)某些金属或金属化合物焰色反应能产生特殊的焰色。下列对其原理的分析中,正确的是_______(填序号)。
(4)氟代硼铍酸钾(含K、B、Be、O、F元素)晶体是唯一可直接倍频产生深紫外激光的非线性光学晶体。氟硼酸钾是制备氟代硼铍酸钾的原料之一,高温下分解为KF和BF3,氟硼酸钾晶体中所含的化学键有_______ (填序号)。
a.离子键 b. 非极性键 c.极性键 d.配位键 e.金属键
(5)BeO晶体也是制备氟代硼铍酸钾的原料,下图为其晶胞结构示意图。

①沿着晶胞体对角线方向的投影,下列图中能正确描述投影结果的是_______ (填序号)

②设O与Be的最近距离为a cm, NA表示阿伏加德罗常数的值,则BeO晶体的密度为_______ g∙cm-3。
(1)
 的空间构型为
的空间构型为(2)从结构的角度解释: MgCO3 热分解温度低于CaCO3热分解温度的原因是
(3)某些金属或金属化合物焰色反应能产生特殊的焰色。下列对其原理的分析中,正确的是_______(填序号)。
| A.电子从基态跃起到较高的激发态 | B.电子从较高的激发态跃迁到基态 |
| C.焰色反应的光谱属吸收光谱 | D.焰色反应的光谱属于发射光谱 |
a.离子键 b. 非极性键 c.极性键 d.配位键 e.金属键
(5)BeO晶体也是制备氟代硼铍酸钾的原料,下图为其晶胞结构示意图。

①沿着晶胞体对角线方向的投影,下列图中能正确描述投影结果的是

②设O与Be的最近距离为a cm, NA表示阿伏加德罗常数的值,则BeO晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】全球首次在350公里时速的奥运版复兴号高铁列车上依托5G技术打造的超高清直播演播室,实现了超高清信号的长时间稳定传输。请回答下列问题:
(1)5G芯片主要材质是高纯硅,基态Si原子有___________ 种不同空间运动状态的电子。高纯硅制备过程中会生成SiHCl3等中间产物,与硅相比,这两种物质的沸点:SiHCl3___________ Si(填“>”或“<”),原因是___________
(2)复兴号高铁车体材质用到Mn、Co等元素。Mn原子的价层电子排布图为___________ ,Mn的一种配合物化学式为[Mn(CO)5(CH3CN)],下列说法正确的是_______
A.CH3CN与Mn原子配位时,提供孤电子对的时C原子
B.Mn原子的配位数为6
C.CH3CN中C原子的杂化类型为sp2、sp3
D.CH3CN中σ键与π键数目之比为5:2
(3)时速600公里的磁浮列车需要用到超导材料。超导材料TiN具有NaCl型结构(如图),晶胞参数为apm,则最近的两个Ti3+间的距离为___________ pm;N3-的配位数为___________ ;阿伏伽德罗常数的值为NA,则该氮化钛的密度___________ g/cm3(列出计算式即可)

(1)5G芯片主要材质是高纯硅,基态Si原子有
(2)复兴号高铁车体材质用到Mn、Co等元素。Mn原子的价层电子排布图为
A.CH3CN与Mn原子配位时,提供孤电子对的时C原子
B.Mn原子的配位数为6
C.CH3CN中C原子的杂化类型为sp2、sp3
D.CH3CN中σ键与π键数目之比为5:2
(3)时速600公里的磁浮列车需要用到超导材料。超导材料TiN具有NaCl型结构(如图),晶胞参数为apm,则最近的两个Ti3+间的距离为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】镍、铜等金属及其化合物在工农业生产上有重要用途。回答下列问题:
(1)基态Ni的核外电子排布式为_______ ,Ni位于元素周期表中_______ 区(填“s”“p”“d”或“ds”),其核外电子占据的最高能层符号为_______ 。
(2)Ni与CO能形成如图所示的配合物 ,该分子中σ键与π键个数比为
,该分子中σ键与π键个数比为_______ 。 易溶于
易溶于_______ (填标号)。
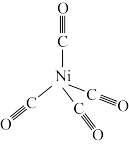
A.水 B.四氯化碳 C.苯 D.稀
(3)将Cu粉加入浓氨水中,并通入 ,充分反应后溶液呈深蓝色,该反应的离子方程式为
,充分反应后溶液呈深蓝色,该反应的离子方程式为_______ 。
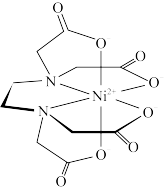
(4)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种 与EDTA形成的螯合物的结构如图所示,1个该配合物中通过螯合作用形成的配位键有
与EDTA形成的螯合物的结构如图所示,1个该配合物中通过螯合作用形成的配位键有_______ 个,其中提供孤对电子的原子为_______ (写元素符号)。
(5)钴的一种化合物的晶胞结构如下图所示:

①已知A点的原子坐标参数为(0,0,0),B点为( ,0,
,0, ),则C点的原子坐标参数为
),则C点的原子坐标参数为_______ 。
②已知晶胞参数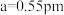 ,则该晶体的密度为
,则该晶体的密度为_______  (用NA表示阿伏加德罗常数,只列出计算表达式即可。
(用NA表示阿伏加德罗常数,只列出计算表达式即可。
(1)基态Ni的核外电子排布式为
(2)Ni与CO能形成如图所示的配合物
 ,该分子中σ键与π键个数比为
,该分子中σ键与π键个数比为 易溶于
易溶于
A.水 B.四氯化碳 C.苯 D.稀

(3)将Cu粉加入浓氨水中,并通入
 ,充分反应后溶液呈深蓝色,该反应的离子方程式为
,充分反应后溶液呈深蓝色,该反应的离子方程式为(4)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种
 与EDTA形成的螯合物的结构如图所示,1个该配合物中通过螯合作用形成的配位键有
与EDTA形成的螯合物的结构如图所示,1个该配合物中通过螯合作用形成的配位键有
(5)钴的一种化合物的晶胞结构如下图所示:

①已知A点的原子坐标参数为(0,0,0),B点为(
 ,0,
,0, ),则C点的原子坐标参数为
),则C点的原子坐标参数为②已知晶胞参数
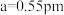 ,则该晶体的密度为
,则该晶体的密度为 (用NA表示阿伏加德罗常数,只列出计算表达式即可。
(用NA表示阿伏加德罗常数,只列出计算表达式即可。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】稀土元素是指元素周期表中原子序数为57到71的15种镧系元素,以及与镧系元素化学性质相似的钪(Sc)和钇(Y)共17种元素。稀土元素有“工业维生素”的美称,如今已成为极其重要的战略资源。
(1)钪(Sc)为21号元素,位于周期表的_____ 区,基态原子价电子排布图为_______ 。
(2)离子化合物Na3[Sc(OH)6]中,存在的化学键除离子键外还有_______ 。
(3)Sm(钐)的单质与l,2-二碘乙烷可发生如下反应:Sm +ICH2CH2I→SmI2+CH2=CH2。
ICH2CH2I中碳原子杂化轨道类型为______ , lmol CH2=CH2中含有的σ键数目为______ 。常温下l,2-二碘乙烷为液体而乙烷为气体,其主要原因是__________ 。
(4) PrO2(二氧化镨)的晶体结构与CaF2相似,晶饱中Pr(镨)原子位于面心和顶点。则PrO2(二氧化镨)的晶胞中有________ 个氧原子。
(5)Ce(铈)单质为面心立方晶体,其晶胞参数a=516pm。晶胞中Ce(铈)原子的配位数为_______ ,列式表示Ce(铈)单质的密度:________ g/cm3(用NA表示阿伏伽德罗常数的值,不必计算出结果)
(1)钪(Sc)为21号元素,位于周期表的
(2)离子化合物Na3[Sc(OH)6]中,存在的化学键除离子键外还有
(3)Sm(钐)的单质与l,2-二碘乙烷可发生如下反应:Sm +ICH2CH2I→SmI2+CH2=CH2。
ICH2CH2I中碳原子杂化轨道类型为
(4) PrO2(二氧化镨)的晶体结构与CaF2相似,晶饱中Pr(镨)原子位于面心和顶点。则PrO2(二氧化镨)的晶胞中有
(5)Ce(铈)单质为面心立方晶体,其晶胞参数a=516pm。晶胞中Ce(铈)原子的配位数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】碘及其化合物在生产、生活中有着广泛的应用。回答下列问题:已知: 电负性: H 2.20; C 2.55; F 3.98; P 2.19; I 2.66
(1)人工合成的 131I是医疗上常用的放射性同位素,基态碘原子价层电子排布式为___________ 。
(2)碘单质在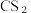 中的溶解度比在水中的大,解释原因
中的溶解度比在水中的大,解释原因___________ 。
(3)HI 主要用于药物合成,通常用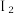 和P反应生成
和P反应生成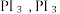 再水解制HI。
再水解制HI。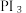 的空间结构是
的空间结构是___________ (用文字描述),PI₃水解生成 HI的化学方程式是___________ 。
(4)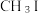 是一种甲基化试剂,
是一种甲基化试剂,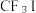 可用作制冷剂,
可用作制冷剂,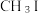 和
和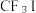 发生水解时的主要反应分别是:
发生水解时的主要反应分别是: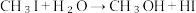 和
和 。
。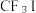 的水解产物是HIO,结合电负性解释原因
的水解产物是HIO,结合电负性解释原因___________ 。
(5) 晶体是一种性能良好的光学材料,其晶胞为立方体,边长为 a nm,晶胞中 K、I、O分别处于顶点、体心、面心位置,结构如图。
晶体是一种性能良好的光学材料,其晶胞为立方体,边长为 a nm,晶胞中 K、I、O分别处于顶点、体心、面心位置,结构如图。
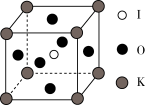
①与 K 原子紧邻的O原子有___________ 个。
② 中
中  里Ⅰ原子的杂化类型是
里Ⅰ原子的杂化类型是___________ 。
③若晶体的密度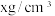 ,则阿伏加德罗常数
,则阿伏加德罗常数
___________  。 (用含x、a的表达式表示)
。 (用含x、a的表达式表示)
(1)人工合成的 131I是医疗上常用的放射性同位素,基态碘原子价层电子排布式为
(2)碘单质在
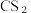 中的溶解度比在水中的大,解释原因
中的溶解度比在水中的大,解释原因(3)HI 主要用于药物合成,通常用
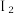 和P反应生成
和P反应生成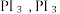 再水解制HI。
再水解制HI。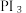 的空间结构是
的空间结构是(4)
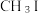 是一种甲基化试剂,
是一种甲基化试剂,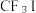 可用作制冷剂,
可用作制冷剂,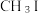 和
和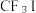 发生水解时的主要反应分别是:
发生水解时的主要反应分别是: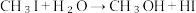 和
和 。
。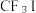 的水解产物是HIO,结合电负性解释原因
的水解产物是HIO,结合电负性解释原因(5)
 晶体是一种性能良好的光学材料,其晶胞为立方体,边长为 a nm,晶胞中 K、I、O分别处于顶点、体心、面心位置,结构如图。
晶体是一种性能良好的光学材料,其晶胞为立方体,边长为 a nm,晶胞中 K、I、O分别处于顶点、体心、面心位置,结构如图。
①与 K 原子紧邻的O原子有
②
 中
中  里Ⅰ原子的杂化类型是
里Ⅰ原子的杂化类型是③若晶体的密度
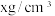 ,则阿伏加德罗常数
,则阿伏加德罗常数
 。 (用含x、a的表达式表示)
。 (用含x、a的表达式表示)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】氮及其化合物与人类生产、生活息息相关。回答下列问题:
(1)基态氮原子的价电子排布图是______________ 。
(2)B、N、O三种元素第一电离能从大到小的顺序是__________ 。
(3)NaNO2中氮原子的杂化方式是____________ ,阴离子的立体构型是__________ 。
(4)NF3的键角____________ NH3的键角(填“<”“>”或“=”),原因是____________ 。
(5)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。1 mol NH4BF4含有_______ mol配位键。
(6)安全气囊的设计原理为6NaN3+Fe2O3 3Na2O+2Fe+9N2↑。
3Na2O+2Fe+9N2↑。
①该反应中元素的电负性由大到小的顺序是____________ ;
②Na2O的晶胞结构如图所示,晶胞边长为566 pm,晶胞中氧离子的配位数为____________ ,Na2O晶体的密度为________ g·cm-3(只要求列算式,不必计算出结果)。

(1)基态氮原子的价电子排布图是
(2)B、N、O三种元素第一电离能从大到小的顺序是
(3)NaNO2中氮原子的杂化方式是
(4)NF3的键角
(5)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。1 mol NH4BF4含有
(6)安全气囊的设计原理为6NaN3+Fe2O3
 3Na2O+2Fe+9N2↑。
3Na2O+2Fe+9N2↑。①该反应中元素的电负性由大到小的顺序是
②Na2O的晶胞结构如图所示,晶胞边长为566 pm,晶胞中氧离子的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】生物体系的酶催化具有高效选择性,主要依靠辅因子和氨基酸残基对底物的协同作用,受此启发科学家设计了一系列金属化合物和非金属化合物也具有对底物多个点的相互作用,管海荣团队报道了一组铁铜双金属有机化合物用于催化在水汽置换条件下的苯甲醛还原反应。已知铁铜双金属有机化合物如图所示(R代表的是烃基,L代表的是复杂集团)。

请回答下列问题:
(1)基态铜原子的价电子排布式为_______ 。
(2)该物质中碳元素的杂化方式为_______ 。
(3)下表是Fe和Cu部分电离能的数据,请解释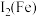 小于
小于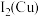 的主要原因:
的主要原因:_______ 。
(4)Cu可以形成多种配合物, 是常见的配合物,具有对称的空间构型。其中两个
是常见的配合物,具有对称的空间构型。其中两个 被两个
被两个 取代,能得到两种不同结构的产物,则
取代,能得到两种不同结构的产物,则 的空间构型为
的空间构型为_______ ,一个 中
中 键和
键和 键的数目之比为
键的数目之比为_______ 。
(5) 可以与多种金属离子形成络合物。且
可以与多种金属离子形成络合物。且 极易溶于水,原因与氢键有关,请问
极易溶于水,原因与氢键有关,请问 的一水合物的结构式为
的一水合物的结构式为_______ ,理由是_______ 。
(6)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。Fe和Cu在自然界常以硫化物的形式存在一种四方结构的晶胞结构及晶胞参数如下图所示。

找出该晶胞中距离 距离最近的S的坐标参数:
距离最近的S的坐标参数:_______ (用分数坐标表示),其密度为_______  (阿伏加德罗常数的值用
(阿伏加德罗常数的值用 表示)。
表示)。

请回答下列问题:
(1)基态铜原子的价电子排布式为
(2)该物质中碳元素的杂化方式为
(3)下表是Fe和Cu部分电离能的数据,请解释
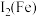 小于
小于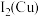 的主要原因:
的主要原因:| 元素 | Fe | Cu |
第一电离能 |  |  |
第二电离能 |  | 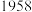 |
 是常见的配合物,具有对称的空间构型。其中两个
是常见的配合物,具有对称的空间构型。其中两个 被两个
被两个 取代,能得到两种不同结构的产物,则
取代,能得到两种不同结构的产物,则 的空间构型为
的空间构型为 中
中 键和
键和 键的数目之比为
键的数目之比为(5)
 可以与多种金属离子形成络合物。且
可以与多种金属离子形成络合物。且 极易溶于水,原因与氢键有关,请问
极易溶于水,原因与氢键有关,请问 的一水合物的结构式为
的一水合物的结构式为(6)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。Fe和Cu在自然界常以硫化物的形式存在一种四方结构的晶胞结构及晶胞参数如下图所示。

| 坐标原子 | x | y | z |
| Cu |  |  |  |
| Fe |  |  |  |
 距离最近的S的坐标参数:
距离最近的S的坐标参数: (阿伏加德罗常数的值用
(阿伏加德罗常数的值用 表示)。
表示)。
您最近一年使用:0次



