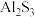常温下,下列各组离子在指定溶液中一定能大量共存的有几组
① 的溶液中:
的溶液中: 、
、 、
、 、
、
②2mol/的HCl溶液中: 、
、 、
、 、
、
③加入Al能放出 的溶液中:
的溶液中: 、
、 、
、 、
、
④由水电离出的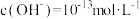 的溶液中:
的溶液中: 、
、 、
、 、
、
⑤1mol/L的 溶液中:
溶液中: 、
、 、
、 、
、
①
 的溶液中:
的溶液中: 、
、 、
、 、
、
②2mol/的HCl溶液中:
 、
、 、
、 、
、
③加入Al能放出
 的溶液中:
的溶液中: 、
、 、
、 、
、
④由水电离出的
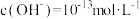 的溶液中:
的溶液中: 、
、 、
、 、
、
⑤1mol/L的
 溶液中:
溶液中: 、
、 、
、 、
、
| A.1组 | B.2组 | C.3组 | D.4组 |
更新时间:2024-05-13 17:25:52
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列有关溶液组成的描述合理的是
| A.无色溶液中可能大量存在Al3+、NH4+、Cl-、S2- |
| B.pH=l的溶液中可能大量存在Na+、NH4+、SiO32-、I- |
| C.弱碱性溶液中可能大量存在Na+、 K+、Cl-、HCO3- |
| D.0.1mol·L-1NaAlO2溶液中可能大量存在Na+、H+、 Cl-、SO42- |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】在下列限定条件下各组离子能大量共存的是
A.无色透明的溶液中: 、 、 、 、 、 、 |
B.使紫色石蕊试液液呈蓝色的溶液中: 、 、 、 、 、 、 |
C.能与铁反应放出 的溶液中: 的溶液中: 、 、 、 、 、 、 |
D.含有大量 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,pH=11的氨水和pH=1的盐酸等体积混合(混合溶液体积为两溶液体积之和),恰好完全反应,则下列说法错误的是
| A.氨水的浓度大于盐酸的浓度 |
B.原氨水中有1%的含氮微粒为NH |
| C.氨水中水电离出的c(H+)是盐酸中水电离出的c(H+)的100倍 |
D.混合溶液中c(NH )+c(NH3·H2O)+c(NH3)=c(Cl-) )+c(NH3·H2O)+c(NH3)=c(Cl-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】NA表示阿伏加德罗常数的值,下列说法正确的是
| A.常温下,pH=1的硫酸溶液中,含有H+数目为0.1NA |
| B.常温下,1 L 0.5 mol·L-1的AlCl3溶液中,含有Al3+数目为0.5NA |
| C.常温下,1 L pH=12的CH3COONa溶液,由水电离产生的OH-数目为0.01NA |
D.标准状况下,4.48 L NH3溶于水得到的溶液中,NH3·H2O和 的总数为0.2NA 的总数为0.2NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】25°C时,用1.0 mol·L-1 NaOH溶液滴定20.00 mL c1 mol·L-1的盐酸,用0.010 mol·L-1 NaOH溶液滴定20.00 mL c2 mol·L-1的盐酸,滴定曲线如图所示。下列说法不正确的是(已知lg5=0.7)
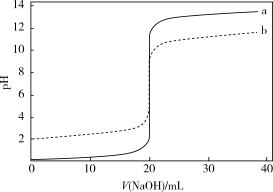

| A.曲线b表示滴定c2 mol·L-1的盐酸 |
| B.水的电离程度在V (NaOH) = 20.00 mL时最大 |
| C.滴定至pH=7时,两份溶液导电能力相同 |
| D.当1.0 mol·L-1 NaOH溶液滴定至19.98 mL时,混合溶液的pH约为3.3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列离子方程式中,能够正确表示题目给出的反应的是
A.铵根和硅酸根不能同时存在于溶液中的原因:NH +SiO +SiO =NH4SiO3↓ =NH4SiO3↓ |
B.硫化钠与稀硫酸混合:S2—+8H++SO =2S↓+4H2O =2S↓+4H2O |
C.氯化铝溶液滴入氨水:Al3++3NH3•H2O=Al(OH)3↓+3NH |
| D.氯化亚铁酸性溶液暴露在空气中变质:3Fe2++3O2+6H+=3Fe(OH)2↓ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验操作、现象以及对结论均正确的是
| 实验操作及现象 | 结论 | |
| A | 明矾的水溶液和小苏打溶液混合,生成大量白色泡沫 | 弱碱阳离子的水解和弱酸阴离子的水解相互促进 |
| B | 在0.1mol/LMgCl2溶液中加入过量NaOH溶液,产生白色沉淀后,再加入等浓度的FeCl3溶液,沉淀变为红褐色 | Fe(OH)3的溶解度小于Mg(OH)2 |
| C | 加热饱和FeCl3溶液制备Fe(OH)3胶体 | 水解过程是吸热过程 |
| D | 用广泛PH试纸测得某NH4Cl溶液的pH为5.8 | NH4Cl水解呈酸性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 溶液与
溶液与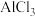 溶液混合制取
溶液混合制取