非金属元素及其化合物广泛应用于生产、生活、国防等多个领域。请回答下列问题:
(1) 的VSEPR模型名称为
的VSEPR模型名称为___________ ,分子的空间结构名称为___________ ,中心原子有___________ 个杂化轨道;
(2)氮可形成多种氧化物, 和
和 (直线形分子)的中心原子均为N原子,但二者中心原子的杂化方式不同,二者均存在大
(直线形分子)的中心原子均为N原子,但二者中心原子的杂化方式不同,二者均存在大 键(
键( 中,3为形成大
中,3为形成大 键的原子数,4为大
键的原子数,4为大 键中的共用电子个数),
键中的共用电子个数), 中中心氮原子的轨道杂化方式为:
中中心氮原子的轨道杂化方式为:___________ ; 中的
中的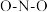 键角
键角___________ (填“ ”“
”“ ”或“
”或“ ”)
”) 中的
中的 键角。
键角。
(3) 的简单平面结构如图。
的简单平面结构如图。___________ 。
②在该晶体中存在的化学键类型有___________ (填标号)。
a.离子键 b.极性共价键 c.非极性共价键 d.氢键 e.配位键
③水分子①中的键角___________ (填“ ”“
”“ ”或“
”或“ ”)
”) ,原因是
,原因是___________ 。
(1)
 的VSEPR模型名称为
的VSEPR模型名称为(2)氮可形成多种氧化物,
 和
和 (直线形分子)的中心原子均为N原子,但二者中心原子的杂化方式不同,二者均存在大
(直线形分子)的中心原子均为N原子,但二者中心原子的杂化方式不同,二者均存在大 键(
键( 中,3为形成大
中,3为形成大 键的原子数,4为大
键的原子数,4为大 键中的共用电子个数),
键中的共用电子个数), 中中心氮原子的轨道杂化方式为:
中中心氮原子的轨道杂化方式为: 中的
中的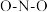 键角
键角 ”“
”“ ”或“
”或“ ”)
”) 中的
中的 键角。
键角。(3)
 的简单平面结构如图。
的简单平面结构如图。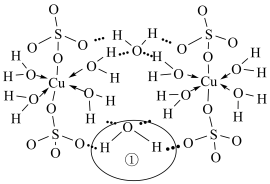
②在该晶体中存在的化学键类型有
a.离子键 b.极性共价键 c.非极性共价键 d.氢键 e.配位键
③水分子①中的键角
 ”“
”“ ”或“
”或“ ”)
”) ,原因是
,原因是
更新时间:2024-05-22 22:59:33
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】填空。
(1) 中的化学键从形成过程来看,属于
中的化学键从形成过程来看,属于___________ (填“σ”或“π”)键。
(2) 和
和 分子中C原子的杂化方式分别为
分子中C原子的杂化方式分别为___________ 和___________ 。
(3) 分子的结构式为
分子的结构式为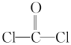 ,每个
,每个 分子内含有的σ键、π键数目分别为___________。
分子内含有的σ键、π键数目分别为___________。
(4)有两种活性反应中间体粒子,它们的粒子中均含有1个碳原子和3个氢原子。请依据下面给出的这两种微粒的球棍模型,写出相应的化学式:
甲: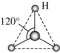
___________ ,乙:
___________ 。
(1)
 中的化学键从形成过程来看,属于
中的化学键从形成过程来看,属于(2)
 和
和 分子中C原子的杂化方式分别为
分子中C原子的杂化方式分别为(3)
 分子的结构式为
分子的结构式为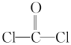 ,每个
,每个 分子内含有的σ键、π键数目分别为___________。
分子内含有的σ键、π键数目分别为___________。| A.4个σ键 | B.2个σ键、2个π键 |
| C.2个σ键、1个π键 | D.3个σ键、1个π键 |
甲:


您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】青金石是碱性铝硅酸盐矿物,其中含钠、铝、硅、硫、氧、氧等元素,曾用来制作颜料。
(1)在周期表中,与Si的化学性质最相似的邻族元素是_________ 。
(2) Na+和 Ne互为等电子体,电离能 I2(Na)_________ I1(Ne)填"〉”或“<")。
(3)已知氯、硫有多种含氧酸,HClO4中共价键类型有_____ ,硫酸的结构式为_____ 。
(4)氢卤酸(HX)的电离过程如图。△H1和△H2的递变规律:HF > HCl> HBr >HI,其中△H1(HF)特别大的原因为________ ,影响△H2递变的因素为________ 。
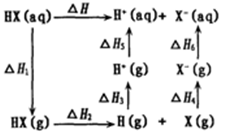
(1)在周期表中,与Si的化学性质最相似的邻族元素是
(2) Na+和 Ne互为等电子体,电离能 I2(Na)
(3)已知氯、硫有多种含氧酸,HClO4中共价键类型有
(4)氢卤酸(HX)的电离过程如图。△H1和△H2的递变规律:HF > HCl> HBr >HI,其中△H1(HF)特别大的原因为
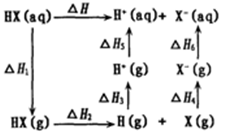
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】I.有下列分子或离子:BF3、H2O、NH 、SO2、HCHO、PCl3、CO2
、SO2、HCHO、PCl3、CO2
(1)粒子构型为直线型的为:______
(2)粒子的立体构型为V型的为:______
(3)粒子的立体构型为平面三角形的为:______
(4)粒子的立体构型为三角锥型的为:______
(5)粒子的立体构型为正四面体的为______
II.在下列分子中,①H2,②CO2,③H2O2,④HCN(填序号)。分子中只有σ键的是______ ,分子中含有π键的是 ______ ,分子中所有原子都满足最外层为8个电子结构的是______ ,分子中含有由两个原子的s轨道重叠形成的σ键的是 ______ ,分子中含有由一个原子的s轨道与另一个原子的p轨道重叠形成的σ键的是______ ,分子中既含有极性键又含有非极性键的是______ 。
 、SO2、HCHO、PCl3、CO2
、SO2、HCHO、PCl3、CO2(1)粒子构型为直线型的为:
(2)粒子的立体构型为V型的为:
(3)粒子的立体构型为平面三角形的为:
(4)粒子的立体构型为三角锥型的为:
(5)粒子的立体构型为正四面体的为
II.在下列分子中,①H2,②CO2,③H2O2,④HCN(填序号)。分子中只有σ键的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】铜是人类最早发现的金属,也是人类广泛使用的一种金属。铜及其化合物在工业、工程技术和工艺上有着广泛的应用。
(1)早期发现的天然准晶颗粒由Cu、Fe、Al三种金属元素组成。Fe元素位于元素周期表的____ 区。基态Al原子的L层电子排布图为___________ 。
(2)Cu2O为半导体材料,可由乙醛(CH3CHO)和新制氢氧化铜反应得到,同时可得到乙酸。乙醛中碳原子的杂化轨道类型为_________ ,1mol乙酸分子中含有的σ键的数目为____________ 。
(3)制造单晶硅太阳能电池片时,一般掺杂微量的铜、碳、硼、氮等。一价铜离子的电子排布式为____ 。碳、硼、氮元素的电负性由大到小的顺序是_____ 。(用元素符号表示)
(4)在络离子[Cu(NH3)4]2+中NH3的VSEPR模型为_________ 。
(5)铜银合金晶体具有面心立方最密堆积结构。在晶胞中,Cu原子位于面心,Ag原子位于顶点,若该晶胞边长为r pm,则合金的密度为____ g·cm-3(设阿伏伽德罗常数的值为NA)。
(1)早期发现的天然准晶颗粒由Cu、Fe、Al三种金属元素组成。Fe元素位于元素周期表的
(2)Cu2O为半导体材料,可由乙醛(CH3CHO)和新制氢氧化铜反应得到,同时可得到乙酸。乙醛中碳原子的杂化轨道类型为
(3)制造单晶硅太阳能电池片时,一般掺杂微量的铜、碳、硼、氮等。一价铜离子的电子排布式为
(4)在络离子[Cu(NH3)4]2+中NH3的VSEPR模型为
(5)铜银合金晶体具有面心立方最密堆积结构。在晶胞中,Cu原子位于面心,Ag原子位于顶点,若该晶胞边长为r pm,则合金的密度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】X、Y、Z、W是元素周期表中前36号元素,且原子序数依次增大。其相关信息如下表:
(1)元素X最高价氧化物分子的空间构型是__________________ ,是_________ (填“极性”或“非极性”)分子。
(2)Y的最简单氢化物的沸点比Z的最简单氢化物的沸点高,原因是____________________________________
(3)基态Z原子中,电子占据的最高电子层符号为_________ ,该电子层具有的原子轨道数为________________
(4)元素W位于元素周期表的第________ 族。
| 元素编号 | 元素性质或原子结构 |
| X | X原子的最外层电子数是其内层电子总数的2倍 |
| Y | Y的基态原子价电子排布式为nsnnpn+2 |
| Z | 最外层中只有两对成对电子 |
| W | 前四周期基态原子中,W元素的未成对电子数最多 |
(1)元素X最高价氧化物分子的空间构型是
(2)Y的最简单氢化物的沸点比Z的最简单氢化物的沸点高,原因是
(3)基态Z原子中,电子占据的最高电子层符号为
(4)元素W位于元素周期表的第
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氮是地球上极为丰富的元素。
(1)下列氮原子的能量最低的是___________。
(2)“笑气”(N2O)是人类最早应用于医疗的麻醉剂之一,有关理论认为N2O与CO2具有相似的结构(包括电子式);已知N2O分子中氧原子只与一个氮原子相连,则N2O的电子式可表示为___________ ,其空间构型是___________ 。
(3)肼(N2H4)可作火箭燃料,其分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物,则其分子中氮原子的杂化轨道类型是___________ 。
(4)氮可以形成多种离子,如N3-、NH 、N
、N 、NH
、NH 、N2H
、N2H 、N2H
、N2H 等,已知N2H
等,已知N2H 与N2H
与N2H 是由中性分子结合质子形成的,类似于NH
是由中性分子结合质子形成的,类似于NH ,因此有类似于 NH
,因此有类似于 NH 的性质。
的性质。
①写出N2H 的结构式并用“→”标出配位键
的结构式并用“→”标出配位键___________ 。
②N2H 在足量碱性溶液中反应的离子方程式:
在足量碱性溶液中反应的离子方程式:___________ 。
(5)I (可看成II
(可看成II )属于多卤素阳离子,根据VSEPR模型推测I
)属于多卤素阳离子,根据VSEPR模型推测I 的空间构型为
的空间构型为___________ 。
(6)据报道,美国科学家卡尔•克里斯特于1998年11月合成了一种名为“N5”的物质,由于其具有极强的爆炸性,又称为“盐粒炸弹”。迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排成V形,如果5个N结合后都达到8电子结构,且含有2个N≡N键,则“N5”分子碎片所带电荷是___________ 。
(1)下列氮原子的能量最低的是___________。
A.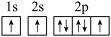 | B.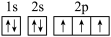 | C.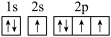 | D.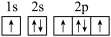 |
(3)肼(N2H4)可作火箭燃料,其分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物,则其分子中氮原子的杂化轨道类型是
(4)氮可以形成多种离子,如N3-、NH
 、N
、N 、NH
、NH 、N2H
、N2H 、N2H
、N2H 等,已知N2H
等,已知N2H 与N2H
与N2H 是由中性分子结合质子形成的,类似于NH
是由中性分子结合质子形成的,类似于NH ,因此有类似于 NH
,因此有类似于 NH 的性质。
的性质。①写出N2H
 的结构式并用“→”标出配位键
的结构式并用“→”标出配位键②N2H
 在足量碱性溶液中反应的离子方程式:
在足量碱性溶液中反应的离子方程式:(5)I
 (可看成II
(可看成II )属于多卤素阳离子,根据VSEPR模型推测I
)属于多卤素阳离子,根据VSEPR模型推测I 的空间构型为
的空间构型为(6)据报道,美国科学家卡尔•克里斯特于1998年11月合成了一种名为“N5”的物质,由于其具有极强的爆炸性,又称为“盐粒炸弹”。迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排成V形,如果5个N结合后都达到8电子结构,且含有2个N≡N键,则“N5”分子碎片所带电荷是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】科学家开发出了多种太阳能电池,除晶体硅太阳能电池外,还有GaAs太阳能电池、铜铟镓硒薄膜太阳能电池等。
(1)基态Ga原子的电子排布式为________ 。
(2)高温下CuO容易转化为Cu2O,试从原子结构角度解释原因________________ 。
(3)H2Se分子的键角_______ H2O分子的键角(选填“>”、“=”或“<”)。写出与SeO3互为等电子体的一种阴离子_____________ (写化学式)。
(4) AsF3分子的立体构型为__________ ;AsF3是极性分子,理由是_________________ 。
(5)Ga(OH)3与NaOH溶液反应生成Na[Ga(OH)4]。Na[Ga(OH)4]溶液中含有的化学键有__________________ 。
A.共价键 B.离子键 C.金属键 D.配位键 E.氢键
(6)金刚砂(SiC)晶胞如图所示:
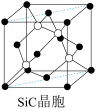
金刚砂中硅原子的杂化轨道类型为_______ ,沿晶胞图中虚线方向的切面图为__________ (填标号)。

(1)基态Ga原子的电子排布式为
(2)高温下CuO容易转化为Cu2O,试从原子结构角度解释原因
(3)H2Se分子的键角
(4) AsF3分子的立体构型为
(5)Ga(OH)3与NaOH溶液反应生成Na[Ga(OH)4]。Na[Ga(OH)4]溶液中含有的化学键有
A.共价键 B.离子键 C.金属键 D.配位键 E.氢键
(6)金刚砂(SiC)晶胞如图所示:

金刚砂中硅原子的杂化轨道类型为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】甲醇(CH3OH)空气氧化法是生产工业甲醛(HCHO)的常用方法。发生的反应为2CH3OH+O2 2
2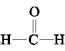 +2H2O
+2H2O
(1)C、H、O 三种元素的电负性由大到小的顺序为_______ 。
(2)H2O的中心原子上的孤电子对数为_______ 。
(3)HCHO分子内σ键与π键个数之比为_______ ,HCHO的空间结构为_______ 。
(4)CH3OH和HCHO分子中碳原子的杂化轨道类型分别为_______ 和_______ 。
(5)工业上利用甲醛易溶于水的性质吸收产品,解释甲醛易溶于水的原因:_______ 。
 2
2 +2H2O
+2H2O(1)C、H、O 三种元素的电负性由大到小的顺序为
(2)H2O的中心原子上的孤电子对数为
(3)HCHO分子内σ键与π键个数之比为
(4)CH3OH和HCHO分子中碳原子的杂化轨道类型分别为
(5)工业上利用甲醛易溶于水的性质吸收产品,解释甲醛易溶于水的原因:
您最近一年使用:0次



