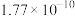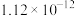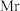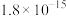是生产金属钛及其化合物的重要中间体,常温下为液体且有毒,暴露在空气中会发烟,极易水解。模拟工业上以
是生产金属钛及其化合物的重要中间体,常温下为液体且有毒,暴露在空气中会发烟,极易水解。模拟工业上以 、木炭和
、木炭和 为原料制备
为原料制备 的装置如图(夹持装置略)。
的装置如图(夹持装置略)。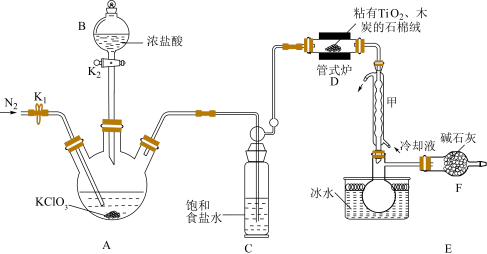
 的制备
的制备(ⅰ)连接仪器,检验装置的气密性,盛装药品;(ⅱ)打开
 ,……(ⅲ)打开
,……(ⅲ)打开 ,加入适量浓盐酸,接通冷凝装置,加热管式炉开始反应。回答下列问题:
,加入适量浓盐酸,接通冷凝装置,加热管式炉开始反应。回答下列问题:(1)操作(ⅱ)的后续操作为
(2)装置D的产物均为有毒化合物,则该反应的化学方程式为
(3)A中反应结束后,再通入适量
 的目的是
的目的是Ⅱ.
 含量的测定
含量的测定将m g样品的水解液配成
 溶液,取
溶液,取 于锥形瓶中,滴加2~3滴
于锥形瓶中,滴加2~3滴 溶液为指示剂,用
溶液为指示剂,用 的
的 标准溶液滴定至终点,消耗溶液
标准溶液滴定至终点,消耗溶液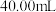 。
。已知:
难溶物 |
|
|
颜色 | 白 | 砖红 |
|
|
|
(4)该产品纯度为
(5)下列实验操作会导致产品纯度测定结果偏低的有________(填字母)。
| A.用待测液润洗锥形瓶 | B.样品暴露在空气中时间较长 |
| C.滴定终点时仰视读数 | D.滴加指示剂的量过多 |
2024·河南·二模 查看更多[2]
更新时间:2024-05-21 09:46:20
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。
其生产工艺如下:回答下列问题:
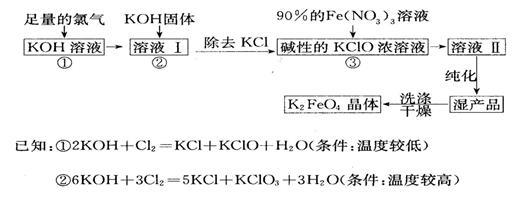
(1)该生产工艺应在_________________ (填“温度较高”或“温度较低”)的情况下进行,在溶液I中加入KOH固体的目的是_____________________ 。
(2)从溶液Ⅱ中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为_______________________ 。
(3)高铁酸钾作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,配平该反应的离子方程式:
______ FeO42- +______ H2O =______ Fe(OH)3(胶体)+______ O2↑ + ______ OH-
(4)目前,人们针对K2FeO4的稳定性进行了大量的探索,并取得了一定的进展。下列物质中有可能提高化合物K2FeO4水溶液稳定性的是(填代号)_________________ 。
a.亚硫酸钠 b.KOH c.醋酸 d.Fe(NO3)3
其生产工艺如下:回答下列问题:

(1)该生产工艺应在
(2)从溶液Ⅱ中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为
(3)高铁酸钾作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,配平该反应的离子方程式:
(4)目前,人们针对K2FeO4的稳定性进行了大量的探索,并取得了一定的进展。下列物质中有可能提高化合物K2FeO4水溶液稳定性的是(填代号)
a.亚硫酸钠 b.KOH c.醋酸 d.Fe(NO3)3
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】化合物 是一种由三种元素组成的重要化工原料,其
是一种由三种元素组成的重要化工原料,其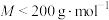 ,进行如图所示操作,已知
,进行如图所示操作,已知 、
、 含有一种相同的元素且在常温下均为气态化合物,其中气体
含有一种相同的元素且在常温下均为气态化合物,其中气体 可使品红溶液褪色(部分反应条件省略)。请回答:
可使品红溶液褪色(部分反应条件省略)。请回答:
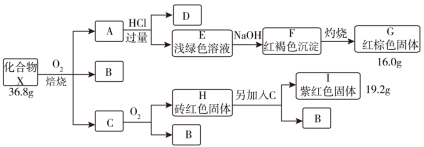
(1)组成 的元素有
的元素有___________ ,化合物 的化学式是
的化学式是___________ 。
(2)溶液 中溶质的主要成分是
中溶质的主要成分是___________ (用化学式表示)。
(3)写出 与
与 反应生成
反应生成 、
、 、
、 的化学方程式:
的化学方程式:___________ 。
(4)写出 与
与 反应生成
反应生成 和
和 的化学方程式:
的化学方程式:___________ 。
(5)请设计实验确定气体 的成分:
的成分:___________ 。
 是一种由三种元素组成的重要化工原料,其
是一种由三种元素组成的重要化工原料,其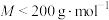 ,进行如图所示操作,已知
,进行如图所示操作,已知 、
、 含有一种相同的元素且在常温下均为气态化合物,其中气体
含有一种相同的元素且在常温下均为气态化合物,其中气体 可使品红溶液褪色(部分反应条件省略)。请回答:
可使品红溶液褪色(部分反应条件省略)。请回答:
(1)组成
 的元素有
的元素有 的化学式是
的化学式是(2)溶液
 中溶质的主要成分是
中溶质的主要成分是(3)写出
 与
与 反应生成
反应生成 、
、 、
、 的化学方程式:
的化学方程式:(4)写出
 与
与 反应生成
反应生成 和
和 的化学方程式:
的化学方程式:(5)请设计实验确定气体
 的成分:
的成分:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】对氯甲苯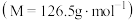 常作为染料、医药、有机合成的中间体,也可用作溶剂。其制取原理是:先用芳胺在一定条件下制成芳香重氮盐,然后在CuCl催化下,芳香重氮盐中的重氮基被氯原子取代生成芳香族氯化物。其原理如下:
常作为染料、医药、有机合成的中间体,也可用作溶剂。其制取原理是:先用芳胺在一定条件下制成芳香重氮盐,然后在CuCl催化下,芳香重氮盐中的重氮基被氯原子取代生成芳香族氯化物。其原理如下:
I.CuCl沉淀的制备
(1)将 、NaCl、
、NaCl、 、NaOH在水溶液中加热一段时间后,即可得到CuCl沉淀。
、NaOH在水溶液中加热一段时间后,即可得到CuCl沉淀。 俗称
俗称________ ,请写出该反应的离子方程式________ 。
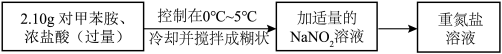
Ⅱ.重氮盐溶液的制备 溶液过量可能带来的弊端是
溶液过量可能带来的弊端是________ ;可用尿素 将其除去,生成的气体无污染,请写出该反应的离子方程式
将其除去,生成的气体无污染,请写出该反应的离子方程式________ 。
Ⅲ.对氯甲苯的制备________ ;________ (填序号)。
①熄灭酒精灯 ②打开旋塞 ③停止通冷凝水
(4)CuCl催化机理分两步进行,请补充完整:________ 。
(5)对氯甲苯粗品经过精制后,得到1.50g产品,本实验的产率最接近于________(填标号)。
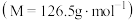 常作为染料、医药、有机合成的中间体,也可用作溶剂。其制取原理是:先用芳胺在一定条件下制成芳香重氮盐,然后在CuCl催化下,芳香重氮盐中的重氮基被氯原子取代生成芳香族氯化物。其原理如下:
常作为染料、医药、有机合成的中间体,也可用作溶剂。其制取原理是:先用芳胺在一定条件下制成芳香重氮盐,然后在CuCl催化下,芳香重氮盐中的重氮基被氯原子取代生成芳香族氯化物。其原理如下: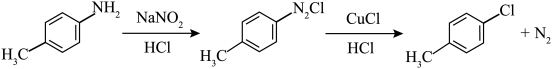
I.CuCl沉淀的制备
(1)将
 、NaCl、
、NaCl、 、NaOH在水溶液中加热一段时间后,即可得到CuCl沉淀。
、NaOH在水溶液中加热一段时间后,即可得到CuCl沉淀。 俗称
俗称Ⅱ.重氮盐溶液的制备
 溶液过量可能带来的弊端是
溶液过量可能带来的弊端是 将其除去,生成的气体无污染,请写出该反应的离子方程式
将其除去,生成的气体无污染,请写出该反应的离子方程式Ⅲ.对氯甲苯的制备
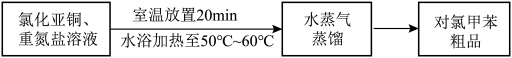
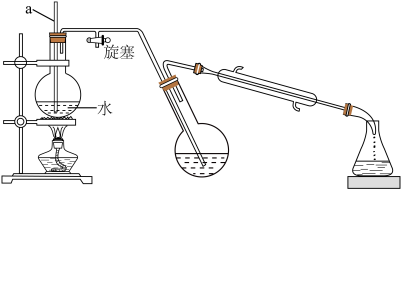
①熄灭酒精灯 ②打开旋塞 ③停止通冷凝水
(4)CuCl催化机理分两步进行,请补充完整:
①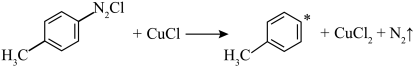
(5)对氯甲苯粗品经过精制后,得到1.50g产品,本实验的产率最接近于________(填标号)。
| A.55% | B.60% | C.65% | D.70% |
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】下图是实验室制备氯气并进行一系列相关实验的装置(部分夹持装置已略):

回答下列问题:
(1)装置A中是用MnO2和浓盐酸反应制备Cl2,请写出其反应的化学方程式:___________ 。
(2)装置B有安全瓶作用,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:___________ 。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ应依次放入:湿润的有色布条、___________ 、干燥的有色布条。
(4)装置E中潮湿的Cl2与Na2CO3反应,生成NaHCO3、Cl2O气体和另一种盐,试写出该反应的化学方程式:___________
(5)装置F的作用是:___________ 。
(6)反应G中的离子方程式为___________ 。
(7)设计最简单的实验方案验证E中生成的固体中存在HCO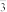 :
:___________ 。

回答下列问题:
(1)装置A中是用MnO2和浓盐酸反应制备Cl2,请写出其反应的化学方程式:
(2)装置B有安全瓶作用,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ应依次放入:湿润的有色布条、
(4)装置E中潮湿的Cl2与Na2CO3反应,生成NaHCO3、Cl2O气体和另一种盐,试写出该反应的化学方程式:
(5)装置F的作用是:
(6)反应G中的离子方程式为
(7)设计最简单的实验方案验证E中生成的固体中存在HCO
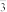 :
:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐2】亚硝酰氯(NOCl)为红褐色液体或黄色气体,其熔点为-64.5℃,沸点为-5.5℃,具有刺鼻恶臭味,遇水剧烈水解,易溶于浓硫酸。常可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温、常压下合成。其制备装置如图所示。
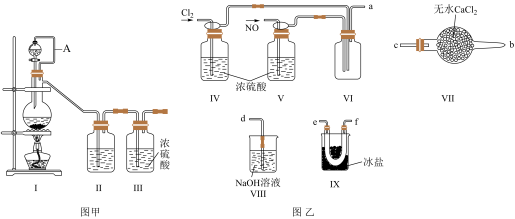
(1)用图甲中装置制备纯净干燥的原料气,试写出该装置制备氯气的离子方程式:___________ 。
(2)将制得的NO和 通入图乙对应装置制备NOCl。
通入图乙对应装置制备NOCl。
①装置连接顺序为a→___________ (按气流自左向右方向,用小写字母表示);
②装置Ⅳ、Ⅴ的作用是___________ 、___________ 。
(3)实验开始时,先通入氯气,再通入NO,原因是___________ 。
(4)有同学认为多余的氯气可以通过下列装置暂时储存然后再利用,下列可以用作氯气的储气装置的是___________ (填序号)。

(5)制得的NOCl中可能含有少量 杂质,为测定产品纯度进行如下实验:称取3.500g样品溶于NaOH配制成1000.00mL溶液,用移液管取10.00mL溶液,加入几滴
杂质,为测定产品纯度进行如下实验:称取3.500g样品溶于NaOH配制成1000.00mL溶液,用移液管取10.00mL溶液,加入几滴 溶液作指示剂,用足量硝酸酸化的0.020 mol/L
溶液作指示剂,用足量硝酸酸化的0.020 mol/L  溶液进行滴定,消耗
溶液进行滴定,消耗 溶液20.00 mL。
溶液20.00 mL。
①滴定终点的现象是___________ ;
②样品的纯度为___________ %(保留1位小数)。

(1)用图甲中装置制备纯净干燥的原料气,试写出该装置制备氯气的离子方程式:
(2)将制得的NO和
 通入图乙对应装置制备NOCl。
通入图乙对应装置制备NOCl。①装置连接顺序为a→
②装置Ⅳ、Ⅴ的作用是
(3)实验开始时,先通入氯气,再通入NO,原因是
(4)有同学认为多余的氯气可以通过下列装置暂时储存然后再利用,下列可以用作氯气的储气装置的是

(5)制得的NOCl中可能含有少量
 杂质,为测定产品纯度进行如下实验:称取3.500g样品溶于NaOH配制成1000.00mL溶液,用移液管取10.00mL溶液,加入几滴
杂质,为测定产品纯度进行如下实验:称取3.500g样品溶于NaOH配制成1000.00mL溶液,用移液管取10.00mL溶液,加入几滴 溶液作指示剂,用足量硝酸酸化的0.020 mol/L
溶液作指示剂,用足量硝酸酸化的0.020 mol/L  溶液进行滴定,消耗
溶液进行滴定,消耗 溶液20.00 mL。
溶液20.00 mL。①滴定终点的现象是
②样品的纯度为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】氯化铁是一种净水剂和化工产品。某小组设计实验制备 并测定产品纯度。
并测定产品纯度。
实验(一)制备 。
。
某小组设计如下装置制备氯化铁。已知: 易升华,遇水蒸气易发生水解反应。
易升华,遇水蒸气易发生水解反应。___________ (填名称)。
(2)写出装置A中发生反应的离子方程式:___________ 。
(3)尾气处理宜选择___________ (填序号)。___________ 。
(5)实验完毕后,取少量装置D中固体溶于水,滴加 溶液,产生蓝色沉淀,有同学认为装置D中氯气与铁反应生成了
溶液,产生蓝色沉淀,有同学认为装置D中氯气与铁反应生成了 ,请你评价(指出正误并分析理由):
,请你评价(指出正误并分析理由):___________ 。
实验(二)测定 样品的纯度。
样品的纯度。
已知: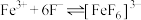 (无色,很稳定),
(无色,很稳定),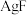 易溶于水且完全电离。
易溶于水且完全电离。
(6)实验步骤如下:
步骤1:准确称取 样品配成
样品配成 溶液,准确量取
溶液,准确量取 配制好的溶液于维形瓶中;
配制好的溶液于维形瓶中;
步骤2:向锥形瓶中加入适量 溶液(恰好与铁离子完全反应),用力振荡,再加入
溶液(恰好与铁离子完全反应),用力振荡,再加入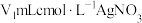 溶液(过量)使
溶液(过量)使 完全沉淀;
完全沉淀;
步骤3:向其中加入硝基苯,用力振荡,使沉淀表面被有机物覆盖;
步骤4:加入3滴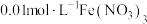 溶液,用
溶液,用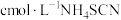 溶液滴定过量的
溶液滴定过量的 至终点,消耗
至终点,消耗 溶液的体积为
溶液的体积为 。已知:常温下,
。已知:常温下, ,
, 。
。
①加入 的目的是
的目的是___________ 。滴定终点时溶液颜色变为___________ 。
②测得样品中 的质量分数为
的质量分数为___________ (用含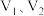 、c、m的代数式表示)。
、c、m的代数式表示)。
③下列操作会使所测结果偏低的是___________ (填字母)。
A.滴定前仰视读数,滴定终点俯视读数 B.锥形瓶没有干燥
C.滴定管没有用 溶液润洗 D.省略了步骤3
溶液润洗 D.省略了步骤3
 并测定产品纯度。
并测定产品纯度。实验(一)制备
 。
。某小组设计如下装置制备氯化铁。已知:
 易升华,遇水蒸气易发生水解反应。
易升华,遇水蒸气易发生水解反应。
(2)写出装置A中发生反应的离子方程式:
(3)尾气处理宜选择

(5)实验完毕后,取少量装置D中固体溶于水,滴加
 溶液,产生蓝色沉淀,有同学认为装置D中氯气与铁反应生成了
溶液,产生蓝色沉淀,有同学认为装置D中氯气与铁反应生成了 ,请你评价(指出正误并分析理由):
,请你评价(指出正误并分析理由):实验(二)测定
 样品的纯度。
样品的纯度。已知:
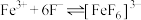 (无色,很稳定),
(无色,很稳定),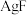 易溶于水且完全电离。
易溶于水且完全电离。(6)实验步骤如下:
步骤1:准确称取
 样品配成
样品配成 溶液,准确量取
溶液,准确量取 配制好的溶液于维形瓶中;
配制好的溶液于维形瓶中;步骤2:向锥形瓶中加入适量
 溶液(恰好与铁离子完全反应),用力振荡,再加入
溶液(恰好与铁离子完全反应),用力振荡,再加入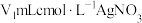 溶液(过量)使
溶液(过量)使 完全沉淀;
完全沉淀;步骤3:向其中加入硝基苯,用力振荡,使沉淀表面被有机物覆盖;
步骤4:加入3滴
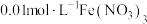 溶液,用
溶液,用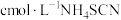 溶液滴定过量的
溶液滴定过量的 至终点,消耗
至终点,消耗 溶液的体积为
溶液的体积为 。已知:常温下,
。已知:常温下, ,
, 。
。①加入
 的目的是
的目的是②测得样品中
 的质量分数为
的质量分数为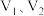 、c、m的代数式表示)。
、c、m的代数式表示)。③下列操作会使所测结果偏低的是
A.滴定前仰视读数,滴定终点俯视读数 B.锥形瓶没有干燥
C.滴定管没有用
 溶液润洗 D.省略了步骤3
溶液润洗 D.省略了步骤3
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐1】苯甲酸可用作食品防腐剂。实验室可通过甲苯氧化制苯甲酸,其反应原理简示如下:

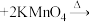
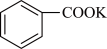


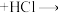


实验步骤:
①在装有温度计、冷凝管和搅拌器的三颈烧瓶中加入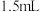 甲苯、
甲苯、 水和
水和 (约
(约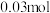 )高锰酸钾,慢慢开启搅拌器,并加热回流反应。
)高锰酸钾,慢慢开启搅拌器,并加热回流反应。
②停止加热,继续搅拌,冷却片刻后,从冷凝管上口慢慢加入适量饱和亚硫酸氢钠溶液,并将反应混合物趁热过滤,用少量热水洗涤滤渣。合并滤液和洗涤液,于冰水浴中冷却,然后用浓盐酸酸化至苯甲酸析出完全。将析出的苯甲酸过滤,用少量冷水洗涤,放在沸水浴上干燥。称量,粗产品为 。
。
③纯度测定:称取经过提纯后的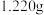 产品,配成
产品,配成 甲醇溶液,取
甲醇溶液,取 溶液与
溶液与 溶液反应,消耗
溶液反应,消耗 的物质的量为
的物质的量为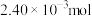 。
。
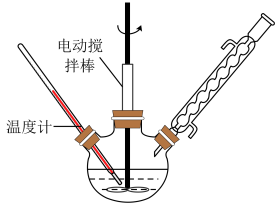
回答下列问题:
(1)步骤①中当看到__________ 现象即可判断反应已完成,可以停止加热。
(2)步骤②中加入适量饱和亚硫酸氢钠溶液的作用是__________ 。
(3)测定粗产品的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔,该同学推测粗产品是苯甲酸与 的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确。按要求填写下列表格:
的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确。按要求填写下列表格:
(4)若要得到纯度更高的苯甲酸可通过__________ 的方法对粗产品提纯。在该操作中,不需要用到的仪器是__________ 。
A. B.
B. C.
C. D.
D.
(5)步骤③纯度测定,根据有关数据计算粗产品中苯甲酸质量分数为__________ 。




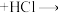


名称 |
| 熔点/℃ | 沸点/℃ | 密度 | 溶解性 |
甲苯 | 92 |
| 110.6 | 0.867 | 不溶于水,易溶于乙醇 |
苯甲酸 | 122 | 122.4(100℃左右开始升华) | 248 | 微溶于冷水,易溶于乙醇,热水 |
①在装有温度计、冷凝管和搅拌器的三颈烧瓶中加入
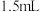 甲苯、
甲苯、 水和
水和 (约
(约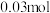 )高锰酸钾,慢慢开启搅拌器,并加热回流反应。
)高锰酸钾,慢慢开启搅拌器,并加热回流反应。②停止加热,继续搅拌,冷却片刻后,从冷凝管上口慢慢加入适量饱和亚硫酸氢钠溶液,并将反应混合物趁热过滤,用少量热水洗涤滤渣。合并滤液和洗涤液,于冰水浴中冷却,然后用浓盐酸酸化至苯甲酸析出完全。将析出的苯甲酸过滤,用少量冷水洗涤,放在沸水浴上干燥。称量,粗产品为
 。
。③纯度测定:称取经过提纯后的
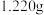 产品,配成
产品,配成 甲醇溶液,取
甲醇溶液,取 溶液与
溶液与 溶液反应,消耗
溶液反应,消耗 的物质的量为
的物质的量为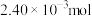 。
。
回答下列问题:
(1)步骤①中当看到
(2)步骤②中加入适量饱和亚硫酸氢钠溶液的作用是
(3)测定粗产品的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔,该同学推测粗产品是苯甲酸与
 的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确。按要求填写下列表格:
的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确。按要求填写下列表格:序号 | 实验方案 | 实验现象 | 结论 |
① | 将粗产品加入水中,加热溶解, | 得到白色晶体和无色溶液 | — |
② | 取少量滤液于试管中,滴入适量的硝酸酸化的 溶液 溶液 | 生成白色沉淀 | 滤液含 |
③ | 干燥白色晶体, | 白色晶体是苯甲酸 |
A.
 B.
B. C.
C. D.
D.
(5)步骤③纯度测定,根据有关数据计算粗产品中苯甲酸质量分数为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】Ⅰ.某化学兴趣小组利用下图所示装置探究金属的电化学防护,观察到的实验现象是:锌电极不断溶解,铁电极表面有气泡产生。
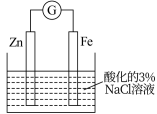
(1)写出负极的电极反应式:___________ 。
(2)某学生认为,铁电极可能参与反应,于是设计了如下实验:
①取
 溶液
溶液 于试管中,加入过量铁粉,取试管的上层清液加入2滴
于试管中,加入过量铁粉,取试管的上层清液加入2滴 溶液,实验现象是:
溶液,实验现象是:___________ ,发生反应的离子方程式为___________ 。
②取铁电极附近的溶液于试管中,加入2滴 溶液,未见明显现象;
溶液,未见明显现象;
③另取少量铁电极附近的溶液于试管中加入2滴___________ 溶液,未见溶液变红;
结论:铁电极附近溶液不含 和
和 。此种金属的电化学防护叫
。此种金属的电化学防护叫___________ 法。
Ⅱ.过氧化钙可以用于改善地表水质、处理含重金属粒子废水和治理赤潮,也可用于应急供氧等。某小组测定样品中 的含量的实验步骤是:
的含量的实验步骤是:
第一步:准确称取mg样品 于锥形瓶中,加入适量蒸馏水和过量的
于锥形瓶中,加入适量蒸馏水和过量的
 晶体的再滴入少量
晶体的再滴入少量 的
的 溶液,充分反应。
溶液,充分反应。
第二步:向上述锥形瓶中加入几滴淀粉溶液。
第三步:用 的
的 溶液进行滴定,装有
溶液进行滴定,装有 溶液的滴定管起始和终点读数如图所示:
溶液的滴定管起始和终点读数如图所示:
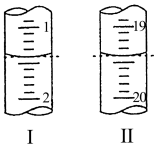
已知: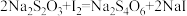
(3)判断此滴定实验达到终点的方法:___________ 。
(4) 的质量分数为
的质量分数为___________ (用字母表示)。
(5)某同学第一步和第二步的操作都很规范,第三步滴速太慢,这样测得的 的质量分数可能
的质量分数可能___________ (填“不受影响”、“偏低”或“偏高”),原因是___________ 。

(1)写出负极的电极反应式:
(2)某学生认为,铁电极可能参与反应,于是设计了如下实验:
①取

 溶液
溶液 于试管中,加入过量铁粉,取试管的上层清液加入2滴
于试管中,加入过量铁粉,取试管的上层清液加入2滴 溶液,实验现象是:
溶液,实验现象是:②取铁电极附近的溶液于试管中,加入2滴
 溶液,未见明显现象;
溶液,未见明显现象;③另取少量铁电极附近的溶液于试管中加入2滴
结论:铁电极附近溶液不含
 和
和 。此种金属的电化学防护叫
。此种金属的电化学防护叫Ⅱ.过氧化钙可以用于改善地表水质、处理含重金属粒子废水和治理赤潮,也可用于应急供氧等。某小组测定样品中
 的含量的实验步骤是:
的含量的实验步骤是:第一步:准确称取mg样品
 于锥形瓶中,加入适量蒸馏水和过量的
于锥形瓶中,加入适量蒸馏水和过量的
 晶体的再滴入少量
晶体的再滴入少量 的
的 溶液,充分反应。
溶液,充分反应。第二步:向上述锥形瓶中加入几滴淀粉溶液。
第三步:用
 的
的 溶液进行滴定,装有
溶液进行滴定,装有 溶液的滴定管起始和终点读数如图所示:
溶液的滴定管起始和终点读数如图所示:
已知:
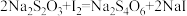
(3)判断此滴定实验达到终点的方法:
(4)
 的质量分数为
的质量分数为(5)某同学第一步和第二步的操作都很规范,第三步滴速太慢,这样测得的
 的质量分数可能
的质量分数可能
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】铬(Cr)属于分布较广的元素之一,其单质与化合物在颜料、纺织、电镀、制革等方面都有着重要作用。
(1)制备氯化铬晶体(CrCl3·6H2O)。氯化铬晶体是一种重要的工业原料,可通过甲醇还原铬酸钠(Na2CrO4)制备。其实验装置和步骤如下:
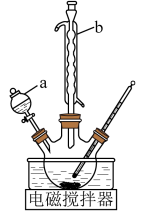
i. 将一定量铬酸钠、甲醇与水的混合物加入三颈瓶;
ii.缓慢滴加足量盐酸,保持温度在100℃反应三小时;
iii.冷却后加入NaOH,得到Cr(OH)3沉淀;
iv.洗净沉淀,加入理论用量1.1倍的盐酸溶解后,通过结晶法得到CrCl3·6H2O晶体。
回答下列问题:
①装置b的主要作用除导气外,还有_______ 。
② 步骤ii中的反应会有CO2生成,请写出反应的化学方程式_______ 。
③步骤iv中,盐酸过量的原因是_______ 。
(2)测定氯化铬晶体(CrCl3·6H2O)的质量分数。
i.称取样品0.6000 g,加水溶解并配成250.0 mL的溶液。
ii.移取25.00 mL样品溶液于带塞的锥形瓶中,加热至沸后加入稍过量的Na2O2,稀释并加热煮沸,再加入过量的硫酸酸化,将Cr3+氧化为 ;再加入过量KI固体,加塞摇匀,使铬完全以Cr3+的形式存在。
;再加入过量KI固体,加塞摇匀,使铬完全以Cr3+的形式存在。
iii.加入1 mL淀粉溶液,用0.025 0 mol·L-1标准Na2S2O3溶液滴定至终点,平行测定3次,平均消耗标准Na2S2O3溶液24.00 mL。
已知反应: +I-+H+——I2+Cr3++H2O(未配平);I2+2
+I-+H+——I2+Cr3++H2O(未配平);I2+2 =
= +2I-。
+2I-。
计算CrCl3·6H2O的质量分数(写出计算过程)_______ 。
(3)已知:碱性条件下,H2O2能把CrO 氧化为
氧化为 ;酸性条件下,H2O2能把
;酸性条件下,H2O2能把 还原为Cr3+;Pb2+形成Pb(OH)2开始沉淀pH值为5,完全沉淀pH值为8。
还原为Cr3+;Pb2+形成Pb(OH)2开始沉淀pH值为5,完全沉淀pH值为8。
以CrCl3·6H2O和Pb(NO3)2为原料可制备铬酸铅(PbCrO4难溶于水),具体步骤如下:边搅拌边向CrCl3·6H2O晶体中加入2 mol·L-1的NaOH溶液至产生的沉淀完全溶解,得到NaCrO2溶液,_______ 。再滴加0.5 mol·L-1的Pb(NO3)2溶液至不再产生沉淀,过滤,冷水洗涤,烘干,得到铬酸铅产品[实验中须使用的试剂:H2O2溶液、6 mol·L-1的醋酸溶液]。
(1)制备氯化铬晶体(CrCl3·6H2O)。氯化铬晶体是一种重要的工业原料,可通过甲醇还原铬酸钠(Na2CrO4)制备。其实验装置和步骤如下:

i. 将一定量铬酸钠、甲醇与水的混合物加入三颈瓶;
ii.缓慢滴加足量盐酸,保持温度在100℃反应三小时;
iii.冷却后加入NaOH,得到Cr(OH)3沉淀;
iv.洗净沉淀,加入理论用量1.1倍的盐酸溶解后,通过结晶法得到CrCl3·6H2O晶体。
回答下列问题:
①装置b的主要作用除导气外,还有
② 步骤ii中的反应会有CO2生成,请写出反应的化学方程式
③步骤iv中,盐酸过量的原因是
(2)测定氯化铬晶体(CrCl3·6H2O)的质量分数。
i.称取样品0.6000 g,加水溶解并配成250.0 mL的溶液。
ii.移取25.00 mL样品溶液于带塞的锥形瓶中,加热至沸后加入稍过量的Na2O2,稀释并加热煮沸,再加入过量的硫酸酸化,将Cr3+氧化为
 ;再加入过量KI固体,加塞摇匀,使铬完全以Cr3+的形式存在。
;再加入过量KI固体,加塞摇匀,使铬完全以Cr3+的形式存在。iii.加入1 mL淀粉溶液,用0.025 0 mol·L-1标准Na2S2O3溶液滴定至终点,平行测定3次,平均消耗标准Na2S2O3溶液24.00 mL。
已知反应:
 +I-+H+——I2+Cr3++H2O(未配平);I2+2
+I-+H+——I2+Cr3++H2O(未配平);I2+2 =
= +2I-。
+2I-。计算CrCl3·6H2O的质量分数(写出计算过程)
(3)已知:碱性条件下,H2O2能把CrO
 氧化为
氧化为 ;酸性条件下,H2O2能把
;酸性条件下,H2O2能把 还原为Cr3+;Pb2+形成Pb(OH)2开始沉淀pH值为5,完全沉淀pH值为8。
还原为Cr3+;Pb2+形成Pb(OH)2开始沉淀pH值为5,完全沉淀pH值为8。以CrCl3·6H2O和Pb(NO3)2为原料可制备铬酸铅(PbCrO4难溶于水),具体步骤如下:边搅拌边向CrCl3·6H2O晶体中加入2 mol·L-1的NaOH溶液至产生的沉淀完全溶解,得到NaCrO2溶液,
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】氮化镓(GaN)在5G基站及工业互联网系统建设等方面用途广泛。从砷化镓废料(主要成分为GaAs,含Fe2O3、 SiO2和CaCO3等杂质)中回收砷,制备GaN的工艺流程如图:
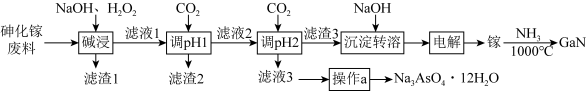
已知:①Ga与Al同主族,化学性质相似;
②离子完全沉淀的pH值: 为8,
为8, 为5.5。
为5.5。
回答下列问题:
(1)为了提高“碱浸”效率应采用的措施是_______ (写 出一种措施)。
(2)“滤液1”中含有NaGaO2等溶质, “碱浸”时反应的离子方程式为_______ 。“滤渣1”的成分为_______ (填化学式)。
(3)通CO2两次调pH的原因是_______ 。
(4)“操作a”为_______ 、过滤、洗涤、干燥。
(5)“电解”时阴极的电极反应为_______ 。
(6)制备GaN时,参与反应的氧化剂与还原剂的物质的量之比为_______ 。
(7)取m克GaN样品溶于足量的热NaOH溶液(GaN+OH- +H2O = +NH3↑)中,用H3BO3溶液将产生的NH3完全吸收,用c mol·L-1的盐酸滴定,消耗盐酸V mL,则样品的纯度是
+NH3↑)中,用H3BO3溶液将产生的NH3完全吸收,用c mol·L-1的盐酸滴定,消耗盐酸V mL,则样品的纯度是_______ 。(已知: NH3+H3BO3 =NH3·H3BO3;NH3·H3BO3 +HCl=NH4Cl+H3BO3 )

已知:①Ga与Al同主族,化学性质相似;
②离子完全沉淀的pH值:
 为8,
为8, 为5.5。
为5.5。回答下列问题:
(1)为了提高“碱浸”效率应采用的措施是
(2)“滤液1”中含有NaGaO2等溶质, “碱浸”时反应的离子方程式为
(3)通CO2两次调pH的原因是
(4)“操作a”为
(5)“电解”时阴极的电极反应为
(6)制备GaN时,参与反应的氧化剂与还原剂的物质的量之比为
(7)取m克GaN样品溶于足量的热NaOH溶液(GaN+OH- +H2O =
 +NH3↑)中,用H3BO3溶液将产生的NH3完全吸收,用c mol·L-1的盐酸滴定,消耗盐酸V mL,则样品的纯度是
+NH3↑)中,用H3BO3溶液将产生的NH3完全吸收,用c mol·L-1的盐酸滴定,消耗盐酸V mL,则样品的纯度是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】被誉为“工业维他命”的铂族金属钌(Ru)广泛用于航天航空、石油化学、信息传感工业、制药等高科技领域。以下工艺实现了电子废弃物中铂族金属钌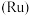 的回收利用。已知电子废弃物主要成分为
的回收利用。已知电子废弃物主要成分为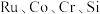 等物质,请回答以下问题:
等物质,请回答以下问题: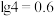 ②常见物质的
②常见物质的 如下表所示:
如下表所示:
(1)为加快“酸浸”时的浸取速率,下列措施中无法达到目的是______ (填字母)。
a.将样品粉碎 b.延长浸取时间 c.充分搅拌 d.适当增加盐酸浓度 e.适当升高温度
(2)滤渣2为______ 。
(3)“氧化溶浸”环节生成配离子 反应的离子方程式为
反应的离子方程式为______ 。
(4)“还原1”环节所需氧化剂和还原剂的物质的量之比为1:1,则 的氧化产物为
的氧化产物为______ 。
(5)滤液1中含 和
和 的浓度分别为
的浓度分别为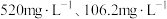 ,“调
,“调 ”时调
”时调 的范围为
的范围为______ 。(已知:当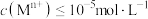 时,可认为
时,可认为 已经沉淀完全)
已经沉淀完全)
(6)沉钴。向除杂后的 溶液中加入
溶液中加入 溶液或
溶液或 溶液作沉淀剂,可得到
溶液作沉淀剂,可得到 ,不能用同浓度的
,不能用同浓度的 溶液代替
溶液代替 溶液的原因是
溶液的原因是______ 。
(7)制备 。将所得的
。将所得的 草酸钴晶体
草酸钴晶体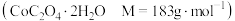 高温灼烧,其热重分析曲线如图:
高温灼烧,其热重分析曲线如图: 点对应的物质的化学式:
点对应的物质的化学式:______ ,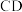 段发生反应的化学方程式为:
段发生反应的化学方程式为:______ 。
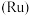 的回收利用。已知电子废弃物主要成分为
的回收利用。已知电子废弃物主要成分为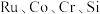 等物质,请回答以下问题:
等物质,请回答以下问题: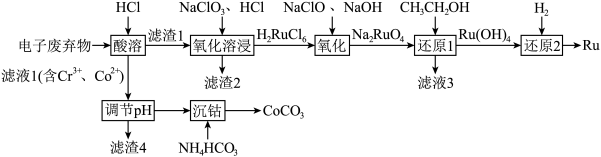
 ②常见物质的
②常见物质的 如下表所示:
如下表所示:化合物 |
|
|
|
|
|
(1)为加快“酸浸”时的浸取速率,下列措施中无法达到目的是
a.将样品粉碎 b.延长浸取时间 c.充分搅拌 d.适当增加盐酸浓度 e.适当升高温度
(2)滤渣2为
(3)“氧化溶浸”环节生成配离子
 反应的离子方程式为
反应的离子方程式为(4)“还原1”环节所需氧化剂和还原剂的物质的量之比为1:1,则
 的氧化产物为
的氧化产物为(5)滤液1中含
 和
和 的浓度分别为
的浓度分别为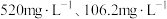 ,“调
,“调 ”时调
”时调 的范围为
的范围为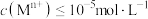 时,可认为
时,可认为 已经沉淀完全)
已经沉淀完全)(6)沉钴。向除杂后的
 溶液中加入
溶液中加入 溶液或
溶液或 溶液作沉淀剂,可得到
溶液作沉淀剂,可得到 ,不能用同浓度的
,不能用同浓度的 溶液代替
溶液代替 溶液的原因是
溶液的原因是(7)制备
 。将所得的
。将所得的 草酸钴晶体
草酸钴晶体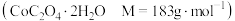 高温灼烧,其热重分析曲线如图:
高温灼烧,其热重分析曲线如图: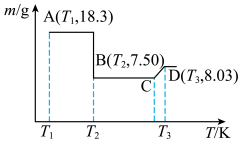
 点对应的物质的化学式:
点对应的物质的化学式: 段发生反应的化学方程式为:
段发生反应的化学方程式为:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】二氧化氯( )常用作饮用水的消毒杀菌剂,沸点为11.0℃,某实验小组在实验室用如下装置制备
)常用作饮用水的消毒杀菌剂,沸点为11.0℃,某实验小组在实验室用如下装置制备 并研究其相关性质。
并研究其相关性质。 气体浓度过高时易爆炸分解;②稳定剂可吸收
气体浓度过高时易爆炸分解;②稳定剂可吸收 ,生成
,生成 ,使用时加酸只释放
,使用时加酸只释放 一种气体。
一种气体。
回答下列问题:
Ⅰ.制备 :
:
(1)打开 、
、 ,关闭
,关闭 ,将浓HCl滴入装置A的圆底烧瓶中。
,将浓HCl滴入装置A的圆底烧瓶中。
①盛装浓HCl的仪器名称为___________ 。
②装置A中发生反应的离子方程式为___________ 。
(2)装置B中盛放的试剂是___________ 。
(3)向装置D中通入 的目的是
的目的是___________ ;装置D中发生反应的化学方程式为___________ 。
Ⅱ.验证 的氧化性:
的氧化性:
(4)停止滴加装置A中的浓HCl,待装置D中反应完全时,使___________ (用 、
、 、
、 填空,下同)开启,
填空,下同)开启,___________ 关闭,再将稀盐酸滴入稳定剂中。
(5)观察到装置G中出现的现象是___________ 。
Ⅲ.测定某 溶液的浓度:
溶液的浓度:
(6)为测定某 溶液的浓度,进行如下实验:准确量取10.00mL
溶液的浓度,进行如下实验:准确量取10.00mL 溶液,酸化后加入过量KI溶液,充分反应后,加入几滴淀粉溶液,用
溶液,酸化后加入过量KI溶液,充分反应后,加入几滴淀粉溶液,用
 标准溶液滴定至终点;重复上述操作2~3次,平均消耗
标准溶液滴定至终点;重复上述操作2~3次,平均消耗 标准溶液30.00mL。已知:
标准溶液30.00mL。已知: ,
, 。则该
。则该 溶液中
溶液中 的物质的量浓度为
的物质的量浓度为___________  。
。
 )常用作饮用水的消毒杀菌剂,沸点为11.0℃,某实验小组在实验室用如下装置制备
)常用作饮用水的消毒杀菌剂,沸点为11.0℃,某实验小组在实验室用如下装置制备 并研究其相关性质。
并研究其相关性质。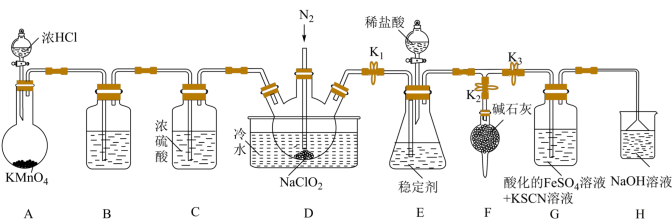
 气体浓度过高时易爆炸分解;②稳定剂可吸收
气体浓度过高时易爆炸分解;②稳定剂可吸收 ,生成
,生成 ,使用时加酸只释放
,使用时加酸只释放 一种气体。
一种气体。回答下列问题:
Ⅰ.制备
 :
:(1)打开
 、
、 ,关闭
,关闭 ,将浓HCl滴入装置A的圆底烧瓶中。
,将浓HCl滴入装置A的圆底烧瓶中。①盛装浓HCl的仪器名称为
②装置A中发生反应的离子方程式为
(2)装置B中盛放的试剂是
(3)向装置D中通入
 的目的是
的目的是Ⅱ.验证
 的氧化性:
的氧化性:(4)停止滴加装置A中的浓HCl,待装置D中反应完全时,使
 、
、 、
、 填空,下同)开启,
填空,下同)开启,(5)观察到装置G中出现的现象是
Ⅲ.测定某
 溶液的浓度:
溶液的浓度:(6)为测定某
 溶液的浓度,进行如下实验:准确量取10.00mL
溶液的浓度,进行如下实验:准确量取10.00mL 溶液,酸化后加入过量KI溶液,充分反应后,加入几滴淀粉溶液,用
溶液,酸化后加入过量KI溶液,充分反应后,加入几滴淀粉溶液,用
 标准溶液滴定至终点;重复上述操作2~3次,平均消耗
标准溶液滴定至终点;重复上述操作2~3次,平均消耗 标准溶液30.00mL。已知:
标准溶液30.00mL。已知: ,
, 。则该
。则该 溶液中
溶液中 的物质的量浓度为
的物质的量浓度为 。
。
您最近一年使用:0次