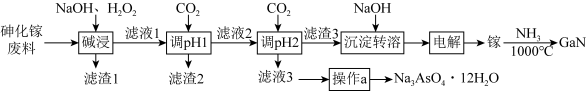
已知:①Ga与Al同主族,化学性质相似;
②离子完全沉淀的pH值:
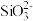 为8,
为8, 为5.5。
为5.5。回答下列问题:
(1)为了提高“碱浸”效率应采用的措施是
(2)“滤液1”中含有NaGaO2等溶质, “碱浸”时反应的离子方程式为
(3)通CO2两次调pH的原因是
(4)“操作a”为
(5)“电解”时阴极的电极反应为
(6)制备GaN时,参与反应的氧化剂与还原剂的物质的量之比为
(7)取m克GaN样品溶于足量的热NaOH溶液(GaN+OH- +H2O =
 +NH3↑)中,用H3BO3溶液将产生的NH3完全吸收,用c mol·L-1的盐酸滴定,消耗盐酸V mL,则样品的纯度是
+NH3↑)中,用H3BO3溶液将产生的NH3完全吸收,用c mol·L-1的盐酸滴定,消耗盐酸V mL,则样品的纯度是相似题推荐
Ⅰ.CO与H2反应合成甲醇
Ⅱ.CO2与H2反应合成甲醇 CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)
(1)上述反应Ⅰ是原子经济性反应,写出化学反应方程式
(2)在工业上,为了提高上述反应Ⅱ的反应速率,除了采用合适的催化剂之外,还可以采取的措施是
(3)一定温度下,在容积固定的密闭容器中发生反应Ⅱ,下列可以表明反应达到化学平衡状态的是
a.单位时间消耗nmolCO2的同时,消耗3n mol的H2
b.容器内CH3OH的浓度不再改变
c.容器内气体压强不再改变
d.容器内气体密度不再改变
(4)生成1mol CH3OH放出 a kJ的能量,反应Ⅰ中拆开1mol化学键所需的能量(E)的相关数据如下:
| 化学键 | H—H | C—O | CO中的 C O O | H—O | C—H |
| E(kJ) | m | n | E1 | x | y |
根据相关数据计算拆开1molC
 O所需的能量E1=
O所需的能量E1=(5) H2还原CO2电化学法制备甲醇的工作原理如下图所示:


通入H2 的一端是电池的
 CH3OCH3(g) + H2O(g) ΔH1
CH3OCH3(g) + H2O(g) ΔH1(1)二甲醚亦可通过合成气反应制得,相关热化学方程式如下:
2H2(g)+ CO(g)
 CH3OH(g) ΔH2
CH3OH(g) ΔH2CO(g)+ H2O(g)
 CO2(g)+ H2(g) ΔH3
CO2(g)+ H2(g) ΔH33H2(g)+ 3CO(g)
 CH3OCH3(g)+ CO2 (g) ΔH4
CH3OCH3(g)+ CO2 (g) ΔH4则ΔH1=
(2)经查阅资料,上述反应平衡状态下 Kp 的计算式为:
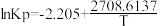 (Kp 为以分压表示的平衡常数,T 为热力学温度)。且催化剂吸附 H2O(g)的量会受压强影响,从而进一步影响催化效率。)
(Kp 为以分压表示的平衡常数,T 为热力学温度)。且催化剂吸附 H2O(g)的量会受压强影响,从而进一步影响催化效率。)①在一定温度范围内,随温度升高,CH3OH(g)脱水转化为二甲醚的倾向
②某温度下(此时 Kp=100),在密闭容器中加入CH3OH,反应到某时刻测得各组分的分压如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 分压/MPa | 0.50 | 0.50 | 0.50 |
此时正、逆反应速率的大小:v正
③200℃时,在密闭容器中加入一定量甲醇 CH3OH,反应到达平衡状态时,体系中CH3OCH3(g)的物质的量分数为
A.<
 B.
B. C.
C. ~
~ D.
D. E.>
E.>
④300℃时,使 CH3OH(g)以一定流速通过催化剂,V/F (按原料流率的催化剂量)、压强对甲醇转化率影响如图1所示。请解释甲醇转化率随压强(压力)变化的规律和产生这种变化的原因,规律
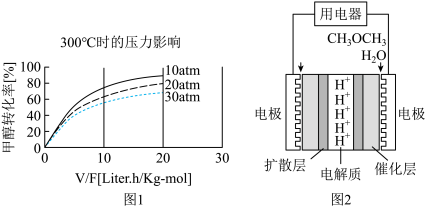
(3)直接二甲醚燃料电池有望大规模商业化应用,工作原理如图2所示。
①该电池的负极反应式为:
②某直接二甲醚燃料电池装置的能量利用率为 50%,现利用该燃料电池电解氯化铜溶液,若消耗 2.3g 二甲醚,得到铜的质量为
 )经碱初步溶解后得到的赤泥含有丰富的钪元素,另含少量CaO、
)经碱初步溶解后得到的赤泥含有丰富的钪元素,另含少量CaO、 、
、 、
、 等氧化物。一种从赤泥中提取氧化钪的工艺流程如下图所示,已知:P2O4(磷酸酯浸取剂)是一种酸性萃取剂。
等氧化物。一种从赤泥中提取氧化钪的工艺流程如下图所示,已知:P2O4(磷酸酯浸取剂)是一种酸性萃取剂。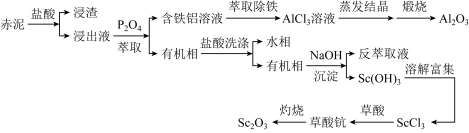
回答下列问题:
(1)写出铝土矿经碱初步溶解时所发生的主要离子方程式:
(2)写出赤泥经盐酸处理后所得“浸渣”的一种用途:
(3)反萃取时,
 完全沉淀(浓度为
完全沉淀(浓度为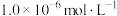 )时,反萃取液的pH为
)时,反萃取液的pH为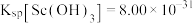 ,
, ,结果保留小数点后2位)。
,结果保留小数点后2位)。(4)草酸钪灼烧分解在无氧环境下进行,其反应的化学方程式为
(5)在流程中可循环使用的物质有
 )是一种重要的化工原料。丙烯水化法制异丙醇(
)是一种重要的化工原料。丙烯水化法制异丙醇( )以及电解法制丙烯都是重要的化工技术。
)以及电解法制丙烯都是重要的化工技术。I.
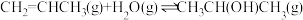
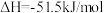
(1)有利于该反应自发进行的条件是
(2)根据下图回答问题:
①在
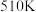 、
、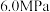 条件下,在密闭容器中充入一定量的
条件下,在密闭容器中充入一定量的 和
和 合成
合成 ,下列叙述能说明此反应达到平衡状态的是
,下列叙述能说明此反应达到平衡状态的是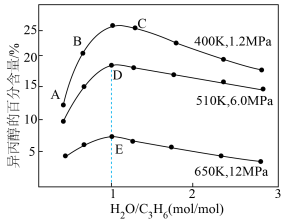
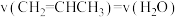 B.
B. 和
和 的转化率相等
的转化率相等C.混合气体的密度保持不变 D.
 的体积分数保持不变
的体积分数保持不变②A、B、C三点,丙烯转化率最大的
(3)在压强分别为
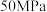 和
和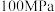 的条件下,在密闭容器中充入物质的量之比为
的条件下,在密闭容器中充入物质的量之比为 的
的 和
和 ,充分反应,平衡时
,充分反应,平衡时 和
和 的物质的量分数随温度的变化如图所示。
的物质的量分数随温度的变化如图所示。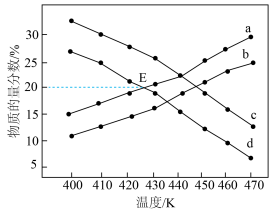
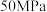 时
时 和
和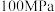 时
时 物质的量分数的是
物质的量分数的是②曲线d上对应的E点的

Ⅱ.电解法制丙烯
(4)在某中性电解质溶液中,以氯化物诱导的双向
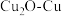 催化材料作电极,可将
催化材料作电极,可将 转化为丙烯,其原理如图所示:
转化为丙烯,其原理如图所示: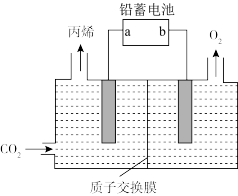
 极是
极是②生成丙烯的电极反应式为
 )被誉为“现代工业、国防与尖端技术维生素”。亚碲酸钠
)被誉为“现代工业、国防与尖端技术维生素”。亚碲酸钠 可用于有机合成和细菌学的研究,一种从阳极泥中提取亚碲酸钠的工艺流程如图。
可用于有机合成和细菌学的研究,一种从阳极泥中提取亚碲酸钠的工艺流程如图。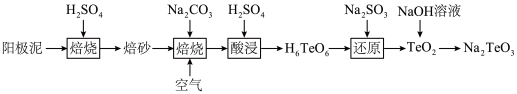
 中Te的化合价为
中Te的化合价为(2)在600K左右往阳极泥中加入一定浓度
 溶液“焙烧”时,单质Te转化为
溶液“焙烧”时,单质Te转化为 的化学方程式为
的化学方程式为(3)“焙砂”与碳酸钠充分混合,通入空气氧化物料,每生成1mol碲酸四氢钠
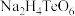 ,则需要的氧化剂
,则需要的氧化剂 至少为
至少为(4)“还原”过程中氧化剂与还原剂的物质的量之比为
 是否过量的实验操作方法为
是否过量的实验操作方法为(5)亚碲酸钠溶液在工业上常用作电解制备单质碲的电解质溶液,用惰性电极电解亚碲酸钠溶液和氢氧化钠溶液的混合液时,析出单质碲电极的电极反应式为
(6)常温下,往
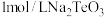 溶液中滴加盐酸,当溶液pH=5时,溶液中
溶液中滴加盐酸,当溶液pH=5时,溶液中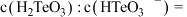
 的
的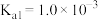 、
、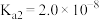 )
)
I.工业上用
 和
和 在一定条件下可以合成乙烯:
在一定条件下可以合成乙烯: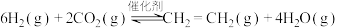

已知:①

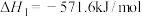
②

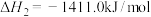
③

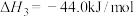
(1)

 、
、 、
、 表示)。
表示)。(2)恒温恒容下,向密闭容器按投料比
 通入原料气,能判断该反应处于平衡状态的是_______(填标号)。
通入原料气,能判断该反应处于平衡状态的是_______(填标号)。A. |
| B.混合气体的密度保持不变 |
| C.混合气体的平均相对分子质量保持不变 |
D.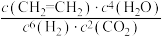 保持不变 保持不变 |
(3)向密闭容器按投料比
 通入原料气(,不同温度对
通入原料气(,不同温度对 的平衡转化率和催化剂催化效率的影响如图所示,则压强
的平衡转化率和催化剂催化效率的影响如图所示,则压强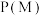
 ,原因是:
,原因是:
Ⅱ.
 催化加氢可以直接合成二甲醚。涉及以下主要反应:
催化加氢可以直接合成二甲醚。涉及以下主要反应:①
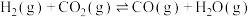

②


恒压条件下,
 、起始量相等时,
、起始量相等时, 的平衡转化率和的选择性随温度变化如下图所示。
的平衡转化率和的选择性随温度变化如下图所示。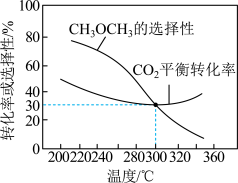
已知:的选择性
 %
%(4)300℃时,通入
 、
、 各
各 ,平衡时
,平衡时 的选择性、
的选择性、 的平衡转化率均为30%,则此温度下反应①的平衡常数
的平衡转化率均为30%,则此温度下反应①的平衡常数
(5)温度高于300℃,
 的平衡转化率随温度升高而增大的原因可能是
的平衡转化率随温度升高而增大的原因可能是Ⅲ.电化学法也可还原二氧化碳制乙烯,原理如下图所示。
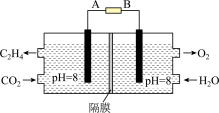
(6)该电池的阴极电极反应式为:
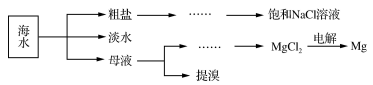
已知:Br2的沸点为59℃,微溶于水,有毒性和强腐蚀性。
(1)电解饱和 NaCl 溶液的化学方程式为
(2)下列方法不可用于海水淡化的是
A. 蒸馏法 B. 萃取法 C. 离子交换法 D. 电渗析法
(3)工业上用电解法制Mg 时,通常在MgCl2中加入适量 CaCl2,其原因是:①
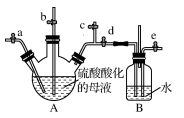
(4) 利用右图所示装置从母液中提取溴,在 B 瓶中得到较浓的溴水。实验方案为:关闭b、d,打开a、c,由a 向A中缓慢通入
 和
和 的流程如图所示:
的流程如图所示: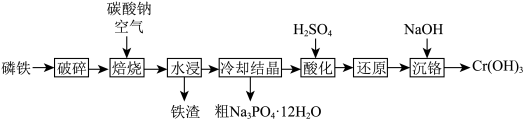
已知:水浸后溶液的主要成分为
 和
和 ;
; 的
的 回答下列问题:
回答下列问题:(1)“破碎”的目的为
(2)“焙烧”时,应将原料加到
(3)进一步提纯粗磷酸钠晶体的方法为
(4)“酸化”时发生反应的离子方程式为
(5)“沉铬”时,加NaOH调节至pH为
 ,离子浓度为10-5mol/L时可认为该离子沉淀完全)
,离子浓度为10-5mol/L时可认为该离子沉淀完全)
【推荐3】保险粉(Na2S2O4)是一种白色粉末,在空气中易被氧化,在强酸性环境中不稳定,遇水自身易发生氧化还原反应。可用作还原剂和漂白剂。
I.实验室制法
将甲酸钠(易溶于水,微溶于甲醇)、80%甲醇水溶液和NaOH溶液混合,再通入SO2气体,并维持体系弱酸性环境。
(1)补全反应的化学方程式:HCOONa+NaOH+SO2=_____+CO2+_____,
(2)实验中采用80%甲醇水溶液的目的是
(3)反应一段时间后,装置中有白色固体析出,将固体过滤、洗涤、干燥、收集。干燥保险粉的最佳方法
a.空气中蒸发干燥b.真空干燥c.氯化氢气流中蒸发干燥
II.工业制法
(4)用惰性电极电解NaHSO3溶液制备Na2S2O4,装置如图所示。写出a电极的电极反应式

III.制备过程中,产生COD值很高的废水的处理方法
资料:COD为化学需氧量,是表示水中还原性物质多少的一个指标。是指在一定的条件下,采用一定的强氧化剂处理水样时,所消耗的氧化剂量。在Fe2+催化下,H2O2分解为具有强氧化性的氢氧自由基(·OH),可利用其氧化性氧化水体中的还原性物质,以达到处理COD值很高的废水的目的。
(5)用化学用语表示产生氢氧自由基(·OH)的过程
(6)当Fe2+投入量超过一定值,会使得还原性物质的脱除率降低,COD无法达到预期指标。可能的原因是

已知:①
 为两性氧化物;②
为两性氧化物;② 易溶于过量的
易溶于过量的 溶液中;③
溶液中;③ 溶液在加热过程中会失水生成
溶液在加热过程中会失水生成 。
。回答下列问题:
(1)
 中砷元素的化合价为
中砷元素的化合价为(2)“焙烧”操作中,
 参与反应的化学方程式为
参与反应的化学方程式为(3)“碱浸”的目的是
(4)“氧化”操作的目的是
(5)“还原、加热”过程中制得
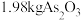 ,则消耗标准状况下气体X的体积为
,则消耗标准状况下气体X的体积为(6)砷酸钠(
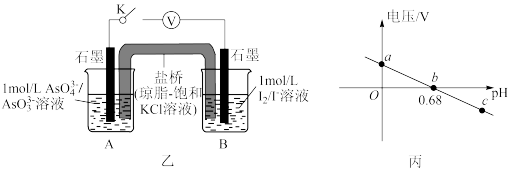
 )可用作可逆电池,装置如图乙所示,其反应原理为
)可用作可逆电池,装置如图乙所示,其反应原理为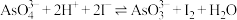 。为探究溶液
。为探究溶液 对
对 氧化性的影响,测得输出电压与溶液
氧化性的影响,测得输出电压与溶液 的变化关系如图丙所示。则a点时,盐桥中
的变化关系如图丙所示。则a点时,盐桥中
I.制备草酸亚铁晶体(装置如图所示):
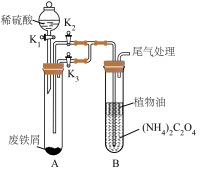
(1)盛放稀硫酸的仪器名称为
(2)实验过程中,制备草酸亚铁的具体操作是
(3)检验草酸亚铁晶体已洗净的操作方法为
II.草酸亚铁晶体热分解产物的探究:
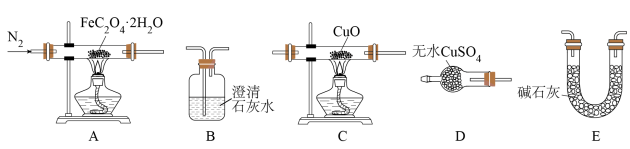
(4)按照气流从左到右的方向,上述装置的连接顺序为
(5)实验结束后,C中黑色固体变为红色,B中澄清石灰水变浑浊,D中无水硫酸铜变为蓝色,A中残留FeO,则A处反应管中发生反应的化学方程式为
III.运用热重分析法推测产物:
(6)称取54.0g草酸亚铁晶体(FeC2O4·2H2O)在隔绝空气的条件下加热,得到剩余固体质量随温度变化的曲线如图所示:
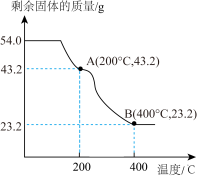
已知B点时,固体只含有一种铁的氧化物,根据上图可知B点固体物质的化学式为
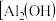
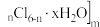 ,它是一种高效无机水处理剂,它的制备原理是调节增大
,它是一种高效无机水处理剂,它的制备原理是调节增大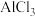 溶液的pH,通过促进其水解而结晶析出。其制备原料主要是铝加工行业的废渣--铝灰,它主要含
溶液的pH,通过促进其水解而结晶析出。其制备原料主要是铝加工行业的废渣--铝灰,它主要含 、Al,还有
、Al,还有 等杂质。聚合氯化铝生产的工艺流程如下:
等杂质。聚合氯化铝生产的工艺流程如下: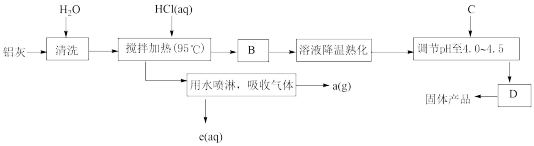
(1)搅拌加热操作过程中发生反应的离子方程式为:
(2)生产过程中B和D的操作名称分别是
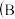 和D均为简单操作
和D均为简单操作 。
。(3)反应中副产品a是
(4)生产过程中可循环使用的物质是
 用化学式表示
用化学式表示 。
。(5)调节pH至
 的目的是
的目的是(6)实验室要测定水处理剂产品中n和x的值。为使测定结果更准确,需得到的晶体较纯净。生产过程C物质可选用下列物质中的
A.氢氧化钠
 铝
铝  氨水
氨水  氧化铝
氧化铝  偏铝酸钠
偏铝酸钠



