回答下列问题。
(1)图1所示的几种碳单质, 属于
属于________ 晶体,石墨中存在的作用力有________ 。金刚石和石墨中碳碳键键长较大的是________ ,理由:________ 。
钴酞菁分子中,钴离子的化合价为________ ,氮原子提供孤对电子与钴离子形成________ 键。 是共价分子,可以单体、二聚体和多聚体形式存在。其中单体和多聚体的结构简式分别如下:Cl—Be—Cl、
是共价分子,可以单体、二聚体和多聚体形式存在。其中单体和多聚体的结构简式分别如下:Cl—Be—Cl、
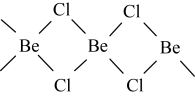
写出二聚体的结构简式________ ,并判断其中Be的杂化轨道类型________ 。
(4)一定条件下, 、K和
、K和 反应生成KCl和化合物X。已知X属于四方晶系,晶胞结构如图3所示(晶胞参数
反应生成KCl和化合物X。已知X属于四方晶系,晶胞结构如图3所示(晶胞参数 ,
, ),其中Cu化合价为+2。若阿伏加德罗常数的值为
),其中Cu化合价为+2。若阿伏加德罗常数的值为 ,化合物X的密度ρ=
,化合物X的密度ρ=________  。(用含
。(用含 的代数式表示,相对原子质量:F19 K39 Cu64)
的代数式表示,相对原子质量:F19 K39 Cu64)
(1)图1所示的几种碳单质,
 属于
属于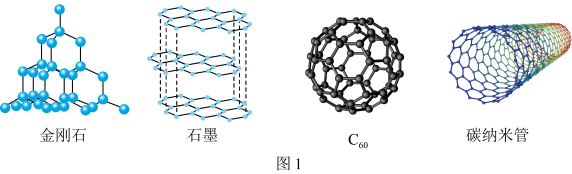
钴酞菁分子中,钴离子的化合价为

 是共价分子,可以单体、二聚体和多聚体形式存在。其中单体和多聚体的结构简式分别如下:Cl—Be—Cl、
是共价分子,可以单体、二聚体和多聚体形式存在。其中单体和多聚体的结构简式分别如下:Cl—Be—Cl、
写出二聚体的结构简式
(4)一定条件下,
 、K和
、K和 反应生成KCl和化合物X。已知X属于四方晶系,晶胞结构如图3所示(晶胞参数
反应生成KCl和化合物X。已知X属于四方晶系,晶胞结构如图3所示(晶胞参数 ,
, ),其中Cu化合价为+2。若阿伏加德罗常数的值为
),其中Cu化合价为+2。若阿伏加德罗常数的值为 ,化合物X的密度ρ=
,化合物X的密度ρ= 。(用含
。(用含 的代数式表示,相对原子质量:F19 K39 Cu64)
的代数式表示,相对原子质量:F19 K39 Cu64)
更新时间:2024-05-24 17:31:47
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】Ga、As、Al、C的相关化合物在化工和医学领域有着广泛的应用。回答下列问题:
(1)写出基态Ga原子的核外电子排布式:_________ ,有_____ 个未成对电子。
(2)合金砷化镓在现代工业中被广泛应用,Ga、As电负性由大到小排序为______________ 。
(3)1个丙二烯分子中σ键总数为___ 个,C原子的杂化方式为______ 。分子中的大π键可以用符号пmn表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为п66),则丙二烯中的大π键应表示为____________ 。
(4)氮化镓是第三代半导体材料,其晶体结构和单晶硅相似,晶胞结构如图所示:

①原子坐标参数是表示晶胞内部各原子的相对位置,其中原子坐标参数A为(0, 0, 0);B为(1/2,1/2,0);C为(1,0,1)。则D原子的坐标参数为_________________ 。
②已知氮化镓晶胞的边长为a nm,其密度为d g/cm3,则阿伏伽德罗常数NA =____ (用a、d表示)
(1)写出基态Ga原子的核外电子排布式:
(2)合金砷化镓在现代工业中被广泛应用,Ga、As电负性由大到小排序为
(3)1个丙二烯分子中σ键总数为
(4)氮化镓是第三代半导体材料,其晶体结构和单晶硅相似,晶胞结构如图所示:

①原子坐标参数是表示晶胞内部各原子的相对位置,其中原子坐标参数A为(0, 0, 0);B为(1/2,1/2,0);C为(1,0,1)。则D原子的坐标参数为
②已知氮化镓晶胞的边长为a nm,其密度为d g/cm3,则阿伏伽德罗常数NA =
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】血红蛋白是高等生物体内负责运载氧的一种蛋白质(缩写为HB或HGB)。与正常血红蛋白相比,硫血红蛋白不能与氧呈可逆的结合,因此失去携带氧的能力。下图所示为硫血红蛋白的结构。请回答下列问题:
(1)硫血红蛋白中所含非金属元素中电负性最大元素是___________ ,第一电离能最大的元素的原子是___________ 。
(2)根据等电子体原理推断氧元素的一种同素异形体O3是___________ 分子(填“极性”或“非极性”)。浓硫酸粘度较大的原因是___________ 。
(3)硫血红蛋白中C原子的杂化方式为___________ 。在图中用“→”标出N和Fe2+形成的配位键。___________

(4)铁的金属密堆积方式为体心立方结构,结构如图所示。
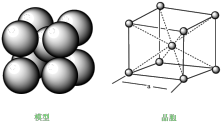

则晶胞中铁原子的配位数为___________ 。如果铁原子的半径为r pm,列式并计算出该堆积方式的空间利用率___________ 。
(1)硫血红蛋白中所含非金属元素中电负性最大元素是
(2)根据等电子体原理推断氧元素的一种同素异形体O3是
(3)硫血红蛋白中C原子的杂化方式为

(4)铁的金属密堆积方式为体心立方结构,结构如图所示。


则晶胞中铁原子的配位数为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】磷酸铁锂电池是以磷酸铁锂(LiFePO4)为正极材料的锂离子电池,具有循环寿命长、安全性能好、无环境污染等特点。
(1)磷酸铁锂具有橄榄石结构,空间骨架结构不易发生形变,化学性质稳定。
①基态 的价层电子排布式为
的价层电子排布式为_______ 。
②Li、P、O三种元素的电负性由大到小的顺序是_______ 。
(2)硫酸亚铁(FeSO4)可用于制备磷酸铁锂。
①根据价层电子对互斥理论可知, 的空间结构为
的空间结构为_______ 。
②比较S原子和O原子的第一电离能大小,并从原子结构的角度说明理由:_______ 。
(3)草酸亚铁(FeC2O4)也可用于制备磷酸铁锂。草酸根离子的结构简式为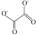 ,其中碳原子的杂化轨道类型为
,其中碳原子的杂化轨道类型为_______ 。
(4)磷酸铁(FePO4)与磷酸铁锂结构相似,其中 围绕
围绕 和
和 分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。充放电过程中,
分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。充放电过程中,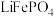 中的
中的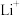 会不断脱嵌或嵌入链之间的孔道内,其结构变化如图所示。
会不断脱嵌或嵌入链之间的孔道内,其结构变化如图所示。
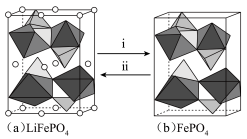
①i表示_______ (填“充电”或“放电”)过程。
②已知Li+的脱嵌率= 。某时刻,若正极材料中Li+的脱嵌率为
。某时刻,若正极材料中Li+的脱嵌率为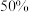 ,则其中
,则其中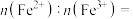
_______ 。
(1)磷酸铁锂具有橄榄石结构,空间骨架结构不易发生形变,化学性质稳定。
①基态
 的价层电子排布式为
的价层电子排布式为②Li、P、O三种元素的电负性由大到小的顺序是
(2)硫酸亚铁(FeSO4)可用于制备磷酸铁锂。
①根据价层电子对互斥理论可知,
 的空间结构为
的空间结构为②比较S原子和O原子的第一电离能大小,并从原子结构的角度说明理由:
(3)草酸亚铁(FeC2O4)也可用于制备磷酸铁锂。草酸根离子的结构简式为
 ,其中碳原子的杂化轨道类型为
,其中碳原子的杂化轨道类型为(4)磷酸铁(FePO4)与磷酸铁锂结构相似,其中
 围绕
围绕 和
和 分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。充放电过程中,
分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。充放电过程中,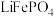 中的
中的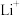 会不断脱嵌或嵌入链之间的孔道内,其结构变化如图所示。
会不断脱嵌或嵌入链之间的孔道内,其结构变化如图所示。
①i表示
②已知Li+的脱嵌率=
 。某时刻,若正极材料中Li+的脱嵌率为
。某时刻,若正极材料中Li+的脱嵌率为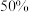 ,则其中
,则其中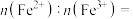
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】硼元素在1808年被发现,硼元素的化合物以硼酸和硼砂最为著名。
(1)写出基态硼原子的价电子排布式_______ ;指出 的空间结构
的空间结构_______ 。
(2)硼酸晶体具有层状结构,每一层的平面层状结构如图所示,判断硼酸晶体中,B原子的杂化类型_____________ ,平面层内所含有的作用力类型_____________ 。

(3)硼砂晶体在溶液中存在四硼酸根离子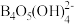 ,结构如图所示,可看成由
,结构如图所示,可看成由 和
和 缩合而成。在硼的总浓度
缩合而成。在硼的总浓度 的硼酸及其盐的水溶液中还存在类似结构的电荷为
的硼酸及其盐的水溶液中还存在类似结构的电荷为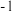 的五硼酸根离子以及电荷为
的五硼酸根离子以及电荷为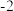 的三硼酸根离子,结构中硼原子均以
的三硼酸根离子,结构中硼原子均以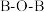 的方式连接成六元环,写出这两种硼酸根离子的化学式
的方式连接成六元环,写出这两种硼酸根离子的化学式______________ 、______________ 。

(4)“白石墨”具有类似石墨的层状结构,在 和
和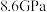 的压力下,“白石墨”可转化为具有闪锌矿型的立方晶体,晶胞结构如图所示。已知晶胞参数
的压力下,“白石墨”可转化为具有闪锌矿型的立方晶体,晶胞结构如图所示。已知晶胞参数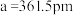 ,计算晶体中硼氮原子间的最短距离
,计算晶体中硼氮原子间的最短距离______________ ,列出密度的计算式______________ 。

(1)写出基态硼原子的价电子排布式
 的空间结构
的空间结构(2)硼酸晶体具有层状结构,每一层的平面层状结构如图所示,判断硼酸晶体中,B原子的杂化类型

(3)硼砂晶体在溶液中存在四硼酸根离子
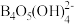 ,结构如图所示,可看成由
,结构如图所示,可看成由 和
和 缩合而成。在硼的总浓度
缩合而成。在硼的总浓度 的硼酸及其盐的水溶液中还存在类似结构的电荷为
的硼酸及其盐的水溶液中还存在类似结构的电荷为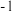 的五硼酸根离子以及电荷为
的五硼酸根离子以及电荷为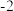 的三硼酸根离子,结构中硼原子均以
的三硼酸根离子,结构中硼原子均以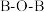 的方式连接成六元环,写出这两种硼酸根离子的化学式
的方式连接成六元环,写出这两种硼酸根离子的化学式
(4)“白石墨”具有类似石墨的层状结构,在
 和
和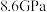 的压力下,“白石墨”可转化为具有闪锌矿型的立方晶体,晶胞结构如图所示。已知晶胞参数
的压力下,“白石墨”可转化为具有闪锌矿型的立方晶体,晶胞结构如图所示。已知晶胞参数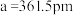 ,计算晶体中硼氮原子间的最短距离
,计算晶体中硼氮原子间的最短距离
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】硼和氮的单质及一些化合物在工农业生产等领域有重要应用。回答下列问题:
(1)N原子核外有_____ 种不同运动状态的电子。基态N原子中,能量最高的电子所占据的原子轨道的形状为_______ 。
(2)经测定发现,N2O5固体由NO2+ 和NO3-两种离子组成,该固体中N原子杂化类型为_______ ;与NO2+互为等电子体的微粒有_________ (写出一种)。
(3)HF和HI电离出H+较难的是____ (填化学式,下同)。铵盐大多不稳定,请预测NH4F、NH4I中,较易分解的是_____ 。
(4)第二周期中,第一电离能介于B元素和N元素间的元素为_______ (填“元素符号”)。
(5)晶体硼有多种变体,但其基本结构单元都是由硼原子组成的正二十面体( 见图I),每个顶点为一个硼原子,每个三角形均为等边三角形。则每一个此基本结构单元由____ 个硼原子构成;若该结构单元中有2 个原子为10B(其余为11B),那么该结构单元有_____ 种不同类型。
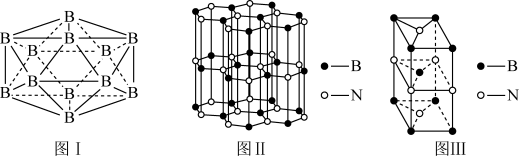
(6)硼和氮构成的一种氮化硼晶体的结构与石墨晶体结构相类似,B、N原子相互交替排列(见图II),其晶胞结构如图III所示。该晶胞有____ 个B和____ 个N。
(1)N原子核外有
(2)经测定发现,N2O5固体由NO2+ 和NO3-两种离子组成,该固体中N原子杂化类型为
(3)HF和HI电离出H+较难的是
(4)第二周期中,第一电离能介于B元素和N元素间的元素为
(5)晶体硼有多种变体,但其基本结构单元都是由硼原子组成的正二十面体( 见图I),每个顶点为一个硼原子,每个三角形均为等边三角形。则每一个此基本结构单元由

(6)硼和氮构成的一种氮化硼晶体的结构与石墨晶体结构相类似,B、N原子相互交替排列(见图II),其晶胞结构如图III所示。该晶胞有
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐3】人体必需的元素包括常量元素与微量元素,常量元素包括碳、氢、氧、氮、钙、镁等,微量元素包括铁、铜、锌、氟、碘等,这些元素形成的化合物种类繁多,应用广泛。
(1)锌、铜、铁、钙四种元素与少儿生长发育息息相关,请写出Fe2+的核外电子排布式___________ 。
(2)1个Cu2+与2个H2N—CH2—COO−形成含两个五元环结构的内配盐(化合物),其结构简式为___________ (用→标出配位键),在H2N—CH2—COO−中,属于第二周期的元素的第一电离能由大到小的顺序是___________ (用元素符号表示),N、C原子存在的相同杂化方式是___________ 杂化。
(3)碳酸盐中的阳离子不同,热分解温度就不同,查阅文献资料可知,离子半径r(Mg2+)=66 pm,r(Ca2+)=99 pm,r(Sr2+)=112 pm,r(Ba2+)=135 pm;碳酸盐分解温度T(MgCO3)=402℃,T(CaCO3)=825℃,T(SrCO3)=1172℃,T(BaCO3)=1360℃。分析数据得出的规律是___________ ,解释出现此规律的原因是___________ 。
(4)自然界的氟化钙矿物为萤石或氟石,CaF2的晶体结构呈立方体形,其结构如下:

①两个最近的F−之间的距离是___________ pm(用含m的代数式表示)。
②CaF2晶胞体积与8个F−形成的立方体的体积比为___________ 。
③CaF2晶胞的密度是___________ g·cm−3(化简至带根号的最简式,NA表示阿伏加 德罗常数的值)。
(1)锌、铜、铁、钙四种元素与少儿生长发育息息相关,请写出Fe2+的核外电子排布式
(2)1个Cu2+与2个H2N—CH2—COO−形成含两个五元环结构的内配盐(化合物),其结构简式为
(3)碳酸盐中的阳离子不同,热分解温度就不同,查阅文献资料可知,离子半径r(Mg2+)=66 pm,r(Ca2+)=99 pm,r(Sr2+)=112 pm,r(Ba2+)=135 pm;碳酸盐分解温度T(MgCO3)=402℃,T(CaCO3)=825℃,T(SrCO3)=1172℃,T(BaCO3)=1360℃。分析数据得出的规律是
(4)自然界的氟化钙矿物为萤石或氟石,CaF2的晶体结构呈立方体形,其结构如下:

①两个最近的F−之间的距离是
②CaF2晶胞体积与8个F−形成的立方体的体积比为
③CaF2晶胞的密度是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】水系镁离子电池的正极材料由铜、铁、氮、碳元素组成。回答下列问题:
(1)铜在元素周期表中的位置___________ ;与铜同周期的过渡金属中,若3d轨道上无未成对电子,其水合离子无色,钪(Sc)离子在水中以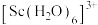 存在,推测
存在,推测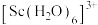
___________ (填“有”或“无”)颜色。
(2)火箭燃料三硝基胺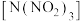 分子中所有原子共平面,中心N原子的价层电子对数为
分子中所有原子共平面,中心N原子的价层电子对数为___________ , 属于
属于___________ 分子(填“极性”或“非极性”)。
(3)陶瓷材料氮化硅中N、Si的成键方式为 ,键角N-Si-N
,键角N-Si-N_______ Si-N-Si(填“>”、“=”或“<”),理由是___________ 。
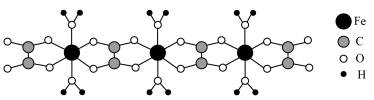
(4)草酸亚铁晶体常用作照相显影剂。下图为草酸亚铁晶体的单链结构, 的配位数为
的配位数为___________ ,两条链之间可以通过___________ 作用力连接。
(5)水系镁离子电池正极材料的化学式可表示为 ,其立方晶胞结构如图1,晶胞参数为a pm,俯视时
,其立方晶胞结构如图1,晶胞参数为a pm,俯视时 的位置如图2,晶胞中两个
的位置如图2,晶胞中两个 之间的距离为
之间的距离为___________ pm;电池放电过程中,电解液中的 会不断嵌入小立方体中心,晶胞中
会不断嵌入小立方体中心,晶胞中 和
和 含量发生变化,当电池放电完全时,形成
含量发生变化,当电池放电完全时,形成 ,x:x′=
,x:x′=___________ 。

(1)铜在元素周期表中的位置
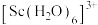 存在,推测
存在,推测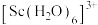
(2)火箭燃料三硝基胺
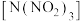 分子中所有原子共平面,中心N原子的价层电子对数为
分子中所有原子共平面,中心N原子的价层电子对数为 属于
属于(3)陶瓷材料氮化硅中N、Si的成键方式为
 ,键角N-Si-N
,键角N-Si-N(4)草酸亚铁晶体常用作照相显影剂。下图为草酸亚铁晶体的单链结构,
 的配位数为
的配位数为
(5)水系镁离子电池正极材料的化学式可表示为
 ,其立方晶胞结构如图1,晶胞参数为a pm,俯视时
,其立方晶胞结构如图1,晶胞参数为a pm,俯视时 的位置如图2,晶胞中两个
的位置如图2,晶胞中两个 之间的距离为
之间的距离为 会不断嵌入小立方体中心,晶胞中
会不断嵌入小立方体中心,晶胞中 和
和 含量发生变化,当电池放电完全时,形成
含量发生变化,当电池放电完全时,形成 ,x:x′=
,x:x′=
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】N元素形成的化合物丰富多彩,试回答下列问题:
(1)向硫酸铜溶液中逐滴加入氨水先产生沉淀,后沉淀溶解为深蓝色溶液,加入乙醇会析出蓝色晶体。
①基态铜原子的核外电子排布式为________________ ;
②1mol该蓝色晶体的阳离子中含有的σ键的数目为___________ ;
③简要解释为什么加入乙醇会有晶体析出_____________________________ ;
(2)已知邻羟基苯胺的结构式为 ,比较:邻羟基苯胺的沸点
,比较:邻羟基苯胺的沸点_____________ 对羟基苯胺的沸点(填“低于”, “高于”, “不确定”);毒奶粉事件中的主角是三聚氰胺,结构简式为 ,该分子中氮原子的杂化方式为
,该分子中氮原子的杂化方式为________________ ;复旦投毒案的主角是N一二甲基亚硝胺,结构简式为 ,则该分子所涉及的第二周期元素第一电离能由小到大的顺序为
,则该分子所涉及的第二周期元素第一电离能由小到大的顺序为____________________ ;
(3)已知CuN3中的阴离子与CO2互为等电子体,CuN3晶体的晶胞与氯化钠的晶胞类似。
①请写出CuN3中的阴离子的电子式__________________ ;
②已知该晶体晶胞边长a,b,c,关系为a=b___________ 个;
(4)已知NH3,NF3,N(CH3)3都可以与铜离子生成配离子。
①稳定性[Cu(NH3)4]2+__________ [Cu(NF3)4]2+。(填“低于”, “高于”,“不确定” )
②已知稳定性[Cu(NH3)4]2+高于[Cu[N(CH3)3]4]2+,请简要解释原因_______________________ 。
(1)向硫酸铜溶液中逐滴加入氨水先产生沉淀,后沉淀溶解为深蓝色溶液,加入乙醇会析出蓝色晶体。
①基态铜原子的核外电子排布式为
②1mol该蓝色晶体的阳离子中含有的σ键的数目为
③简要解释为什么加入乙醇会有晶体析出
(2)已知邻羟基苯胺的结构式为
 ,比较:邻羟基苯胺的沸点
,比较:邻羟基苯胺的沸点 ,该分子中氮原子的杂化方式为
,该分子中氮原子的杂化方式为 ,则该分子所涉及的第二周期元素第一电离能由小到大的顺序为
,则该分子所涉及的第二周期元素第一电离能由小到大的顺序为(3)已知CuN3中的阴离子与CO2互为等电子体,CuN3晶体的晶胞与氯化钠的晶胞类似。
①请写出CuN3中的阴离子的电子式
②已知该晶体晶胞边长a,b,c,关系为a=b
(4)已知NH3,NF3,N(CH3)3都可以与铜离子生成配离子。
①稳定性[Cu(NH3)4]2+
②已知稳定性[Cu(NH3)4]2+高于[Cu[N(CH3)3]4]2+,请简要解释原因
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】明朝《天工开物》中有世界上最早的“火法”炼锌技术的记载,锌是生命体必需的微量元素,被称为“生命之花”。(已知阿伏加德罗常数的值为NA)
(1)基态Zn原子核外的最高能层符号是_______ 。
(2)乳酸锌(如图)是一种很好的食品锌强化剂,其中存在的作用力有_______ (填编号)。

A.离子键 B.极性共价键 C.金属键 D.配位键 E.范德华力
(3)一水合甘氨酸锌是一种矿物类饲料添加剂,结构简式如图所示。其中所涉及的非金属元素的电负性由大到小的顺序是_______ ,Zn2+的配位数为_______ ;甘氨酸易溶于水,试从结构角度解释_______ 。

(4)Zn与S形成某种化合物的晶胞如图所示。

①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。例如图中原子1的坐标为(0,0,0),则原子2的坐标为_______ 。
②已知晶胞参数为a pm,阿伏加德罗常数为NA,求该晶胞的密度ρ=_______ g/cm3(写计算表达式)。
(1)基态Zn原子核外的最高能层符号是
(2)乳酸锌(如图)是一种很好的食品锌强化剂,其中存在的作用力有

A.离子键 B.极性共价键 C.金属键 D.配位键 E.范德华力
(3)一水合甘氨酸锌是一种矿物类饲料添加剂,结构简式如图所示。其中所涉及的非金属元素的电负性由大到小的顺序是

(4)Zn与S形成某种化合物的晶胞如图所示。

①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。例如图中原子1的坐标为(0,0,0),则原子2的坐标为
②已知晶胞参数为a pm,阿伏加德罗常数为NA,求该晶胞的密度ρ=
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】现有A、B、C、D、E五种元素,他们性质如下:
请回答如下问题:
(1)基态E原子有_____ 个未成对电子,二价E离子的核外电子排布式为_______ 。
(2)A2D分子中D原子的杂化类型是______ ,D的氧化物DO3分子空间构型为_______ 。
(3)CA3极易溶于水,其原因主要是_____ ,试判断CA3溶于水后,形成CA3· H2O的合理结构:____ (填字母代号), 推理依据是_____ 。

(4)在ESO4溶液中滴入过量氨水,形成配合物的颜色为______ ,反应的离子方程式为_____ 。
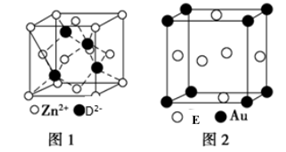
(5)ZnD的晶胞结构如图1所示,在ZnD晶胞中,D2-的配位数为______ 。
(6)E与金形成的金属互化物结构如图2所示,其晶胞边长为a nm,该金属互化物的密度为______ (用含a、NA的代数式表示)g· cm-3。
| A | 周期表中原子半径最小的元素 |
| B | 电负性最大的元素 |
| C | C的2p轨道中有三个未成对的单电子 |
| D | 原子核外电子数是B与C核外电子数之和 |
| E | E能形成红色(或砖红色)的E2O和黑色的EO两种氧化物 |
请回答如下问题:
(1)基态E原子有
(2)A2D分子中D原子的杂化类型是
(3)CA3极易溶于水,其原因主要是

(4)在ESO4溶液中滴入过量氨水,形成配合物的颜色为
(5)ZnD的晶胞结构如图1所示,在ZnD晶胞中,D2-的配位数为
(6)E与金形成的金属互化物结构如图2所示,其晶胞边长为a nm,该金属互化物的密度为

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】磷酸锌常用作氯化橡胶合成高分子材料的阻燃剂。工业上利用烧渣灰( 主要含ZnO,还含少量FeO、Al2O3、 CuO 及SiO2)为原料制取磷酸锌的工艺流程如图所示:
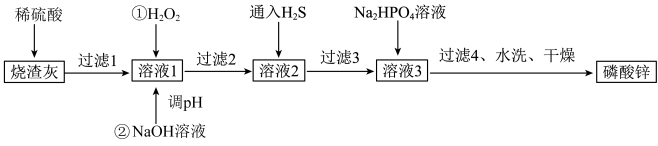
已知:①Zn3(PO4)2在水中几乎不溶,其在水中的溶解度随温度的升高而降低;
②“溶液1”中几种金属离子开始沉淀与沉淀完全的pH如表所示:
回答下列问题:
(1)基态锌原子的价电子排布式为_____________ 。
(2)加入H2O2的作用是___________________________ 。
(3)经过滤2得到滤渣的主要成分是Fe( OH)3和Al(OH)3,则用NaOH溶液调节pH的范围是___________ 。
(4)通入H2S的目的是除去Cu2+,写出该反应的离子方程式:_________________ 。
(5)洗涤磷酸锌沉淀时应选用________ (填“冷水”或“热水”),洗涤沉淀的操作是________________ 。
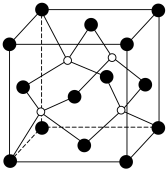
(6)图是碳化硅的晶胞结构,其晶体类型属于___________ 晶体。若碳化硅晶胞边长为a pm,阿伏加德罗常数的值为NA,则碳化硅晶体的密度为______________ g·cm-3 (列出计算式即可)。

已知:①Zn3(PO4)2在水中几乎不溶,其在水中的溶解度随温度的升高而降低;
②“溶液1”中几种金属离子开始沉淀与沉淀完全的pH如表所示:
| 金属离子 | Al3+ | Fe3+ | Cu2+ | Zn2+ |
| 开始沉淀的pH | 3.0 | 2.2 | 5.4. | 6.5 |
| 完全沉淀的pH | 5.0 | 3.6 | 6.7 | 8.5 |
(1)基态锌原子的价电子排布式为
(2)加入H2O2的作用是
(3)经过滤2得到滤渣的主要成分是Fe( OH)3和Al(OH)3,则用NaOH溶液调节pH的范围是
(4)通入H2S的目的是除去Cu2+,写出该反应的离子方程式:
(5)洗涤磷酸锌沉淀时应选用
(6)图是碳化硅的晶胞结构,其晶体类型属于

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】2018年11月《物理评论快报》报道了艾姆斯实验室制造的包含钙、钾、铁和砷以及少量镍的CaK(Fe1-xNix)4As4新型化合物材料,呈现出被称为刺猬自旋新磁态。有助于更好理解磁性 与非常规超导性之间的联系。回答下列问题:
(1)基态镍原子的价电子排布式为_______ ;上述材料中所含元素的基态原子中,未成对电子数最多的是_______ (填元素符号)。
(2)铁及其离子易形成配离子,如[Fe(CN)6]3-、[Fe(CN)x]4-、Fe(CO)5等。所包括的非金属元素中第一电离能最大的是______ (填元素符号);[Fe(CN)6] 4-中含有σ键与π键的数目比为_____________ 。
(3)K3AsO3可用于碘的微量分析。
①AsO33-的立体构型为_______ ,写出一种与其互为等电子体的分子_______ (填化学式)。
②K+的焰色反应呈紫色,金属元素能产生焰色实验的微观原因为_______ 。
(4)Ni与Ca处于同一周期,且核外最外层电子构型相同,但金属Ni的熔点和沸点均比金属Ca的高,其原因为_______ 。
(5)①金属镍的原子堆积方式如图所示,则金属镍晶胞俯视图为_______ 。

a. b.
b. c.
c. d.
d.
②某砷镍合金的晶胞如图所示,设阿伏加 德罗常数的值为NA,该晶体的密度ρ=_____ g·cm-3。

(1)基态镍原子的价电子排布式为
(2)铁及其离子易形成配离子,如[Fe(CN)6]3-、[Fe(CN)x]4-、Fe(CO)5等。所包括的非金属元素中第一电离能最大的是
(3)K3AsO3可用于碘的微量分析。
①AsO33-的立体构型为
②K+的焰色反应呈紫色,金属元素能产生焰色实验的微观原因为
(4)Ni与Ca处于同一周期,且核外最外层电子构型相同,但金属Ni的熔点和沸点均比金属Ca的高,其原因为
(5)①金属镍的原子堆积方式如图所示,则金属镍晶胞俯视图为

a.
 b.
b. c.
c. d.
d.
②某砷镍合金的晶胞如图所示,设阿伏加 德罗常数的值为NA,该晶体的密度ρ=

您最近一年使用:0次



