三氯化硼可用于有机反应催化剂、电子工业等,其熔点为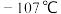 ,沸点为12.5℃,易水解。其制备及纯度测定实验如下:
,沸点为12.5℃,易水解。其制备及纯度测定实验如下:
Ⅰ.制备
将氯气通入装有mg 和木炭的管式反应炉,加热,开始充分反应,反应结束后在氮气的氛围中冷却至室温。
和木炭的管式反应炉,加热,开始充分反应,反应结束后在氮气的氛围中冷却至室温。
Ⅱ.纯度测定
已知:AgSCN是一种白色沉淀且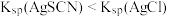 。
。
取反应后 的产品于水解瓶中完全水解,稀释至100.00mL。取10.00mL该溶液于锥形瓶中,加入
的产品于水解瓶中完全水解,稀释至100.00mL。取10.00mL该溶液于锥形瓶中,加入
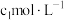
 溶液,再加入适量硝基苯,用力摇动,将沉淀表面完全覆盖(不考虑杂质的反应)。以
溶液,再加入适量硝基苯,用力摇动,将沉淀表面完全覆盖(不考虑杂质的反应)。以 溶液为指示剂,用
溶液为指示剂,用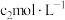 KSCN标准溶液滴定过量
KSCN标准溶液滴定过量 溶液,消耗标准溶液
溶液,消耗标准溶液 。
。
下列说法正确的是)
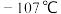 ,沸点为12.5℃,易水解。其制备及纯度测定实验如下:
,沸点为12.5℃,易水解。其制备及纯度测定实验如下:Ⅰ.制备
将氯气通入装有mg
 和木炭的管式反应炉,加热,开始充分反应,反应结束后在氮气的氛围中冷却至室温。
和木炭的管式反应炉,加热,开始充分反应,反应结束后在氮气的氛围中冷却至室温。Ⅱ.纯度测定
已知:AgSCN是一种白色沉淀且
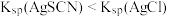 。
。取反应后
 的产品于水解瓶中完全水解,稀释至100.00mL。取10.00mL该溶液于锥形瓶中,加入
的产品于水解瓶中完全水解,稀释至100.00mL。取10.00mL该溶液于锥形瓶中,加入
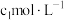
 溶液,再加入适量硝基苯,用力摇动,将沉淀表面完全覆盖(不考虑杂质的反应)。以
溶液,再加入适量硝基苯,用力摇动,将沉淀表面完全覆盖(不考虑杂质的反应)。以 溶液为指示剂,用
溶液为指示剂,用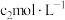 KSCN标准溶液滴定过量
KSCN标准溶液滴定过量 溶液,消耗标准溶液
溶液,消耗标准溶液 。
。下列说法正确的是)
| A.滴入最后半滴标准溶液,溶液由红色变为无色,且半分钟不褪色,说明达到滴定终点 |
B.实验所得产品的产率是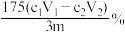 |
| C.若未加硝基苯,则测定结果将偏大 |
D.实验中用碱式滴定管盛放 水解液 水解液 |
更新时间:2024-05-24 15:24:47
|
相似题推荐
单选题
|
较难
(0.4)
解题方法
【推荐1】电位滴定法是根据滴定过程中指示电极电位的变化来确定滴定终点的一种滴定分析方法。在化学计量点附近,被测离子浓度发生突跃,指示电极电位(ERC)也产生了突跃,进而确定滴定终点的位置。苹果酸( ,用
,用 表示)是应用广泛的植物酸味剂,现利用电位滴定法向5.60mL苹果酸溶液滴加0.18mol/LNaOH溶液以测定苹果酸溶液的浓度,滴定曲线如图所示。下列说法正确的是
表示)是应用广泛的植物酸味剂,现利用电位滴定法向5.60mL苹果酸溶液滴加0.18mol/LNaOH溶液以测定苹果酸溶液的浓度,滴定曲线如图所示。下列说法正确的是

 ,用
,用 表示)是应用广泛的植物酸味剂,现利用电位滴定法向5.60mL苹果酸溶液滴加0.18mol/LNaOH溶液以测定苹果酸溶液的浓度,滴定曲线如图所示。下列说法正确的是
表示)是应用广泛的植物酸味剂,现利用电位滴定法向5.60mL苹果酸溶液滴加0.18mol/LNaOH溶液以测定苹果酸溶液的浓度,滴定曲线如图所示。下列说法正确的是
| A.该滴定过程可选用甲基橙作指示剂 |
B.a点存在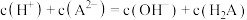 |
C.b点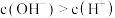 |
| D.若a、b两点横坐标分别为2.90、5.80,则苹果酸的浓度约为0.047mol/L |
您最近一年使用:0次
单选题
|
较难
(0.4)
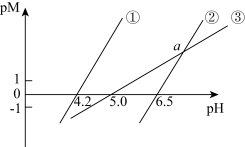
【推荐2】25℃时,用NaOH溶液分别滴定HX、 、
、 三种溶液,pM (p表示负对数,M表示
三种溶液,pM (p表示负对数,M表示 、
、 、
、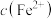 ),随pH变化关系如图所示,已知:
),随pH变化关系如图所示,已知: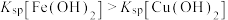 (不考虑二价铁的氧化)。下列说法错误的是
(不考虑二价铁的氧化)。下列说法错误的是
 、
、 三种溶液,pM (p表示负对数,M表示
三种溶液,pM (p表示负对数,M表示 、
、 、
、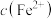 ),随pH变化关系如图所示,已知:
),随pH变化关系如图所示,已知: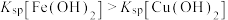 (不考虑二价铁的氧化)。下列说法错误的是
(不考虑二价铁的氧化)。下列说法错误的是 
A.②代表滴定 溶液的变化关系 溶液的变化关系 |
B.经计算, 固体难溶于HX溶液 固体难溶于HX溶液 |
C.调节溶液的pH=6.0时,可将工业废水中的 沉淀完全 沉淀完全 |
D.滴定HX溶液至a点时,溶液中 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】在镀锌铁皮的锌镀层厚度的测定过程中,下列操作会导致测定结果偏高的是
| A.过迟判断反应终点 |
| B.过早判断反应终点 |
| C.锌在酸中溶解后,铁皮未烘干就去称重 |
| D.在测定铁皮的面积时测得面积比铁皮的实际面积大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列表述中,说法正确的个数是( )
①pH=6的溶液一定是酸性溶液
②常温下某CH3COONa溶液的pH=8能证明CH3COOH是弱电解质
③CO2的水溶液导电能力很弱,所以CO2是弱电解质
④用未知浓度的盐酸滴定KOH标准溶液,若读数时,滴定前仰视,滴定到终点后俯视,会导致测定结果偏高
⑤25℃时,水溶液中水电离出的c(H+)和水电离出的c(OH-)的乘积一定等于10-14
⑥氯化铵溶液中含有杂质氯化铁,可以加入氨水调节pH至7~8,使Fe3+生成Fe(OH)3沉淀而出除去
⑦如果Na2Y的水溶液显中性,该溶液中一定没有电离平衡
⑧Mg与NH4Cl溶液反应生成H2以及为保存FeCl3溶液,要在溶液中加少量盐酸都与盐类水解有关
⑨某温度下,在难溶电解质AB2的饱和溶液中,c(A2+)=amol/L,c(B-)=bmol/L,则该温度下,AB2的Ksp为ab2
①pH=6的溶液一定是酸性溶液
②常温下某CH3COONa溶液的pH=8能证明CH3COOH是弱电解质
③CO2的水溶液导电能力很弱,所以CO2是弱电解质
④用未知浓度的盐酸滴定KOH标准溶液,若读数时,滴定前仰视,滴定到终点后俯视,会导致测定结果偏高
⑤25℃时,水溶液中水电离出的c(H+)和水电离出的c(OH-)的乘积一定等于10-14
⑥氯化铵溶液中含有杂质氯化铁,可以加入氨水调节pH至7~8,使Fe3+生成Fe(OH)3沉淀而出除去
⑦如果Na2Y的水溶液显中性,该溶液中一定没有电离平衡
⑧Mg与NH4Cl溶液反应生成H2以及为保存FeCl3溶液,要在溶液中加少量盐酸都与盐类水解有关
⑨某温度下,在难溶电解质AB2的饱和溶液中,c(A2+)=amol/L,c(B-)=bmol/L,则该温度下,AB2的Ksp为ab2
| A.3 | B.4 | C.5 | D.6 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】下列说法正确的是
| A.用盐酸标准溶液测定NaOH溶液浓度滴定实验中,滴定前无气泡而滴定后有气泡,会使测定值偏高 |
| B.将地下钢管与直流电源的正极相连,用来保护钢管 |
| C.已知在101KPa下,1gH2燃烧生成水蒸气放出121kJ热量,其热化学方程式为:2H2(g)+O2(g)=2H2O(g) △H=-484 kJ·mol-1 |
| D.25℃,101kPa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3kJ·mol-1,表示稀H2SO4与KOH 溶液反应的中和热的热化学方程式为:H2SO4(aq)+2KOH(aq)=K2SO4(aq)+2H2O(l)△H=-114.6kJ·mol-1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】已知NaHSO3溶液显酸性,表示0.1mol/LNaHSO3溶液中有关微粒浓度大小的关系式,正确的是( )
| A.c(Na+)>c(HSO3-)>c(SO32-)>c(H+)>c(OH-) |
| B.c(Na+)+c(H+)=c(HSO3-)+c(SO32-)+c(OH-) |
| C.c(Na+)>c(HSO3-)>c(SO32-)>c(H2SO3)>c(OH-) |
| D.c(Na+)=c(HSO3-)+c(SO32-)+c(H2SO3) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】经测定,某溶液中只含有 、Cl-、H+、OH-四种离子,下列说法中错误的是
、Cl-、H+、OH-四种离子,下列说法中错误的是
 、Cl-、H+、OH-四种离子,下列说法中错误的是
、Cl-、H+、OH-四种离子,下列说法中错误的是A.溶液中四种离子之间可能满足:c(Cl-)>c(H+)>c( )>c(OH-) )>c(OH-) |
B.若溶液中的溶质是NH4Cl 和NH3·H2O,则离子间可能满足:c( )>c(Cl-)>c(OH-)>c(H+) )>c(Cl-)>c(OH-)>c(H+) |
C.若溶液中四种离子满足:c(Cl-)>c( )>c(H+)>c(OH-),则溶液中的溶质一定只有NH4Cl )>c(H+)>c(OH-),则溶液中的溶质一定只有NH4Cl |
D.若溶液中c(Cl-)=c( ),则该溶液一定呈中性 ),则该溶液一定呈中性 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】用亚硫酸盐(X)吸收烟气中的SO2。已知吸收过程中含硫组分物质的量分数(δ)与溶液pH的变化关系如下图所示。下列说法中不正确 的是


| A.若X为Na2SO3,当吸收液pH=1.85时:c(Na+)=c(HSO3-)+c(H2SO3) |
| B.若X为Na2SO3,当吸收液呈中性时:2c(SO32-)+c(HSO3-)=c(Na+) |
| C.若X为 (NH4)2SO3,(NH4)2SO3溶液呈碱性,说明水解程度:SO32-> NH4+ |
| D.若X为 (NH4)2SO3,图中b点溶液中n(HSO3-)∶n(NH4+)= 1∶3 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】在含单质碘的KI溶液中存在可逆反应: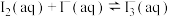 ,为测定该反应的平衡常数K进行如下实验,实验步骤如下:
,为测定该反应的平衡常数K进行如下实验,实验步骤如下:
①在装有 的KI溶液的碘量瓶中加入足量
的KI溶液的碘量瓶中加入足量 ,充分搅拌溶解,待过量的固体碘沉于瓶底后,取42.5mL上层清液,用
,充分搅拌溶解,待过量的固体碘沉于瓶底后,取42.5mL上层清液,用 萃取,充分振荡、静置、分液,得到42.5mL萃取后的水溶液、
萃取,充分振荡、静置、分液,得到42.5mL萃取后的水溶液、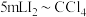 溶液。
溶液。
②取萃取后的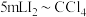 溶液于碘量瓶中,加水充分振荡,再加入质量分数为0.01%KI溶液,充分振荡后,静置5分钟,注入4mL0.2%的淀粉溶液,用
溶液于碘量瓶中,加水充分振荡,再加入质量分数为0.01%KI溶液,充分振荡后,静置5分钟,注入4mL0.2%的淀粉溶液,用 的
的 标准溶液滴定,平行滴定3次,平均消耗
标准溶液滴定,平行滴定3次,平均消耗 溶液。
溶液。
③将萃取后的水溶液42.5mL移入碘量瓶中,注入4mL0.2%的淀粉溶液,用 的
的 标准溶液滴定,平行滴定3次,平均消耗
标准溶液滴定,平行滴定3次,平均消耗 溶液。
溶液。
已知:(1)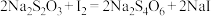 ;(2)
;(2) 与
与 难溶于
难溶于 ;(3)达到溶解平衡后,
;(3)达到溶解平衡后, 在
在 层和水层中的分配比
层和水层中的分配比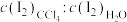 为
为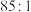

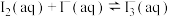 的平衡常数K计算正确的是
的平衡常数K计算正确的是
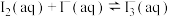 ,为测定该反应的平衡常数K进行如下实验,实验步骤如下:
,为测定该反应的平衡常数K进行如下实验,实验步骤如下:①在装有
 的KI溶液的碘量瓶中加入足量
的KI溶液的碘量瓶中加入足量 ,充分搅拌溶解,待过量的固体碘沉于瓶底后,取42.5mL上层清液,用
,充分搅拌溶解,待过量的固体碘沉于瓶底后,取42.5mL上层清液,用 萃取,充分振荡、静置、分液,得到42.5mL萃取后的水溶液、
萃取,充分振荡、静置、分液,得到42.5mL萃取后的水溶液、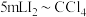 溶液。
溶液。②取萃取后的
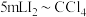 溶液于碘量瓶中,加水充分振荡,再加入质量分数为0.01%KI溶液,充分振荡后,静置5分钟,注入4mL0.2%的淀粉溶液,用
溶液于碘量瓶中,加水充分振荡,再加入质量分数为0.01%KI溶液,充分振荡后,静置5分钟,注入4mL0.2%的淀粉溶液,用 的
的 标准溶液滴定,平行滴定3次,平均消耗
标准溶液滴定,平行滴定3次,平均消耗 溶液。
溶液。③将萃取后的水溶液42.5mL移入碘量瓶中,注入4mL0.2%的淀粉溶液,用
 的
的 标准溶液滴定,平行滴定3次,平均消耗
标准溶液滴定,平行滴定3次,平均消耗 溶液。
溶液。已知:(1)
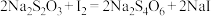 ;(2)
;(2) 与
与 难溶于
难溶于 ;(3)达到溶解平衡后,
;(3)达到溶解平衡后, 在
在 层和水层中的分配比
层和水层中的分配比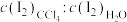 为
为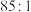

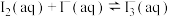 的平衡常数K计算正确的是
的平衡常数K计算正确的是A.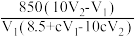 | B.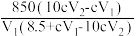 |
C. | D.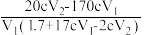 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】下列实验能达到实验目的的是
| A | B | C | D |
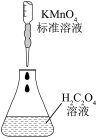 |  | 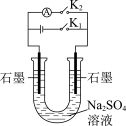 | 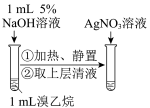 |
| 测定H2C2O4溶液的浓度 | 证明苯环使羟基活化 | 制作简单的燃料电池 | 检验溴乙烷的水解产物 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】硼氢化钠为白色粉末,是有机合成中常用的还原剂,在潮湿空气中分解。偏硼酸钠( )易溶于水,不溶于乙醇,易水解,但在碱性条件下可稳定存在。用硼精矿(含有一定量
)易溶于水,不溶于乙醇,易水解,但在碱性条件下可稳定存在。用硼精矿(含有一定量 ,及
,及 、
、 、
、 等杂质)制取
等杂质)制取 的流程和分析
的流程和分析 样品纯度(杂质不参加反应)的步骤如下。
样品纯度(杂质不参加反应)的步骤如下。 样品配成
样品配成 溶液,取
溶液,取 置于碘量瓶中,加入
置于碘量瓶中,加入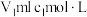 的
的 溶液,发生反应:
溶液,发生反应: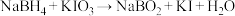 (化学方程式未配平)。
(化学方程式未配平)。
步骤Ⅱ:向步骤Ⅰ反应后的溶液中加入过量的 溶液,调节
溶液,调节 ,使
,使 转化为
转化为 ,冷却后于暗处放置数分钟。
,冷却后于暗处放置数分钟。
步骤Ⅲ:将步骤Ⅱ所得混合液的 调为弱酸性,加入几滴淀粉溶液,用
调为弱酸性,加入几滴淀粉溶液,用 标准溶液滴定至终点,发生反应:
标准溶液滴定至终点,发生反应: ,消耗
,消耗 标准溶液
标准溶液 。
。
下列关于该实验的相关操作正确的是
 )易溶于水,不溶于乙醇,易水解,但在碱性条件下可稳定存在。用硼精矿(含有一定量
)易溶于水,不溶于乙醇,易水解,但在碱性条件下可稳定存在。用硼精矿(含有一定量 ,及
,及 、
、 、
、 等杂质)制取
等杂质)制取 的流程和分析
的流程和分析 样品纯度(杂质不参加反应)的步骤如下。
样品纯度(杂质不参加反应)的步骤如下。
 样品配成
样品配成 溶液,取
溶液,取 置于碘量瓶中,加入
置于碘量瓶中,加入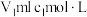 的
的 溶液,发生反应:
溶液,发生反应: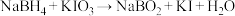 (化学方程式未配平)。
(化学方程式未配平)。步骤Ⅱ:向步骤Ⅰ反应后的溶液中加入过量的
 溶液,调节
溶液,调节 ,使
,使 转化为
转化为 ,冷却后于暗处放置数分钟。
,冷却后于暗处放置数分钟。步骤Ⅲ:将步骤Ⅱ所得混合液的
 调为弱酸性,加入几滴淀粉溶液,用
调为弱酸性,加入几滴淀粉溶液,用 标准溶液滴定至终点,发生反应:
标准溶液滴定至终点,发生反应: ,消耗
,消耗 标准溶液
标准溶液 。
。下列关于该实验的相关操作正确的是
| A.“步骤Ⅱ”中调节pH的试剂可以是适量KOH溶液 |
| B.“步骤Ⅲ”的操作过程中不慎将混和液调至强酸性会导致测得的样品纯度偏大 |
C.滴入最后半滴 标准溶液,溶液蓝色退去,则到达滴定终点 标准溶液,溶液蓝色退去,则到达滴定终点 |
| D.读数时,滴定前平视,滴定后俯视会导致测得的样品纯度偏大 |
您最近一年使用:0次

 时,向
时,向 溶液中滴入等浓度的
溶液中滴入等浓度的 溶液,混合溶液的
溶液,混合溶液的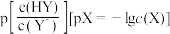 的关系如图所示。下列叙述错误的是
的关系如图所示。下列叙述错误的是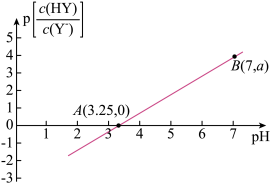
 的电离常数
的电离常数




