根据实验目的设计方案并进行实验,观察到相关现象,其中方案设计或结论不正确 的是
| 实验目的 | 方案设计 | 现象 | 结论 | |
| A | 探究Fe和S反应特点 | 将适量硫粉和铁粉混合堆成条状。用灼热的玻璃棒触及一端,当混合物呈红热状态时,移开玻璃棒。 | 混合物继续保持红热并持续扩散,粉末呈黑色 | 该反应为放热反应 |
| B | 比较沉淀的Ksp大小 | 向相同浓度和体积的浓氨水中,分别加入等量AgCl和AgI固体,充分搅拌 | 氯化银溶解,碘化银无变化 | Ksp:AgCl>AgI |
| C | 判断平衡移动的方向 | 将装有NO2气体的注射器的活塞缓慢向外拉 | 红棕色逐渐变浅 | 可逆反应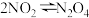 平衡正向移动 平衡正向移动 |
| D | 检验Na2S2O3样品是否含有Na2SO4杂质 | 取少量样品溶于水,先加入过量稀盐酸,过滤,向滤液中滴加少量BaCl2溶液 | 滤液中出现浑浊 | 该样品中含有Na2SO4杂质 |
| A.A | B.B | C.C | D.D |
更新时间:2024-05-24 16:21:57
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】根据如图所示的能量转化关系判断下列说法不正确的是


| A.该反应是放热反应 |
B.1mol  生成物的能量是510kJ 生成物的能量是510kJ |
C.反应中若生成1mol  , , 会发生改变 会发生改变 |
D.反应的热化学方程式是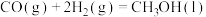 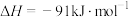 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】汽车受到猛烈碰撞时,安全气囊内的 固体迅速分解,产生氮气和金属钠,该过程中的能量变化如下图所示。下列说法错误的是
固体迅速分解,产生氮气和金属钠,该过程中的能量变化如下图所示。下列说法错误的是
 固体迅速分解,产生氮气和金属钠,该过程中的能量变化如下图所示。下列说法错误的是
固体迅速分解,产生氮气和金属钠,该过程中的能量变化如下图所示。下列说法错误的是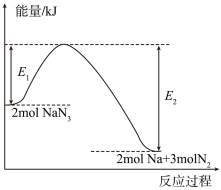
A. 属于离子化合物 属于离子化合物 |
B. 的分解反应属于放热反应 的分解反应属于放热反应 |
C. 表示2mol 表示2mol 固体的能量 固体的能量 |
D. 作为安全气囊的气体发生剂,具有产气快、产气量大等优点 作为安全气囊的气体发生剂,具有产气快、产气量大等优点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】化学反应进行的方向和限度是化学反应原理所要研究的两个重要问题,下列有关化学反应进行的方向和限度的说法中正确的是
A.反应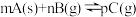 ,达到平衡时增加A的物质的量,平衡不移动,是因为A是固体,而分子间的碰撞只能在固体表面进行,固体的物质的量浓度对平衡没有影响 ,达到平衡时增加A的物质的量,平衡不移动,是因为A是固体,而分子间的碰撞只能在固体表面进行,固体的物质的量浓度对平衡没有影响 |
B.将一定量纯净的氨基甲酸铵置于密闭真空恒容容器中,在恒定温度下使其分解达到平衡: , , 的体积分数不变可以作为平衡判断的依据 的体积分数不变可以作为平衡判断的依据 |
C.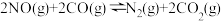 在常温下能自发进行,则该反应的 在常温下能自发进行,则该反应的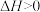 |
D.对于反应 ,起始充入等物质的量的A和B,达到平衡时A的体积分数为 ,起始充入等物质的量的A和B,达到平衡时A的体积分数为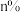 ,此时若给体系加压则A的体积分数一定会发生改变 ,此时若给体系加压则A的体积分数一定会发生改变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】对于反应:A(g)+B(g) 2C(g)+ D(s) △H<0,下列措施会使该反应的平衡正向移动的是
2C(g)+ D(s) △H<0,下列措施会使该反应的平衡正向移动的是
 2C(g)+ D(s) △H<0,下列措施会使该反应的平衡正向移动的是
2C(g)+ D(s) △H<0,下列措施会使该反应的平衡正向移动的是| A.升高温度 | B.分离出C |
| C.加入合适的催化剂 | D.恒压充入不参与反应的稀有气体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】1807年化学家戴维电解熔融氢氧化钠制得钠:4NaOH(熔融) O2↑+4Na+2H2O;后来盖·吕萨克用铁与熔融氢氧化钠作用也制得钠:3Fe(s)+4NaOH(l)⇌Fe3O4(s)+2H2(g)+4Na(g)。下列有关说法正确的是
O2↑+4Na+2H2O;后来盖·吕萨克用铁与熔融氢氧化钠作用也制得钠:3Fe(s)+4NaOH(l)⇌Fe3O4(s)+2H2(g)+4Na(g)。下列有关说法正确的是
 O2↑+4Na+2H2O;后来盖·吕萨克用铁与熔融氢氧化钠作用也制得钠:3Fe(s)+4NaOH(l)⇌Fe3O4(s)+2H2(g)+4Na(g)。下列有关说法正确的是
O2↑+4Na+2H2O;后来盖·吕萨克用铁与熔融氢氧化钠作用也制得钠:3Fe(s)+4NaOH(l)⇌Fe3O4(s)+2H2(g)+4Na(g)。下列有关说法正确的是| A.戴维法制钠,阳极的电极反应式为:Na++e-=Na |
| B.盖·吕萨克法制钠原理是利用铁的金属性比钠的强 |
| C.若用戴维法与盖·吕萨克法制得等量的钠,两方法转移电子总数相等 |
| D.盖·吕萨克法制钠原理是减小生成物浓度促进平衡正向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
A.碳酸氢钠溶液因 水解程度强于电离程度而显酸性: 水解程度强于电离程度而显酸性: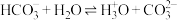 |
B.向含有硝酸银的氯化银悬浊液中加入适量 溶液,证明 溶液,证明 比 比 更难溶: 更难溶: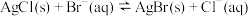 |
C.用 制备 制备 的反应原理为 的反应原理为 水解: 水解: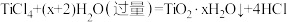 |
D.向偏铝酸钠溶液中加入适量小苏打, 和 和 两者都发生水解并相互促进: 两者都发生水解并相互促进: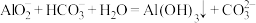 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列叙述不正确的是( )
| A.95℃纯水的pH<7,说明加热可导致水呈酸性 |
B.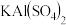 可作净水剂 可作净水剂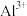 水解生成的 水解生成的 胶体具有吸附性 胶体具有吸附性 |
C.配制 溶液时加入少量NaOH,是因为 溶液时加入少量NaOH,是因为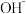 抑制 抑制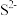 的水解 的水解 |
D.银能置换出HI(aq)中的氢,Ag与HI反应生成Ksp很小的AgI沉淀,利于 生成 生成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列实验操作的现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将某钾盐溶于硝酸溶液,再滴加1~2滴品红 | 品红不褪色 | 该钾盐不含 或 或 |
| B | 向两份蛋白质溶液中分别滴加饱和NaCl溶液和CuSO4溶液 | 均有固体析出 | 蛋白质均发生变性 |
| C | 将金属钠在燃烧匙中点燃,迅速伸入集满CO2的集气瓶 | 集气瓶中产生大量白烟,同时有黑色颗粒产生 | 钠可以置换出碳 |
| D | 向FeCl2溶液中滴加几滴K3[Fe(CN)6]溶液 | 溶液变成蓝色 | K3[Fe(CN)6]溶液可用于鉴别Fe2+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】由下列实验操作及现象不能得出相应结论的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将盛有相同浓度的CuCl2溶液的两支试管分别置于冷水和热水中 | 冷水中溶液呈蓝色,热水中则为黄色 | Cu2+在不同温度下颜色不同 |
| B | 向填充有经硫酸处理的K2Cr2O7的导管中吹入乙醇蒸气 | 固体由橙色变为绿色 | 乙醇具有还原性 |
| C | 向盛有FeCl2溶液的试管中加入酸化后的H2O2溶液 | 溶液变为棕黄色且出现无色气泡 | 生成了Fe3+,同时Fe3+催化分解H2O2 |
| D | 用玻璃棒蘸取Na2O2与足量水反应后得到的溶液,点在pH试纸上 | pH试纸呈蓝色 | 反应生成了碱 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列实验操作和现象正确,且所得到的结论也正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将 的NaHCO3溶液和等浓度的 CaCl2溶液混合 的NaHCO3溶液和等浓度的 CaCl2溶液混合 | 有沉淀生成 | 沉淀为碳酸氢钙 |
| B | 向5mL某无色溶液中滴加2滴酚酞溶液后呈橘红色溶液,再加5mL水混合均匀,加水后变为无色 | 加酚酞溶液后呈橘红色,加水后变为无色 | 原无色溶液可能为强酸性 |
| C | 将溴乙烷和 NaOH的乙醇溶液混合加热,产生气体通入酸性 KMnO4溶液 | 酸性KMnO4溶液褪色 | 产生了乙烯 |
| D | 向滴有酚酞的Na2CO3溶液中,逐滴加入BaCl2溶液 | 溶液红色逐渐褪去 | BaCl2溶液呈酸性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次


 溶液分别与相同浓度相同体积的
溶液分别与相同浓度相同体积的 溶液反应,观察现象
溶液反应,观察现象 溶液和
溶液和 溶液的
溶液的 ,比较溶液
,比较溶液 与
与 的酸性强弱
的酸性强弱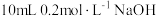 溶液中滴加2滴
溶液中滴加2滴 溶液,产生白色沉淀,再滴加2滴
溶液,产生白色沉淀,再滴加2滴 溶液,又生成红褐色沉淀
溶液,又生成红褐色沉淀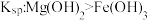
 溶液中,滴入几滴
溶液中,滴入几滴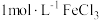 溶液,然后滴加几滴
溶液,然后滴加几滴 溶液
溶液 与
与 的反应是可逆反应
的反应是可逆反应

