在元素周期表前四周期中原子序数依次增大的六种元素A、B、C、D、E、F中,A与其余五种元素既不同周期也不同主族,B的一种核素在考古时常用来鉴定一些文物的年代,C的氧化物是导致酸雨的主要物质之一,D原子核外电子有8种不同的运动状态,E的基态原子在前四周期元素的基态原子中单电子数最多,F元素的基态原子最外能层只有一个电子,其它能层均已充满电子。
(1)写出基态E原子的价电子排布式_____ 。
(2)B、C、D三元素第一电离能由小到大的顺序为(用元素符号表 示)_____ ;A与C形成CA3型分子,分子中C原子的杂化类型为_______ ,分子的立体结构为 _______ ;C的单质与 BD化合物是等电子体,据等电子体的原理,写出BD化合物的电子式________ ; A2D由液态形成晶体时密度______ (填增大,不变或减小),分析主要原因(用文字叙述) ____________________________________________________ 。
(3)已知D、F能形成一种化合物,其晶胞的结构如图所示,则该化合物的化学式为(用元素符号表示)______ ;若相邻D原子和F原子间的距离为a cm,阿伏加德罗常数为NA,则该晶体的密度为_____ g/cm3(用含a、NA的符号表示)。
(1)写出基态E原子的价电子排布式
(2)B、C、D三元素第一电离能由小到大的顺序为(用元素符号表 示)
(3)已知D、F能形成一种化合物,其晶胞的结构如图所示,则该化合物的化学式为(用元素符号表示)
更新时间:2016-12-09 11:04:23
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】回答下列问题:
(1)金属元素铁能形成多种配合物,如:[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(III)]和Fe(CO)x等。
①基态氧原子的价电子排布式为___________ 。
②尿素(H2NCONH2)分子中C、N原子的杂化方式分别是___________ 、___________ 。
③配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=_____ 。Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于________ (填晶体类型)。
(2)O和Na形成的一种只含有离子键的离子化合物的晶胞结构如图,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为___________ 。已知该晶胞的密度为 g/cm3,阿伏加德罗常数为NA,求晶胞边长a=
g/cm3,阿伏加德罗常数为NA,求晶胞边长a=___________ cm。(用含p、NA的计算式表示)___________ 。
a.第一电离能大小:S>P>Si
b.电负性顺序:C<N<O<F
c.因为晶格能CaO比KC1高,所以KCl比CaO熔点低
d.SO2与CO2的化学性质类似,分子结构也都呈直线形,相同条件下SO2的溶解度更大
(1)金属元素铁能形成多种配合物,如:[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(III)]和Fe(CO)x等。
①基态氧原子的价电子排布式为
②尿素(H2NCONH2)分子中C、N原子的杂化方式分别是
③配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=
(2)O和Na形成的一种只含有离子键的离子化合物的晶胞结构如图,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为
 g/cm3,阿伏加德罗常数为NA,求晶胞边长a=
g/cm3,阿伏加德罗常数为NA,求晶胞边长a=
a.第一电离能大小:S>P>Si
b.电负性顺序:C<N<O<F
c.因为晶格能CaO比KC1高,所以KCl比CaO熔点低
d.SO2与CO2的化学性质类似,分子结构也都呈直线形,相同条件下SO2的溶解度更大
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐2】人体必需的元素包括常量元素与微量元素,常量元素包括碳、氢、氧、氮、钙、镁等,微量元素包括铁、铜、锌、氟、碘等,这些元素形成的化合物种类繁多,应用广泛。
(1)锌、铜、铁、钙四种元素与少儿生长发育息息相关,请写出Fe2+的核外电子排布式___________ 。
(2)1个Cu2+与2个H2N—CH2—COO−形成含两个五元环结构的内配盐(化合物),其结构简式为___________ (用→标出配位键),在H2N—CH2—COO−中,属于第二周期的元素的第一电离能由大到小的顺序是___________ (用元素符号表示),N、C原子存在的相同杂化方式是___________ 杂化。
(3)碳酸盐中的阳离子不同,热分解温度就不同,查阅文献资料可知,离子半径r(Mg2+)=66 pm,r(Ca2+)=99 pm,r(Sr2+)=112 pm,r(Ba2+)=135 pm;碳酸盐分解温度T(MgCO3)=402℃,T(CaCO3)=825℃,T(SrCO3)=1172℃,T(BaCO3)=1360℃。分析数据得出的规律是___________ ,解释出现此规律的原因是___________ 。
(4)自然界的氟化钙矿物为萤石或氟石,CaF2的晶体结构呈立方体形,其结构如下:

①两个最近的F−之间的距离是___________ pm(用含m的代数式表示)。
②CaF2晶胞体积与8个F−形成的立方体的体积比为___________ 。
③CaF2晶胞的密度是___________ g·cm−3(化简至带根号的最简式,NA表示阿伏加 德罗常数的值)。
(1)锌、铜、铁、钙四种元素与少儿生长发育息息相关,请写出Fe2+的核外电子排布式
(2)1个Cu2+与2个H2N—CH2—COO−形成含两个五元环结构的内配盐(化合物),其结构简式为
(3)碳酸盐中的阳离子不同,热分解温度就不同,查阅文献资料可知,离子半径r(Mg2+)=66 pm,r(Ca2+)=99 pm,r(Sr2+)=112 pm,r(Ba2+)=135 pm;碳酸盐分解温度T(MgCO3)=402℃,T(CaCO3)=825℃,T(SrCO3)=1172℃,T(BaCO3)=1360℃。分析数据得出的规律是
(4)自然界的氟化钙矿物为萤石或氟石,CaF2的晶体结构呈立方体形,其结构如下:

①两个最近的F−之间的距离是
②CaF2晶胞体积与8个F−形成的立方体的体积比为
③CaF2晶胞的密度是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】第ⅢA、ⅤA族元素组成的化合物AlN、AlP、AlAs等是人工合成的半导体材料,它们的晶体结构与单晶硅相似,与NaCl的晶体类型不同。
(1)核电荷数比As小4的原子基态的电子排布式为_________________________ 。
(2)前四周期元素中,基态原子中未成对电子与其所在周期数相同的元素有______ 种。
(3)NCl3中心原子杂化方式为________________ ,NCl3的空间构型为__________ 。
(4)在AlN晶体中,每个Al原子与________ 个N原子相连,AlN属于________ 晶体。
(5)设NaCl的摩尔质量为Mr g·mol-1,食盐晶体的密度为ρ g·cm-3,阿伏加德罗常数的值为NA。食盐晶体中两个距离最近的钠离子中心间的距离为________ cm。
(1)核电荷数比As小4的原子基态的电子排布式为
(2)前四周期元素中,基态原子中未成对电子与其所在周期数相同的元素有
(3)NCl3中心原子杂化方式为
(4)在AlN晶体中,每个Al原子与
(5)设NaCl的摩尔质量为Mr g·mol-1,食盐晶体的密度为ρ g·cm-3,阿伏加德罗常数的值为NA。食盐晶体中两个距离最近的钠离子中心间的距离为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐1】镍是一种银白色金属,具有良好的机械强度和延展性,常用来制造货币等,镀在其他金属上可以防止生锈。回答下列问题:
(1)基态镍原子核外未成对的电子数为_______ 个。
(2)镍不溶于水,在稀酸中可缓慢溶解,生成Ni2+。用丁二酮肟(dmg)鉴定Ni2+的存在时生成鲜红色的沉淀,其反应的离子方程式为Ni2++2dmg-Ni(dmg)2↓+2H+。已知:丁二酮肟的结构式为 ;Ni(dmg)2的结构如图所示。
;Ni(dmg)2的结构如图所示。
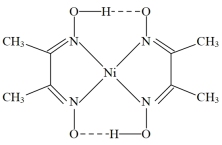
①Ni(dmg)2中所含的作用力有_______ (填字母序号)。
A.极性键 B.非极性键 C.离子键 D.配位键 E.氢键
②Ni(dmg)2中所含元素电负性由大到小的顺序是_______ ,N原子的杂化方式为_______ 。
③Ni(dmg)2中Ni与N成键,而非和O成键的原因可能是_______ 。
④Ni(dmg)2在水中的溶解度比较小的原因是_______ 。
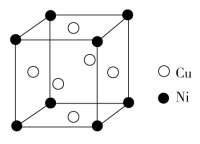
(3)铜镍合金主要用于造币,亦可用于制作仿银饰品。其立方晶胞结构如图所示,则该晶体的化学式为_______ ,铜原子构成的空间构型为_______ ,铜原子距离最近的Ni有_______ 个;已知该晶体的密度为ρg·cm-3,则晶胞中距离最近的Ni原子和Cu原子的核间距为 _______ pm(用NA表示阿伏加德罗常数的值,列出计算式即可)。
(1)基态镍原子核外未成对的电子数为
(2)镍不溶于水,在稀酸中可缓慢溶解,生成Ni2+。用丁二酮肟(dmg)鉴定Ni2+的存在时生成鲜红色的沉淀,其反应的离子方程式为Ni2++2dmg-Ni(dmg)2↓+2H+。已知:丁二酮肟的结构式为
 ;Ni(dmg)2的结构如图所示。
;Ni(dmg)2的结构如图所示。
①Ni(dmg)2中所含的作用力有
A.极性键 B.非极性键 C.离子键 D.配位键 E.氢键
②Ni(dmg)2中所含元素电负性由大到小的顺序是
③Ni(dmg)2中Ni与N成键,而非和O成键的原因可能是
④Ni(dmg)2在水中的溶解度比较小的原因是
(3)铜镍合金主要用于造币,亦可用于制作仿银饰品。其立方晶胞结构如图所示,则该晶体的化学式为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐2】第四周期元素由于受3d电子的影响,性质的递变规律与短周期元素略有不同。
(1)镓的基态原子电子排布式是_______ 。
(2)已知钛和铝的相对原子半径分别是1.45和1.43,钛的硬度比铝大的原因是_______ 。
(3)多酚氧化酶与植物的抗病性有关。配合物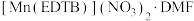 是多酚氧化酶的模型配合物。
是多酚氧化酶的模型配合物。
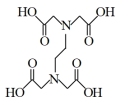 (EDTA)+
(EDTA)+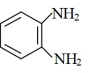 (邻苯二氨)
(邻苯二氨)
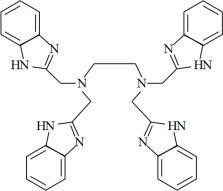 (EDTB)
(EDTB)
①EDTA中N的杂化轨道类型为_______ 。
②邻苯二胺分子中 键的数目为
键的数目为_______ 。
③EDTB分子中所含元素的电负性由小到大的顺序为_______ 。
④与 互为等电子体的一种阴离子为
互为等电子体的一种阴离子为_______ 。
⑤配离子 中的配位原子是
中的配位原子是_______ 。
(4)向盛有硫酸铜水溶液的试管中加入氨水,首先形成蓝色沉淀,继续加入氨水,沉淀溶解,得到深蓝色透明溶液,向该溶液中加入乙醇,析出深蓝色晶体。蓝色沉淀先溶解、后析出的原因是(用离子方程式和简单的文字说明加以解释):_______ 。
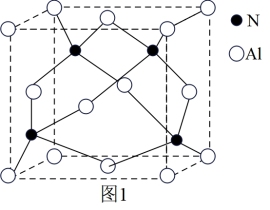
(5)氮化铝在电子工业上有广泛应用,其晶胞如图1所示。N原子所在空隙的类型是_______ (填“正四面体”“正八面体”或“立方体”)空隙,该空隙的填充率为_______ 。
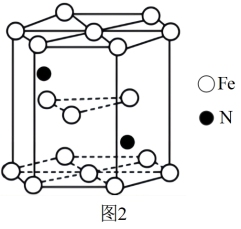
(6)铁和氮组成一种过渡金属氮化物,其结构如图2所示。直六棱柱的底边边长为xcm,高为ycm,阿伏加德罗常数的值为NA,则晶体的密度算式为_______  。
。
(1)镓的基态原子电子排布式是
(2)已知钛和铝的相对原子半径分别是1.45和1.43,钛的硬度比铝大的原因是
(3)多酚氧化酶与植物的抗病性有关。配合物
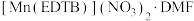 是多酚氧化酶的模型配合物。
是多酚氧化酶的模型配合物。 (EDTA)+
(EDTA)+ (邻苯二氨)
(邻苯二氨)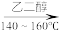
 (EDTB)
(EDTB)①EDTA中N的杂化轨道类型为
②邻苯二胺分子中
 键的数目为
键的数目为③EDTB分子中所含元素的电负性由小到大的顺序为
④与
 互为等电子体的一种阴离子为
互为等电子体的一种阴离子为⑤配离子
 中的配位原子是
中的配位原子是(4)向盛有硫酸铜水溶液的试管中加入氨水,首先形成蓝色沉淀,继续加入氨水,沉淀溶解,得到深蓝色透明溶液,向该溶液中加入乙醇,析出深蓝色晶体。蓝色沉淀先溶解、后析出的原因是(用离子方程式和简单的文字说明加以解释):
(5)氮化铝在电子工业上有广泛应用,其晶胞如图1所示。N原子所在空隙的类型是

(6)铁和氮组成一种过渡金属氮化物,其结构如图2所示。直六棱柱的底边边长为xcm,高为ycm,阿伏加德罗常数的值为NA,则晶体的密度算式为
 。
。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】 主要用于电镀工业、生产镍镉电池,用作油脂加氢催化剂、媒染剂等。某兴趣小组用含镍废催化剂(主要含有
主要用于电镀工业、生产镍镉电池,用作油脂加氢催化剂、媒染剂等。某兴趣小组用含镍废催化剂(主要含有 ,还含有
,还含有 、
、 、
、 及其他不溶于酸、碱的杂质)制备
及其他不溶于酸、碱的杂质)制备 ,其流程如下:
,其流程如下:
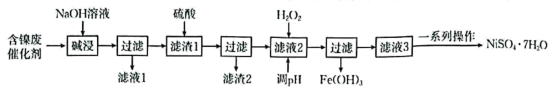
已知:①常温下,部分金属化合物的 近似值如表所示:
近似值如表所示:
②金属活泼性: 。
。
③ 。
。
回答下列问题:
(1) 元素在元素周期表中的位置为
元素在元素周期表中的位置为_______ ,其基态原子的价层电子排布式为_______ 。
(2)“滤液1”中的主要溶质为 、
、_______ 。
(3)加入硫酸时, 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(4)加入 的目的是将
的目的是将 氧化为
氧化为 ,该步骤
,该步骤_______ (填“能”或“不能”)用适量稀硝酸代替,理由是_______ 。然后调节溶液的 ,则此时应调节溶液的
,则此时应调节溶液的 至少为
至少为_______ (保留3位有效数字,离子浓度小于或等于 时认为沉淀完全),检验“滤液3”中杂质金属离子已除尽的操作和现象是
时认为沉淀完全),检验“滤液3”中杂质金属离子已除尽的操作和现象是_______ 。
(5)用配位滴定法测定粗品中 的纯度。取
的纯度。取 粗品溶于水(滴加几滴稀硫酸)配成
粗品溶于水(滴加几滴稀硫酸)配成 溶液,取
溶液,取 溶液于锥形瓶中,滴入几滴紫脲酸胺指示剂(紫色试剂,遇
溶液于锥形瓶中,滴入几滴紫脲酸胺指示剂(紫色试剂,遇 显橙黄色),用浓度为
显橙黄色),用浓度为 的
的 标准液滴定,平均消耗标准液
标准液滴定,平均消耗标准液 。已知:
。已知: 。粗品中
。粗品中 的纯度是
的纯度是_______ %;下列操作会使测定结果偏低的是_______ (填标号)。
A.锥形瓶中溶液颜色由橙黄色局部变为紫色后立即停止滴定
B.滴定前滴定管尖嘴内有气泡,滴定后尖嘴内无气泡
C.滴定前平视读数,滴定后仰视读数
 主要用于电镀工业、生产镍镉电池,用作油脂加氢催化剂、媒染剂等。某兴趣小组用含镍废催化剂(主要含有
主要用于电镀工业、生产镍镉电池,用作油脂加氢催化剂、媒染剂等。某兴趣小组用含镍废催化剂(主要含有 ,还含有
,还含有 、
、 、
、 及其他不溶于酸、碱的杂质)制备
及其他不溶于酸、碱的杂质)制备 ,其流程如下:
,其流程如下:
已知:①常温下,部分金属化合物的
 近似值如表所示:
近似值如表所示:| 化学式 |  |  | 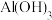 |  |  |
 近似值 近似值 | 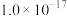 | 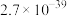 | 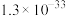 | 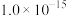 |  |
 。
。③
 。
。回答下列问题:
(1)
 元素在元素周期表中的位置为
元素在元素周期表中的位置为(2)“滤液1”中的主要溶质为
 、
、(3)加入硫酸时,
 发生反应的离子方程式为
发生反应的离子方程式为(4)加入
 的目的是将
的目的是将 氧化为
氧化为 ,该步骤
,该步骤 ,则此时应调节溶液的
,则此时应调节溶液的 至少为
至少为 时认为沉淀完全),检验“滤液3”中杂质金属离子已除尽的操作和现象是
时认为沉淀完全),检验“滤液3”中杂质金属离子已除尽的操作和现象是(5)用配位滴定法测定粗品中
 的纯度。取
的纯度。取 粗品溶于水(滴加几滴稀硫酸)配成
粗品溶于水(滴加几滴稀硫酸)配成 溶液,取
溶液,取 溶液于锥形瓶中,滴入几滴紫脲酸胺指示剂(紫色试剂,遇
溶液于锥形瓶中,滴入几滴紫脲酸胺指示剂(紫色试剂,遇 显橙黄色),用浓度为
显橙黄色),用浓度为 的
的 标准液滴定,平均消耗标准液
标准液滴定,平均消耗标准液 。已知:
。已知: 。粗品中
。粗品中 的纯度是
的纯度是A.锥形瓶中溶液颜色由橙黄色局部变为紫色后立即停止滴定
B.滴定前滴定管尖嘴内有气泡,滴定后尖嘴内无气泡
C.滴定前平视读数,滴定后仰视读数
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】铜是应用广泛的金属单质。硫酸铜晶体(CuSO4•5H2O),俗称蓝矾、胆矾,具有催吐、解毒作用,同时也是一种重要的化工原料,具有十分广泛的应用。
(1)Cu的价电子排布式为____ 。
(2)与铜同周期,N能层电子数与铜相同,熔点最低的金属是____ 。
(3)已知CuSO4在碱性条件下加入双缩脲HN(CONH2)2中,会得到紫色物质,该物质为-2价的配位阴离子,其结构如图所示。该反应原理在化学上可以用于检验蛋白质。

①该-2价的配位阴离子中sp3杂化的原子与sp2杂化的原子个数之比为____ (不考虑羰基氧的杂化)。
②该-2价的配位阴离子中Cu的配位数为____ 。
(4)卤化亚铜的熔点如表所示,CuF熔点高于其他三种卤化物,自CuCl至CuI熔点依次升高,原因是____ ;CuI的晶体类型为____ 。
(5)白铜(铜镍合金)的立方晶胞结构如图所示,其中原子A的坐标参数为(0,1,0)。

①原子B的坐标参数为____ 。
②若该晶体的密度为dg•cm-3,晶胞参数为anm,则阿伏加德罗常数值NA=____ (用含a、d的代数式表示)。
(1)Cu的价电子排布式为
(2)与铜同周期,N能层电子数与铜相同,熔点最低的金属是
(3)已知CuSO4在碱性条件下加入双缩脲HN(CONH2)2中,会得到紫色物质,该物质为-2价的配位阴离子,其结构如图所示。该反应原理在化学上可以用于检验蛋白质。

①该-2价的配位阴离子中sp3杂化的原子与sp2杂化的原子个数之比为
②该-2价的配位阴离子中Cu的配位数为
(4)卤化亚铜的熔点如表所示,CuF熔点高于其他三种卤化物,自CuCl至CuI熔点依次升高,原因是
| 化合物 | CuF | CuCl | CuBr | CuI |
| 熔点/℃ | 908 | 426 | 498 | 605 |

①原子B的坐标参数为
②若该晶体的密度为dg•cm-3,晶胞参数为anm,则阿伏加德罗常数值NA=
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】在一定条件下,金属相互化合形成的化合物称为金属互化物,如Cu9Al4、Cu5Zn8等。
(1)某金属互化物具有自范性,原子在三维空间里呈周期性有序排列,该金属互化物属于________ (填“晶体”或“非晶体”)。
(2)基态铜原子有________ 个未成对电子;Cu2+的电子排布式为____________________ ;在CuSO4溶液中加入过量氨水,充分反应后加入少量乙醇,析出一种深蓝色晶体,该晶体的化学式为____________________ ,其所含化学键有____________________ ,乙醇分子中C原子的杂化轨道类型为________ 。
(3)铜能与类卤素(SCN)2反应生成Cu(SCN)2,1 mol(SCN)2分子中含有σ键的数目为________ 。(SCN)2对应的酸有硫氰酸(H—S—C≡N)、异硫氰酸(H—N===C===S)两种。理论上前者沸点低于后者,其原因是______________________________________________________________________________________ 。
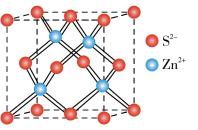
(4)ZnS的晶胞结构如图所示,在ZnS晶胞中,S2-的配位数为_______________ 。
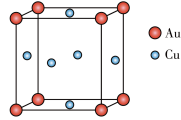
(5)铜与金形成的金属互化物的晶胞结构如图所示,其晶胞边长为a nm,该金属互化物的密度为________ g·cm-3(用含a、NA的代数式表示)。
(1)某金属互化物具有自范性,原子在三维空间里呈周期性有序排列,该金属互化物属于
(2)基态铜原子有
(3)铜能与类卤素(SCN)2反应生成Cu(SCN)2,1 mol(SCN)2分子中含有σ键的数目为

(4)ZnS的晶胞结构如图所示,在ZnS晶胞中,S2-的配位数为

(5)铜与金形成的金属互化物的晶胞结构如图所示,其晶胞边长为a nm,该金属互化物的密度为
您最近一年使用:0次
【推荐3】回答下列问题
(1)有下列固体:①水晶 ②冰醋酸 ③灰锡 ④干冰 ⑤过氧化钠 ⑥碳化钙(CaC2) ⑦刚玉 ⑧Si3N4⑨白磷 ⑩氩 ⑪尿素 ⑫AlCl3⑬铁铝合金 ⑭SiCl4其中含有极性键的分子晶体:_______ (填编号)
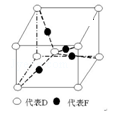
(2)NaCl晶体在50~300GPa 的高压下和Na 或Cl2反应,可以形成不同组成、不同结构的晶体和颗粒。下图给出了其中三种晶体A、B、C的晶胞(大球为氯原子,小球为钠原子),D是纳米颗粒,大小和形状则恰好如图所示。

写出A、B、C、D 的化学式。A:_______ ;B:_______ ;C:_______ ;D:_______ ;
(3)石墨一种晶胞结构和部分晶胞参数如图。原子坐标参数描述的是晶胞内原子间的相对位置。石墨晶胞中碳原子A、B的坐标参数分别为A(0,0,0)、B(0,1, ),则C原子的坐标参数为
),则C原子的坐标参数为_______ 。
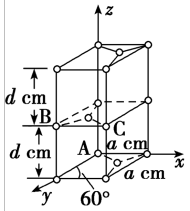
(4)灰硒的晶体为六方晶胞结构,原子排列为无限螺旋链,分布在六方晶格上,同一条链内原子作用力很强,相邻链之间原子作用较弱,其螺旋链状图、晶胞结构图、晶胞俯视图如图所示。

已知正六棱柱的边长为acm,高为bcm,阿伏加德罗常数的值为NA,则该晶体的密度为_______ g·cm-3(用含NA、a、b的式子表示)。
(1)有下列固体:①水晶 ②冰醋酸 ③灰锡 ④干冰 ⑤过氧化钠 ⑥碳化钙(CaC2) ⑦刚玉 ⑧Si3N4⑨白磷 ⑩氩 ⑪尿素 ⑫AlCl3⑬铁铝合金 ⑭SiCl4其中含有极性键的分子晶体:
(2)NaCl晶体在50~300GPa 的高压下和Na 或Cl2反应,可以形成不同组成、不同结构的晶体和颗粒。下图给出了其中三种晶体A、B、C的晶胞(大球为氯原子,小球为钠原子),D是纳米颗粒,大小和形状则恰好如图所示。

写出A、B、C、D 的化学式。A:
(3)石墨一种晶胞结构和部分晶胞参数如图。原子坐标参数描述的是晶胞内原子间的相对位置。石墨晶胞中碳原子A、B的坐标参数分别为A(0,0,0)、B(0,1,
 ),则C原子的坐标参数为
),则C原子的坐标参数为
(4)灰硒的晶体为六方晶胞结构,原子排列为无限螺旋链,分布在六方晶格上,同一条链内原子作用力很强,相邻链之间原子作用较弱,其螺旋链状图、晶胞结构图、晶胞俯视图如图所示。

已知正六棱柱的边长为acm,高为bcm,阿伏加德罗常数的值为NA,则该晶体的密度为
您最近一年使用:0次



