选考[化学—选修化学与技术]
通常情况下,当空气中CO2的体积分数超过0.050%时,会引起明显的温室效应。为减小和消除CO2对环境的影响,各国都在限制CO2的排量,同时也加强对CO2创新利用的研究。
(1)目前,推广用超临界CO2(介于气态和液态之间)代替氟利昂作制冷剂,这一做法对环境的积极意义是___________________________ 。
(2)科学家为提取空气中的CO2,把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应使之变为可再生燃料甲醇。流程如图:
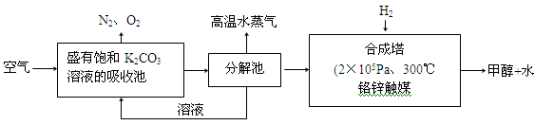
①分解池中反应的化学方程式为:___________________ 。
②合成塔中,若有4.4g CO2与足量H2恰好反应生成气态产物,放出4.947kJ的热量,写出该反应的热化学方程式:______________________________ 。
(3)某同学拟用沉淀法测定空气中CO2的体积分数,他查得CaCO3、BaCO3的溶度积Ksp分别为4.96×10-9、2.58×10-9。他最好将空气通入足量的__________ 溶液,实验时除测定温度、压强和空气的体积外,还需测定__________________ 。
通常情况下,当空气中CO2的体积分数超过0.050%时,会引起明显的温室效应。为减小和消除CO2对环境的影响,各国都在限制CO2的排量,同时也加强对CO2创新利用的研究。
(1)目前,推广用超临界CO2(介于气态和液态之间)代替氟利昂作制冷剂,这一做法对环境的积极意义是
(2)科学家为提取空气中的CO2,把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应使之变为可再生燃料甲醇。流程如图:

①分解池中反应的化学方程式为:
②合成塔中,若有4.4g CO2与足量H2恰好反应生成气态产物,放出4.947kJ的热量,写出该反应的热化学方程式:
(3)某同学拟用沉淀法测定空气中CO2的体积分数,他查得CaCO3、BaCO3的溶度积Ksp分别为4.96×10-9、2.58×10-9。他最好将空气通入足量的
2010·宁夏银川·二模 查看更多[3]
更新时间:2016-12-09 00:25:57
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】甲烷是一种重要的基础化工原料,不仅可制备多种重要有机产品,还可用于环境保护。请回答下列问题:
(1)用甲烷催化还原氮的氧化物可消除氮氧化物的污染。已知:

反应过程(2)是__ 反应(填“放热”或“吸热”),甲烷还原NO2生成H2O(g)、N2和CO2时的热化学方程式是__ 。
(2)工厂利用甲烷与氯气的反应原理制取氯甲烷,为妥善处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏。化学家研究在催化条件下,通过下列反应:CCl4(g)+H2(g) CHCl3(g)+HCl(g),使CCl4转化为重要的化工原料氯仿(CHCl3)(不考虑副反应)。在固定容积为2L的密闭容器中,该反应达到平衡后,测得如下数据:
CHCl3(g)+HCl(g),使CCl4转化为重要的化工原料氯仿(CHCl3)(不考虑副反应)。在固定容积为2L的密闭容器中,该反应达到平衡后,测得如下数据:
①此反应在110℃时平衡常数为___ 。
②实验l中,CCl4的转化率为__ 。
③判断该反应的正反应是__ (填“放热”或“吸热”),理由是__ 。
④为提高实验3中CCl4的转化率,可采取的措施是__ 。
a.使用高效催化剂
b.向容器中再投入1molCCl4和1molH2
c.温度升高到200℃
d.向容器中再投入1molHCl
e.向容器中再投入1molH2
(1)用甲烷催化还原氮的氧化物可消除氮氧化物的污染。已知:

反应过程(2)是
(2)工厂利用甲烷与氯气的反应原理制取氯甲烷,为妥善处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏。化学家研究在催化条件下,通过下列反应:CCl4(g)+H2(g)
 CHCl3(g)+HCl(g),使CCl4转化为重要的化工原料氯仿(CHCl3)(不考虑副反应)。在固定容积为2L的密闭容器中,该反应达到平衡后,测得如下数据:
CHCl3(g)+HCl(g),使CCl4转化为重要的化工原料氯仿(CHCl3)(不考虑副反应)。在固定容积为2L的密闭容器中,该反应达到平衡后,测得如下数据:| 实验 序号 | 温度℃ | 初始n(CCl4)( mol) | 初始n(H2)( mol) | 平衡时n(CHCl3)( mol) |
| 1 | 110 | 0.8 | 1.2 | |
| 2 | 110 | 2 | 2 | 1 |
| 3 | 100 | 1 | 1 | 0.6 |
①此反应在110℃时平衡常数为
②实验l中,CCl4的转化率为
③判断该反应的正反应是
④为提高实验3中CCl4的转化率,可采取的措施是
a.使用高效催化剂
b.向容器中再投入1molCCl4和1molH2
c.温度升高到200℃
d.向容器中再投入1molHCl
e.向容器中再投入1molH2
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
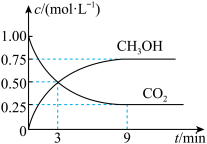
【推荐2】CO2可转化成有机物实现碳循环。在体积为2L的恒温密闭容器中,按物质的量之比1∶3.5充入CO2和H2,一定条件下发生反应:
 ,测得CO2和CH3OH的浓度随时间变化如图所示。
,测得CO2和CH3OH的浓度随时间变化如图所示。
已知键能数据:
(1)
___________ 。
(2)能说明上述反应达到平衡状态的是___________ (填字母)。
A.反应中CO2和CH3OH的物质的量浓度之比为1∶1(即图中交叉点)
B.混合气体的压强不随时间的变化而变化
C.单位时间内生成 ,同时生成
,同时生成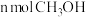
D.混合气体的平均相对分子质量不随时间的变化而变化
E.混合气体的密度不随时间的变化而变化
(3)平衡时H2的转化率为___________ (保留一位小数)。
(4)保持温度和容积不变,除充入H2外,还能使平衡后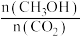 增大的措施是
增大的措施是___________ (任写两条)。
(5)若其他条件不变,平衡后再同时充入四种物质各0.5mol,则平衡如何移动?请简要说明理由:___________ 。

 ,测得CO2和CH3OH的浓度随时间变化如图所示。
,测得CO2和CH3OH的浓度随时间变化如图所示。
已知键能数据:
| C=O | C-O | C-H | H-H | O-H | |
| 键能/kJ/mol | 799 | 358 | 411 | 432 | 459 |

(2)能说明上述反应达到平衡状态的是
A.反应中CO2和CH3OH的物质的量浓度之比为1∶1(即图中交叉点)
B.混合气体的压强不随时间的变化而变化
C.单位时间内生成
 ,同时生成
,同时生成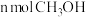
D.混合气体的平均相对分子质量不随时间的变化而变化
E.混合气体的密度不随时间的变化而变化
(3)平衡时H2的转化率为
(4)保持温度和容积不变,除充入H2外,还能使平衡后
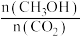 增大的措施是
增大的措施是(5)若其他条件不变,平衡后再同时充入四种物质各0.5mol,则平衡如何移动?请简要说明理由:
您最近一年使用:0次
【推荐3】研究和深度开发CO、CO2的应用具有重要的社会意义。回答下列问题:
I.CO可用于高炉炼铁,已知:
Fe3O4(s)+4CO(g)=3Fe(s)+4CO2(g)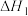 =a kJ·mol-1
=a kJ·mol-1
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) =b kJ·mol-1
=b kJ·mol-1
(1)反应Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) =
=______ kJ·mol-1
Ⅱ.某温度下,在容积为2L的恒容密闭容器中投入8mol CO2(g)、16 mol H2(g)发生反应CO2(g)+H2(g)⇌CO(g)+H2O(g)。反应15min后达到平衡,此时CO2的转化率为75%。
(2)0~15min内用二氧化碳表示的平均反应速率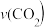 =
=_______ ;计算此条件下该反应的平衡常数K=______ 。
Ⅲ.捕碳技术是指从空气中捕获二氧化碳的各种科学技术的统称。目前NH3和(NH4)2CO3,等物质已经被用作工业捕碳剂。
(3)用(NH4)2CO3捕碳的反应为 。为研究温度对(NH4)2CO3捕获CO2效率的影响,将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体,保持其他初始实验条件不变,分别在不同温度下,经过相同时间测得CO2气体浓度,得到的趋势图如图所示。
。为研究温度对(NH4)2CO3捕获CO2效率的影响,将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体,保持其他初始实验条件不变,分别在不同温度下,经过相同时间测得CO2气体浓度,得到的趋势图如图所示。
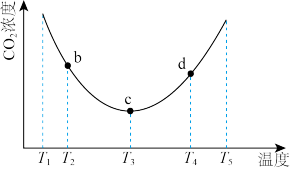
①c点的逆反应速率和d点的正反应速率的大小关系为v逆c______ (填“>”“=”或“<”)v正d。
②b、c、d三点的平衡常数Kb、Kc、Kd 从大到小的顺序为______ 。
I.CO可用于高炉炼铁,已知:
Fe3O4(s)+4CO(g)=3Fe(s)+4CO2(g)
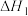 =a kJ·mol-1
=a kJ·mol-1 3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g)
 =b kJ·mol-1
=b kJ·mol-1(1)反应Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)
 =
=Ⅱ.某温度下,在容积为2L的恒容密闭容器中投入8mol CO2(g)、16 mol H2(g)发生反应CO2(g)+H2(g)⇌CO(g)+H2O(g)。反应15min后达到平衡,此时CO2的转化率为75%。
(2)0~15min内用二氧化碳表示的平均反应速率
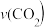 =
=Ⅲ.捕碳技术是指从空气中捕获二氧化碳的各种科学技术的统称。目前NH3和(NH4)2CO3,等物质已经被用作工业捕碳剂。
(3)用(NH4)2CO3捕碳的反应为
 。为研究温度对(NH4)2CO3捕获CO2效率的影响,将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体,保持其他初始实验条件不变,分别在不同温度下,经过相同时间测得CO2气体浓度,得到的趋势图如图所示。
。为研究温度对(NH4)2CO3捕获CO2效率的影响,将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体,保持其他初始实验条件不变,分别在不同温度下,经过相同时间测得CO2气体浓度,得到的趋势图如图所示。
①c点的逆反应速率和d点的正反应速率的大小关系为v逆c
②b、c、d三点的平衡常数Kb、Kc、Kd 从大到小的顺序为
您最近一年使用:0次
【推荐1】页岩气的主要成分为CH4,还含有少量的CO2、H2S等气体,工业上可采用下列方法除去其中的CO2、H2S。
I.CO2的处理:
(1)CO2和CH4重整可制得合成气(CO、H2)。已知下列热化学反应方程式:
CH4(g)=C(s)+2H2(g); ΔH=74.5kJ·mol-1
CO2(g)+H2(g)=CO(g)+H2O(g); ΔH=40.0kJ·mol-1
C(s)+H2O(g)=CO(g)+H2(g); ΔH=+132.0kJ·mol-1
反应CO2(g)+CH4(g)=2CO(g)+2H2(g)的ΔH=___________ kJ·mol-1。
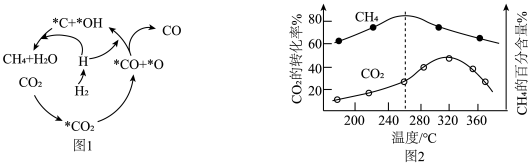
(2)Ni催化CO2加H2形成CH4,其历程如图1所示(吸附在催化剂表面的物种用*标注),反应相同时间,含碳产物中CH4的百分含量及CO2的转化率随温度的变化如图2所示。
①260℃时生成主要产物所发生反应的化学方程式为___________ 。
②温度高于320℃,CO2的转化率下降的原因是___________ 。
(3)利用电解转化法从烟气中分离CO2的原理如图3所示。已知气体可选择性通过膜电极,溶液不能通过。写出电解时膜电极b上所发生的电极反应式:___________ 。

II.H2S的处理:Fe2O3可用作脱除H2S气体的脱硫剂,其脱硫和再生的原理如图4所示。
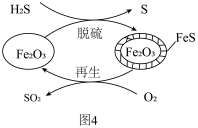
(4)Fe2O3脱硫剂的脱硫和再生过程可以描述为___________ 。
(5)脱硫剂再生时可以使用水蒸气代替O2,700℃条件下生成Fe3O4、H2S和H2.采用O2和水蒸气混合再生的方法,可以将产生的SO2和H2S全部转化为S单质。理论上O2和水蒸气的物质的量之比应为___________ 。
I.CO2的处理:
(1)CO2和CH4重整可制得合成气(CO、H2)。已知下列热化学反应方程式:
CH4(g)=C(s)+2H2(g); ΔH=74.5kJ·mol-1
CO2(g)+H2(g)=CO(g)+H2O(g); ΔH=40.0kJ·mol-1
C(s)+H2O(g)=CO(g)+H2(g); ΔH=+132.0kJ·mol-1
反应CO2(g)+CH4(g)=2CO(g)+2H2(g)的ΔH=
(2)Ni催化CO2加H2形成CH4,其历程如图1所示(吸附在催化剂表面的物种用*标注),反应相同时间,含碳产物中CH4的百分含量及CO2的转化率随温度的变化如图2所示。

①260℃时生成主要产物所发生反应的化学方程式为
②温度高于320℃,CO2的转化率下降的原因是
(3)利用电解转化法从烟气中分离CO2的原理如图3所示。已知气体可选择性通过膜电极,溶液不能通过。写出电解时膜电极b上所发生的电极反应式:

II.H2S的处理:Fe2O3可用作脱除H2S气体的脱硫剂,其脱硫和再生的原理如图4所示。

(4)Fe2O3脱硫剂的脱硫和再生过程可以描述为
(5)脱硫剂再生时可以使用水蒸气代替O2,700℃条件下生成Fe3O4、H2S和H2.采用O2和水蒸气混合再生的方法,可以将产生的SO2和H2S全部转化为S单质。理论上O2和水蒸气的物质的量之比应为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】目前有效控制及高效利用CO、 的研究正引起全球广泛关注,根据
的研究正引起全球广泛关注,根据 中国化工报
中国化工报 报道,美国科学家发现了几种新的可将CO、
报道,美国科学家发现了几种新的可将CO、 转化为甲醇的高活性催化体系,比目前工业使用的常见催化剂快近 90倍。
转化为甲醇的高活性催化体系,比目前工业使用的常见催化剂快近 90倍。
已知工业上可以利用 制备
制备 涉及反应如下:
涉及反应如下:
反应I: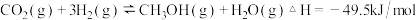
反应II:
(1)写出工业上CO和 制取甲醇的热化学方程式
制取甲醇的热化学方程式 ______ 。
(2)反应I能自发进行的条件是______ 。
(3)一定温度下, 、CO在体积固定的密闭容器中发生如下反应:
、CO在体积固定的密闭容器中发生如下反应: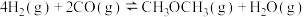 ,下列选项能判断该反应达到平衡状态的依据有
,下列选项能判断该反应达到平衡状态的依据有 ______ 。
A.该反应的平衡常数不变
 的消耗速率等于
的消耗速率等于 的生成速率
的生成速率
C.容器内的压强保持不变
 混合气体的密度保持不变
混合气体的密度保持不变
E.混合气体的平均相对分子质量不随时间而变化
(4)500K, 恒容密闭容器中充入
恒容密闭容器中充入 的
的  和
和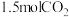 仅发生反应I,该反应10min时生成
仅发生反应I,该反应10min时生成 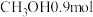 ,此时达到平衡:
,此时达到平衡:
①用氢气表示该反应的速率为______ 。
②该温度下,反应I的平衡常数为______ 。
 的研究正引起全球广泛关注,根据
的研究正引起全球广泛关注,根据 中国化工报
中国化工报 报道,美国科学家发现了几种新的可将CO、
报道,美国科学家发现了几种新的可将CO、 转化为甲醇的高活性催化体系,比目前工业使用的常见催化剂快近 90倍。
转化为甲醇的高活性催化体系,比目前工业使用的常见催化剂快近 90倍。已知工业上可以利用
 制备
制备 涉及反应如下:
涉及反应如下:反应I:
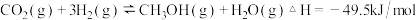
反应II:

(1)写出工业上CO和
 制取甲醇的热化学方程式
制取甲醇的热化学方程式 (2)反应I能自发进行的条件是
(3)一定温度下,
 、CO在体积固定的密闭容器中发生如下反应:
、CO在体积固定的密闭容器中发生如下反应: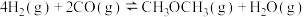 ,下列选项能判断该反应达到平衡状态的依据有
,下列选项能判断该反应达到平衡状态的依据有 A.该反应的平衡常数不变
 的消耗速率等于
的消耗速率等于 的生成速率
的生成速率C.容器内的压强保持不变
 混合气体的密度保持不变
混合气体的密度保持不变E.混合气体的平均相对分子质量不随时间而变化
(4)500K,
 恒容密闭容器中充入
恒容密闭容器中充入 的
的  和
和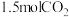 仅发生反应I,该反应10min时生成
仅发生反应I,该反应10min时生成 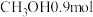 ,此时达到平衡:
,此时达到平衡:①用氢气表示该反应的速率为
②该温度下,反应I的平衡常数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】在元素周期表中,锌(30Zn)、镉(48Cd)、汞(80Hg)同属于锌族,锌和汞在自然界中常共生,镉的金属活动性介于锌和汞之间。湿法炼锌过程中产生的铜镉渣中含有Cu、Cd、Zn等多种金属,可用于生产金属镉。镉的主要用途可以用作镍―镉电池,以及用于颜料生产,镉化合物还在PVC稳定剂、发光材料、半导体材料、杀菌剂等方面有广泛的应用。镉的生产流程如图示意如下:
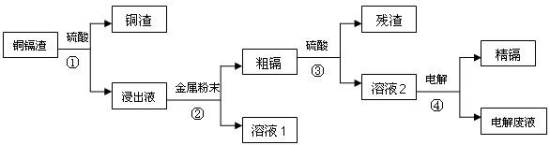 请回答下列问题:
请回答下列问题:
(1)镉元素位于周期表中第_____ 周期,第_____ 族,其原子结构示意图为_________ ;
(2)写出步骤①反应的离子方程式______________ 。
(3)步骤②所加入的金属是______________ 。
(4)步骤④用“溶液2”作电解液,镉在__________ 极析出,该电极材料是______ ;
(5) “电解废液”中含有镉,不能直接作为污水排放。目前含镉的废水处理的方式有两种,一种是在含镉污水中加入硫化钠,沉淀镉离子,另一种是加入聚合硫酸铁和聚合氯化铝,沉淀镉离子。写出硫化钠沉淀镉离子的离子方程式____________ 。
 请回答下列问题:
请回答下列问题:(1)镉元素位于周期表中第
(2)写出步骤①反应的离子方程式
(3)步骤②所加入的金属是
(4)步骤④用“溶液2”作电解液,镉在
(5) “电解废液”中含有镉,不能直接作为污水排放。目前含镉的废水处理的方式有两种,一种是在含镉污水中加入硫化钠,沉淀镉离子,另一种是加入聚合硫酸铁和聚合氯化铝,沉淀镉离子。写出硫化钠沉淀镉离子的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】铬渣是生产金属铬和铬盐过程中产生的工业废渣,其中含有Na2SO4及少量Cr2O72—、Fe3+。从铬渣中提取Na2SO4的工艺流程:
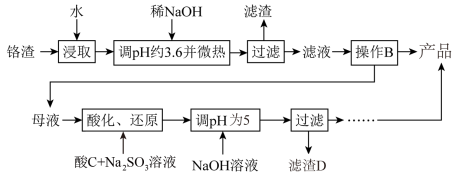
已知:常温时,Fe3+、Cr3+完全沉淀时c≤1×10-5mol·L-1,Ksp[Fe(OH)3]=4×10-38,Ksp[Cr(OH)3]=6×10-31。
(1)调pH约为3.6目的是_________ 。
(2)根据下图溶解度(S)—温度(T)曲线,判断操作B为蒸发浓缩、_________________ 。
(3)“酸化、还原”步骤反应的离子方程式为_______________________________ 。
(4)滤渣D为________________________ (填化学式)。
(5)如图,某工厂采用电解法处理含铬废水,用铁板作阴阳极,槽中盛放含铬废水,A接电源的_______ 极;阳极区溶液中发生的氧化还原反应为__________________ 。若不考虑气体的溶解,当收集到6.72L(标准状况)的H2时,理论上有___ molCr2O72—被还原。


已知:常温时,Fe3+、Cr3+完全沉淀时c≤1×10-5mol·L-1,Ksp[Fe(OH)3]=4×10-38,Ksp[Cr(OH)3]=6×10-31。
(1)调pH约为3.6目的是
(2)根据下图溶解度(S)—温度(T)曲线,判断操作B为蒸发浓缩、
(3)“酸化、还原”步骤反应的离子方程式为
(4)滤渣D为
(5)如图,某工厂采用电解法处理含铬废水,用铁板作阴阳极,槽中盛放含铬废水,A接电源的

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】硫酸锌可作为食品锌强化剂的原料。工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3 、FeCO3 MgO、CaO等,生产工艺流程示意如下:
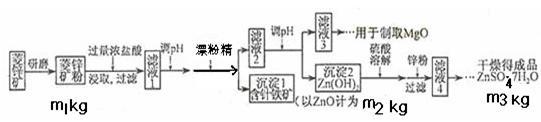
(1)将菱锌矿研磨成粉的目的是_______ ,滤液1后两步操作的目是:__________________ 。
(2)完成加漂粉精反应的离子方程式:
_____ Fe(OH)2+_____ ____ +____ _____ →_____ Fe(OH)3+______ Cl-
(3)针铁矿的组成元素是Fe、O和H,化学式量为89,化学式是_______ 。
(4)为了了解如何调节滤液2的PH,请写出两个你认为需要查阅的数据_______________________ ,________________________ (用文字叙述)
(5)“滤液4”之后的操作依次为______ 、_______ 、过滤,洗涤,干燥。
(6)分析图中数据,菱锌矿粉中ZnCO3的质量分数不低于________ 。

(1)将菱锌矿研磨成粉的目的是
(2)完成加漂粉精反应的离子方程式:
(3)针铁矿的组成元素是Fe、O和H,化学式量为89,化学式是
(4)为了了解如何调节滤液2的PH,请写出两个你认为需要查阅的数据
(5)“滤液4”之后的操作依次为
(6)分析图中数据,菱锌矿粉中ZnCO3的质量分数不低于
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】SO2是高中化学重点学习的三大气体之一,是常见的大气污染物之一,同时也是重要的工业原料,探究其制备方法和性质具有非常重要的意义,请回答下列问题。
Ⅰ.某研究小组将纯净的SO2气体通入0.5 mol·L-1的Ba(NO3)2溶液中,得到了BaSO4沉淀。为探究上述溶液中何种微粒能氧化通入的SO2,该小组提出了如下假设:
假设一:溶液中的NO ;假设二:溶液中溶解的O2
;假设二:溶液中溶解的O2
(1)验证假设一:
①请在下表空白处填写相关实验现象
②设计实验一的目的是________________ 。
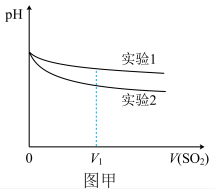
(2)为深入研究该反应,该小组还测得上述两个实验中溶液的pH随通入SO2体积的变化曲线如图甲。实验2中溶液pH小于实验1的原因是(用离子方程式表示)___________________ 。
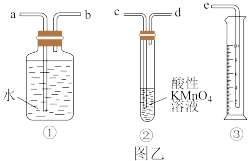
Ⅱ.我国规定空气中SO2含量不得超过0.02 mg/L。某化学兴趣小组选用图乙实验装置,测定工业原料气(含SO2、N2、O2)中SO2的含量。
(3)若原料气从左向右流,上述装置连接的顺序是:原料气→_______________ (用字母和箭头表示)。当装置②中出现______ 现象时,立即停止通气。
(4)你认为以下试剂中,可以用来代替试管中的酸性高锰酸钾溶液的是________。
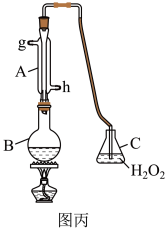
Ⅲ.中华人民共和国国家标准(GB2760-2011)规定葡萄酒中SO2最大使用量为0.25g/L。某兴趣小组用图丙装置(夹持装置略)收集某葡萄酒中SO2,并对含量定性测定。
(5)B中加入250.00ml葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,除去C中过量的H2O2,然后用0.0600mol/LNaOH标准溶液进行滴定,滴定至终点时,消耗NaOH溶液25.00ml,该葡萄酒中SO2含量为__________ g/L。
(6)该测定结果比实际值偏高,分析原因并利用现有装置提出改进措施______________ 。
Ⅰ.某研究小组将纯净的SO2气体通入0.5 mol·L-1的Ba(NO3)2溶液中,得到了BaSO4沉淀。为探究上述溶液中何种微粒能氧化通入的SO2,该小组提出了如下假设:
假设一:溶液中的NO
 ;假设二:溶液中溶解的O2
;假设二:溶液中溶解的O2(1)验证假设一:
①请在下表空白处填写相关实验现象
| 实 验 步 骤 | 实验现象 | 结论 |
| 实验1:在盛有不含O2的10 mL 0.5 mol/L BaCl2溶液的烧杯中,缓慢通入纯净的SO2气体。 | 假设一 成立 | |
| 实验2:在盛有不含O2的10 mL 0.5mol/L Ba(NO3)2溶液的烧杯中,缓慢通入纯净的SO2气体。 |
(2)为深入研究该反应,该小组还测得上述两个实验中溶液的pH随通入SO2体积的变化曲线如图甲。实验2中溶液pH小于实验1的原因是(用离子方程式表示)


Ⅱ.我国规定空气中SO2含量不得超过0.02 mg/L。某化学兴趣小组选用图乙实验装置,测定工业原料气(含SO2、N2、O2)中SO2的含量。
(3)若原料气从左向右流,上述装置连接的顺序是:原料气→
(4)你认为以下试剂中,可以用来代替试管中的酸性高锰酸钾溶液的是________。
| A.NaOH溶液 | B.溴水 |
| C.氨水 | D.BaCl2溶液 |

Ⅲ.中华人民共和国国家标准(GB2760-2011)规定葡萄酒中SO2最大使用量为0.25g/L。某兴趣小组用图丙装置(夹持装置略)收集某葡萄酒中SO2,并对含量定性测定。
(5)B中加入250.00ml葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,除去C中过量的H2O2,然后用0.0600mol/LNaOH标准溶液进行滴定,滴定至终点时,消耗NaOH溶液25.00ml,该葡萄酒中SO2含量为
(6)该测定结果比实际值偏高,分析原因并利用现有装置提出改进措施
您最近一年使用:0次
【推荐2】合理利用资源,加强环境保护,降低碳的排放,实施低碳经济是今后经济生活主流。
(1)下列措施不利于有效减少二氧化碳排放的是___ 。
A.植树造林,保护森林,保护植被
B.加大对煤和石油的开采,并鼓励使用石油液化气
C.大力发展风能、水力、潮汐能发电和核电,大力推行太阳能的综合开发
D.推广使用节能灯和节能电器,使用空调时夏季温度不宜设置过低,冬天不宜过高
E.倡导出行时多步行和骑自行车,建设现代物流信息系统,减少运输工具空驶率
(2)科学家致力于二氧化碳的“组合转化”技术研究,如将CO2和H2以1∶4比例混合通入反应器,在适当条件下反应可获得一种重要能源。请完成以下化学方程式:
CO2+4H2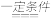
______ +2H2O。
(3)CO2合成生产燃料甲醇(CH3OH)是碳减排的新方向。现进行如下实验:某温度下在体积为1 L的密闭容器中,充入2 mol CO2和6 mol H2,发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)能判断该反应已达化学反应限度的标志是
CH3OH(g)+H2O(g)能判断该反应已达化学反应限度的标志是____ (填字母)。
A.CO2百分含量保持不变
B.容器中H2浓度与CO2浓度之比为3:1
C.容器中混合气体的质量保持不变
D.CO2的生成速率与CH3OH的生成速率相等
现测得CO2和CH3OH(g)的浓度随时间变化如图所示。

从反应开始到平衡,氢气的平均反应速率v(H2)=_____ mol/(L·min)。
(4)以KOH为电解质的甲醇燃料电池总反应为:2CH3OH+3O2+4KOH = 2K2CO3+6H2O,通入甲醇的电极为燃料电池的___ 极,正极发生的电极反应式为______ 。
(1)下列措施不利于有效减少二氧化碳排放的是
A.植树造林,保护森林,保护植被
B.加大对煤和石油的开采,并鼓励使用石油液化气
C.大力发展风能、水力、潮汐能发电和核电,大力推行太阳能的综合开发
D.推广使用节能灯和节能电器,使用空调时夏季温度不宜设置过低,冬天不宜过高
E.倡导出行时多步行和骑自行车,建设现代物流信息系统,减少运输工具空驶率
(2)科学家致力于二氧化碳的“组合转化”技术研究,如将CO2和H2以1∶4比例混合通入反应器,在适当条件下反应可获得一种重要能源。请完成以下化学方程式:
CO2+4H2
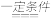
(3)CO2合成生产燃料甲醇(CH3OH)是碳减排的新方向。现进行如下实验:某温度下在体积为1 L的密闭容器中,充入2 mol CO2和6 mol H2,发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)能判断该反应已达化学反应限度的标志是
CH3OH(g)+H2O(g)能判断该反应已达化学反应限度的标志是A.CO2百分含量保持不变
B.容器中H2浓度与CO2浓度之比为3:1
C.容器中混合气体的质量保持不变
D.CO2的生成速率与CH3OH的生成速率相等
现测得CO2和CH3OH(g)的浓度随时间变化如图所示。

从反应开始到平衡,氢气的平均反应速率v(H2)=
(4)以KOH为电解质的甲醇燃料电池总反应为:2CH3OH+3O2+4KOH = 2K2CO3+6H2O,通入甲醇的电极为燃料电池的
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.氮元素在地球上含量丰富,氮及其化合物在工农业生产和生活中有着重要作用,氮氧化物也是主要的大气污染物。
(1)汽车尾气中的NO和CO气体,可以利用催化剂转化为对环境无害的两种气体,请写出该过程的化学方程式___________ ;
(2)含有NO和NO2的工业尾气可以利用NaOH溶液吸收处理。主要反应为NO+NO2+2OH-=2NO +H2O、2NO2+2OH-=NO
+H2O、2NO2+2OH-=NO +NO
+NO +H2O。
+H2O。
①下列措施不能提高尾气中NO和NO2去除率的有___________ (填标号)。
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气的过程中定期补加适量NaOH溶液
D.将尾气通入NaOH溶液的同时通入氧气
②若将NO和NO2组成的混合气体通入1L0.5mol/LNaOH溶液中,NaOH和气体恰好完全反应,吸收后的溶液经浓缩、结晶、过滤、洗涤、干燥后,得到晶体36.9g,则原混合气体中NO和NO2的物质的量之比为___________ 。
(3)用HClO也可以吸收工业尾气中的NO,HClO氧化NO生成Cl-和NO ,其离子方程式为
,其离子方程式为___________ 。
Ⅱ.该研究性学习小组同学还认为NO易与O2发生反应,应该更易被氧化。查阅资料:2NO+Na2O2=2NaNO2;2NaNO2+2HCl=2NaCl+NO2↑+NO↑+H2O;酸性条件下,NO能与MnO 反应生成NO
反应生成NO 和Mn2+。
和Mn2+。
(4)丙同学用下图所示装置(部分夹持装置略)探究NO与Na2O2的反应。___________ ;
②C中所装试剂可以是___________ ;
③充分反应后,检验D装置中产物的方法是:取D装置中产物少许,___________ ,则产物是NaNO2。
(1)汽车尾气中的NO和CO气体,可以利用催化剂转化为对环境无害的两种气体,请写出该过程的化学方程式
(2)含有NO和NO2的工业尾气可以利用NaOH溶液吸收处理。主要反应为NO+NO2+2OH-=2NO
 +H2O、2NO2+2OH-=NO
+H2O、2NO2+2OH-=NO +NO
+NO +H2O。
+H2O。①下列措施不能提高尾气中NO和NO2去除率的有
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气的过程中定期补加适量NaOH溶液
D.将尾气通入NaOH溶液的同时通入氧气
②若将NO和NO2组成的混合气体通入1L0.5mol/LNaOH溶液中,NaOH和气体恰好完全反应,吸收后的溶液经浓缩、结晶、过滤、洗涤、干燥后,得到晶体36.9g,则原混合气体中NO和NO2的物质的量之比为
(3)用HClO也可以吸收工业尾气中的NO,HClO氧化NO生成Cl-和NO
 ,其离子方程式为
,其离子方程式为Ⅱ.该研究性学习小组同学还认为NO易与O2发生反应,应该更易被氧化。查阅资料:2NO+Na2O2=2NaNO2;2NaNO2+2HCl=2NaCl+NO2↑+NO↑+H2O;酸性条件下,NO能与MnO
 反应生成NO
反应生成NO 和Mn2+。
和Mn2+。(4)丙同学用下图所示装置(部分夹持装置略)探究NO与Na2O2的反应。
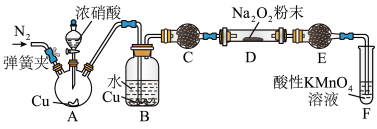
②C中所装试剂可以是
③充分反应后,检验D装置中产物的方法是:取D装置中产物少许,
您最近一年使用:0次




