有短周期元素A、B、C、D、E,已知:
①常温下,A元素的单质在空气或浓硫酸中,表面都能生成致密的氧化膜
② B元素的原子序数比A元素大,其原子的次外层的电子数是最外层电子数的2倍
③ E与A同周期,C、D、E三种元素形成的单质或化合物可发生如下图所示的反应。
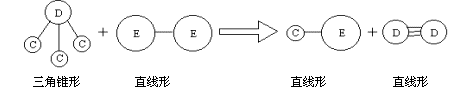
请用化学式或相应的符号回答下列问题:
(1)写出A元素最高价氧化物与NaOH溶液反应的离子方程式__________ ;
(2)B元素在元素周期表第_____ 周期第____ 族;
B的固态氧化物的晶体类型是_____ ;
(3)D元素的原子结构示意图是:_____________________ ;
(4)B元素与E元素的最高价氧化物的水化物的酸性强弱_____ >_______ ;
(5)请用化学方程式表示E元素的单质在工业上的一种重要用途:____ 。
①常温下,A元素的单质在空气或浓硫酸中,表面都能生成致密的氧化膜
② B元素的原子序数比A元素大,其原子的次外层的电子数是最外层电子数的2倍
③ E与A同周期,C、D、E三种元素形成的单质或化合物可发生如下图所示的反应。

请用化学式或相应的符号回答下列问题:
(1)写出A元素最高价氧化物与NaOH溶液反应的离子方程式
(2)B元素在元素周期表第
B的固态氧化物的晶体类型是
(3)D元素的原子结构示意图是:
(4)B元素与E元素的最高价氧化物的水化物的酸性强弱
(5)请用化学方程式表示E元素的单质在工业上的一种重要用途:
2010·山西太原·一模 查看更多[1]
(已下线)山西省太原五中2010届高三5月末考试试题理综化学
更新时间:2016-12-09 00:32:21
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,A元素的原子核内只有1个质子;B元素的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层多4;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C;C、E同主族。
(1)E元素形成的氧化物对应的水化物的化学式为_______________________________ 。
(2)元素C、D、E形成的简单离子半径大小关系是____________ (用离子符号表示)。
(3)用电子式表示化合物D2C的形成过程:_________________ 。C、D还可形成化合物D2C2,D2C2中含有的化学键类型是_______________________________________________ 。
(4)由A、B、C三种元素形成的离子化合物的化学式为__________________ ,它与强碱溶液共热,发生反应的离子方程式是______________________ 。
(5)某一反应体系中含有D2E、D2EC3、D2EC4三种物质,若此反应为分解反应,则此反应的化学方程式为________________________ (化学式用具体的元素符号表示)。
(1)E元素形成的氧化物对应的水化物的化学式为
(2)元素C、D、E形成的简单离子半径大小关系是
(3)用电子式表示化合物D2C的形成过程:
(4)由A、B、C三种元素形成的离子化合物的化学式为
(5)某一反应体系中含有D2E、D2EC3、D2EC4三种物质,若此反应为分解反应,则此反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D四种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E;D的L层电子数等于K、M两个电子层上的电子数之和。
(1)A为___________ , D ________ 。(填元素符号)
写出含有10个中子的B原子的核素符号_____________ 。
(2)C在周期表中的位置________________________ 。
(3)写出A、B的化合物与E反应的化学方程式:___________________________ 。
(4)A、D两元素的最高价氧化物的水化物酸性更强的是______________ (填化学式)。
(5)写出D的最高价氧化物对应的水化物和A反应的化学方程式:______________ 。
(1)A为
写出含有10个中子的B原子的核素符号
(2)C在周期表中的位置
(3)写出A、B的化合物与E反应的化学方程式:
(4)A、D两元素的最高价氧化物的水化物酸性更强的是
(5)写出D的最高价氧化物对应的水化物和A反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】下表中的实线表示元素周期表的部分边界。

(1)请在上表中用实线补出元素周期表的上边界。_____________
(2)某主族元素原子的核外电子排布为: ,该元素在元素周期表中的位置为
,该元素在元素周期表中的位置为_______________ 。
(3)元素I的非金属性________ (填“强于”或“弱于”)元素H,用原子结构的观点解释原因:同周期元素随着原子序数的递增,______________________ ,非金属性增强。设计实验证明元素E的金属性强于元素F:__________________________ 。
(4)处于周期表中对角线位置(左上方和右下方) 的元素,其性质具有相似性,称为“对角线规则”。元素D与F的单质及其化合物性质相似,如D、DO、D(OH)2与NaOH溶液都能反应生成Na2DO2等物质。回答下列问题。
①写出F的单质与氢氧化钠溶液反应的离子方程式___________________________ 。
②鉴别元素D与E的氢氧化物可用试剂是_________________ 。

(1)请在上表中用实线补出元素周期表的上边界。
(2)某主族元素原子的核外电子排布为:
 ,该元素在元素周期表中的位置为
,该元素在元素周期表中的位置为(3)元素I的非金属性
(4)处于周期表中对角线位置(左上方和右下方) 的元素,其性质具有相似性,称为“对角线规则”。元素D与F的单质及其化合物性质相似,如D、DO、D(OH)2与NaOH溶液都能反应生成Na2DO2等物质。回答下列问题。
①写出F的单质与氢氧化钠溶液反应的离子方程式
②鉴别元素D与E的氢氧化物可用试剂是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、E、F、G是核电荷数依次增大的短周期主族元素,A的一种核素的原子核内无中子,B的一种核素被考古学家用于测定文物的年代,D原子的最外层电子数比次外层多4,D的阴离子与E的阳离子具有相同的电子排布,两元素可形成化合物E2D,D、F同主族。用化学用语回答下列问题:
(1)D在元素周期表中的位置为___________ 。
(2)G的离子结构示意图为___________ 。
(3)E、F、G三种元素所形成的简单离子,半径由大到小的顺序为___________ 。
(4)由A、C、D三元素按原子个数4:2:3之比形成物质的化学式为___________ ,其中所含化学键的类型有___________ 。
(5)B、D、F可形成一个三原子分子,且每个原子均达到8电子稳定结构,则该分子的结构式为___________ 。
(6)下列实验操作对应的实验现象中,不正确的是___________ 。
(1)D在元素周期表中的位置为
(2)G的离子结构示意图为
(3)E、F、G三种元素所形成的简单离子,半径由大到小的顺序为
(4)由A、C、D三元素按原子个数4:2:3之比形成物质的化学式为
(5)B、D、F可形成一个三原子分子,且每个原子均达到8电子稳定结构,则该分子的结构式为
(6)下列实验操作对应的实验现象中,不正确的是
| 选项 | 实验操作 | 实验现象 |
| A | 将E单质投入到 溶液中 溶液中 | 有红色固体析出 |
| B | 向 溶液中通入过量C的气态氢化物 溶液中通入过量C的气态氢化物 | 先产生白色沉淀,后沉淀溶解 |
| C | 将G的单质通入到 溶液中充分反应后,加入四氯化碳,振荡,静置 溶液中充分反应后,加入四氯化碳,振荡,静置 | 下层溶液变为橙色 |
| D | 过量B的最高价氧化物通入到饱和 溶液中 溶液中 | 有白色晶体析出 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、E五种元素均是短周期的主族元素,原子序数依次增大。B、E原子的最外层电子数均为其电子层数的两倍,D、E元素原子的最外层电子数相等。X、Y、Z、W均由上述元素的两种元素组成,甲、乙均由上述元素的三种元素组成。元素B形成的单质M与甲、乙均能反应(相对分子质量甲<乙)。转化关系如图(反应条件略去)。请回答下列问题:
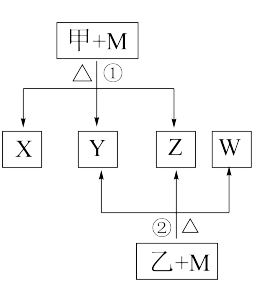
(1)X、Y、Z、W属于同一类物质,这类化合物可称为_____________ ;X、Y、W都能与Z反应,则Z为_____________ (写化学式)。
(2)写出M与甲的浓溶液、M与乙的浓溶液加热时反应的化学方程式:
①______________________ ;②__________________ 。
(3)化合物BE2与化合物Y结构相似,则BE2的电子式为_____________ 。
(4)上述六种化合物中________ 是空气质量日报必须分析测定的物质,他们的危害是________ 。(写一种及对应危害即可)
(5)将X、W与D按1:1:n通入Z中,充分反应后无气体剩余或生成,写出反应的化学方程式________ 。

(1)X、Y、Z、W属于同一类物质,这类化合物可称为
(2)写出M与甲的浓溶液、M与乙的浓溶液加热时反应的化学方程式:
①
(3)化合物BE2与化合物Y结构相似,则BE2的电子式为
(4)上述六种化合物中
(5)将X、W与D按1:1:n通入Z中,充分反应后无气体剩余或生成,写出反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】现有A、B、C、D、E、F、G七种短周期主族元素,其原子序数依次增大。已如A、D位于同一主族,D是短周期中原子半径最大的。B、E最外层电子数是最内层电子数的2倍。C、F的最外层电子数相等,且C、F的原子序数之和为A、D原子序数之和的两倍。
(1)A、C、D、F形成的简单离子半径由大到小的顺序是____________ (用元素符号填写)。
(2)B、E、F、G最高价氧化物对应的水化物酸性最强的是___________ (用化学式填写)。
(3)由C、D两元素能形成一种原子个数比为1:1的化合物,该化合物所含的化学键类型有____________ 。
(4)下列事实能说明G元素的非金属性比F元素的非金属性强的是______________ 。
a. G单质与Na2S溶液反应溶液变浑浊
b. F氢化物的酸性比G的氢化物酸性弱
c. G和F两元素的简单氢化物受热分解,前者的分解温度高
(5)A、C、D、F四种元素形成的化合物M和N在溶液中相互反应的离子方程式是________________ 。
(1)A、C、D、F形成的简单离子半径由大到小的顺序是
(2)B、E、F、G最高价氧化物对应的水化物酸性最强的是
(3)由C、D两元素能形成一种原子个数比为1:1的化合物,该化合物所含的化学键类型有
(4)下列事实能说明G元素的非金属性比F元素的非金属性强的是
a. G单质与Na2S溶液反应溶液变浑浊
b. F氢化物的酸性比G的氢化物酸性弱
c. G和F两元素的简单氢化物受热分解,前者的分解温度高
(5)A、C、D、F四种元素形成的化合物M和N在溶液中相互反应的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D为原子序数依次增大短周期元素,A的最外层电子数是其电子层数2倍;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E;D的L层电子数等于其它电子层上的电子数之和。
(1)A元素名称为______ ,D在周期表中的位置________ ,离子半径大小B___ C(填“>”“<”或“=”)。
(2)B的两种单质在常温下都是气体,它们互为____________ 。比较B的氢化物和D的氢化物沸点:B___ D(填“>”“<”或“=”),原因是_________________ 。
(3)E中含有化学键类型:_________ ,属于___________ 化合物(填“离子化合物”或“共价化合物”)。
(4)用电子式表示C与D的二元化合物的形成过程:_____________________ 。
(5)氢原子与B分别形成10电子和18电子分子,写出18电子分子转化成10电子分子的化学方程式__________________ 。
(1)A元素名称为
(2)B的两种单质在常温下都是气体,它们互为
(3)E中含有化学键类型:
(4)用电子式表示C与D的二元化合物的形成过程:
(5)氢原子与B分别形成10电子和18电子分子,写出18电子分子转化成10电子分子的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、E为元素周期表中原子序数依次增大的短周期主族元素,X、Y、Z分别为B、C、E对应的单质,甲、乙 、丙、丁为其中部分元素组成的化合物,其中C、D同主族,甲是一种能使湿润的红色石蕊试纸变蓝的气体,甲可用于检验Z气体是否泄漏。上述物质间的转化关系如图所示:
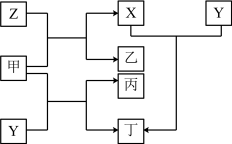
(1)B、C、D、E四种元素形成的简单离子中,离子半径由小到大的顺序是___ (用化学用语表示)。
(2)下列事实能说明D元素的非金属性小于E的是___
a.对应氢化物的还原性:D>E
b.D和E两元素的简单氢化物受热分解,后者的分解温度高
c.单质的沸点:D>E
(3)已知元素Ts位于第七周期,与E同族,写出其中子数为176的核素符号___ ,预测Ts及其化合物最不可能具有的性质是___ 。
a.单质易溶于某些有机溶剂 b.单质是有色固体
c.氢化物很稳定 d.简单阴离子可与Ag+形成难溶物
(4)A、B两种元素可组成一种离子化合物BA5,该化合物的电子式为___ 。
(5)A、B、D三种元素组成离子化合物W,已知:
①1molW能与足量氢氧化钠溶液共热,生成22.4L气体(标准状况);
②W能与盐酸反应产生一种臭鸡蛋气味的气体。则W是___ ,写出①的离子方程式___ 。

(1)B、C、D、E四种元素形成的简单离子中,离子半径由小到大的顺序是
(2)下列事实能说明D元素的非金属性小于E的是
a.对应氢化物的还原性:D>E
b.D和E两元素的简单氢化物受热分解,后者的分解温度高
c.单质的沸点:D>E
(3)已知元素Ts位于第七周期,与E同族,写出其中子数为176的核素符号
a.单质易溶于某些有机溶剂 b.单质是有色固体
c.氢化物很稳定 d.简单阴离子可与Ag+形成难溶物
(4)A、B两种元素可组成一种离子化合物BA5,该化合物的电子式为
(5)A、B、D三种元素组成离子化合物W,已知:
①1molW能与足量氢氧化钠溶液共热,生成22.4L气体(标准状况);
②W能与盐酸反应产生一种臭鸡蛋气味的气体。则W是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】有四种短周期元素,它们的结构、性质等信息如下表所述:
请根据表中信息填写:
(1)A原子的外围电子排布式__________________________________ 。
(2)B元素在周期表中的位置________ ;离子半径:B________ A(填“大于”或“小于”)。
(3)C元素原子核外有________ 个未成对电子,能量最高的电子为________ 轨道上的电子,其轨道呈________ 形。
(4)D元素原子的价电子排布式为________ ,D-的结构示意图是________ 。
(5)B的最高价氧化物对应的水化物的化学式___________________ ,与A的最高价氧化物对应的水化物相比,碱性较强的是:_______________ (填化学式)。
| 元素 | 结构、性质等信息 |
| A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
| B | B与A同周期,其最高价氧化物的水化物呈两性 |
| C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
(1)A原子的外围电子排布式
(2)B元素在周期表中的位置
(3)C元素原子核外有
(4)D元素原子的价电子排布式为
(5)B的最高价氧化物对应的水化物的化学式
您最近一年使用:0次



