对于反应3S+6KOH====2K2S+K2SO3+3H2O,下列说法正确的是
| A.是氧化剂,KOH是还原剂 |
| B.还原剂与氧化剂的质量比是2:1 |
| C.氧化产物和还原产物的物质的量之比为3:2 |
| D.若3mol硫完全反应,则反应中共转移了4mol电子 |
9-10高一下·广西南宁·期末 查看更多[1]
(已下线)2009—2010学年南宁二中高一下学期期末考试化学
更新时间:2016-12-09 00:43:35
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】 与浓硫酸在一定条件下可发生反应:
与浓硫酸在一定条件下可发生反应: (方程式未配平),下列说法正确的是
(方程式未配平),下列说法正确的是
 与浓硫酸在一定条件下可发生反应:
与浓硫酸在一定条件下可发生反应: (方程式未配平),下列说法正确的是
(方程式未配平),下列说法正确的是A.X为 | B. 既作氧化剂又作还原剂 既作氧化剂又作还原剂 |
| C.浓硫酸表现出了氧化性和酸性 | D. 发生反应时转移电子 发生反应时转移电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】古文献《余冬录》中对胡粉[主要成分为 ]制法的相关描述:“铅块悬酒缸内,封闭四十九日,开之则化为粉矣。化不白者(Pb),炒为黄丹(Pb3O4)。黄丹滓为密陀僧(PbO)”。下列说法错误的是
]制法的相关描述:“铅块悬酒缸内,封闭四十九日,开之则化为粉矣。化不白者(Pb),炒为黄丹(Pb3O4)。黄丹滓为密陀僧(PbO)”。下列说法错误的是
 ]制法的相关描述:“铅块悬酒缸内,封闭四十九日,开之则化为粉矣。化不白者(Pb),炒为黄丹(Pb3O4)。黄丹滓为密陀僧(PbO)”。下列说法错误的是
]制法的相关描述:“铅块悬酒缸内,封闭四十九日,开之则化为粉矣。化不白者(Pb),炒为黄丹(Pb3O4)。黄丹滓为密陀僧(PbO)”。下列说法错误的是| A.Pb3O4属于氧化物 |
| B.黄丹与盐酸反应只生成PbCl2和水 |
| C.铅块制胡粉的过程中发生了氧化还原反应 |
| D.密陀僧与一氧化碳高温加热可以制得铅 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
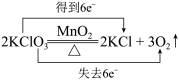
【推荐1】下列化学方程式中电子转移正确的是
A. |
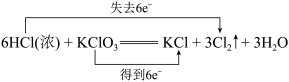
B.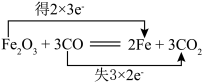 |
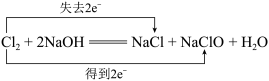
C.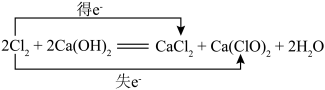 |
D.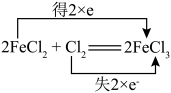 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在明代宋应星所著的《天工开物》中,记载有火法炼锌工艺。该工艺涉及的化学反应方程式为: 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是| A.在该反应中,ZnCO3做还原剂 |
B.该反应转移电子方向和数目是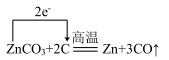 |
| C.在该反应中,单质C失去电子被氧化,发生氧化反应 |
| D.在该反应中,还原产物只有Zn |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知反应①、②、③分别为 和盐酸、硝酸、氢碘酸反应的离子方程式
和盐酸、硝酸、氢碘酸反应的离子方程式
①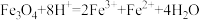
②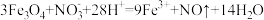
③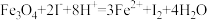
下列分析中正确的是
 和盐酸、硝酸、氢碘酸反应的离子方程式
和盐酸、硝酸、氢碘酸反应的离子方程式①
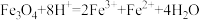
②
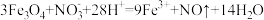
③
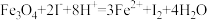
下列分析中正确的是
| A.反应①、②、③均为氧化还原反应 |
B.根据题中条件可判断氧化性的强弱关系为: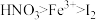 |
C.等质量的 参加反应时,反应②和③转移的电子数相同 参加反应时,反应②和③转移的电子数相同 |
D.向 溶液中通入少量氯气,反应的离子方程式: 溶液中通入少量氯气,反应的离子方程式: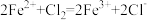 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】设 为阿伏加 德罗常数的值。化工厂常用浓氨水来检验氯气管道是否发生泄漏,其原理是:
为阿伏加 德罗常数的值。化工厂常用浓氨水来检验氯气管道是否发生泄漏,其原理是: 。下列说法正确的是
。下列说法正确的是
 为阿伏加 德罗常数的值。化工厂常用浓氨水来检验氯气管道是否发生泄漏,其原理是:
为阿伏加 德罗常数的值。化工厂常用浓氨水来检验氯气管道是否发生泄漏,其原理是: 。下列说法正确的是
。下列说法正确的是| A.如果氯气管道漏气,则会看到有大量白雾生成 |
B.反应中每形成 键,转移电子数为 键,转移电子数为 |
C. 的 的 溶液中, 溶液中, 的数目小于 的数目小于 |
D.该反应中,氧化剂与还原剂的物质的量之比为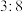 |
您最近一年使用:0次
【推荐1】向200 mL FeBr2溶液中逐渐通入Cl2,其中n(Fe 3+)、n(Br2) 随通入n(Cl2)的变化如图所示,下列说法不正确的是( )
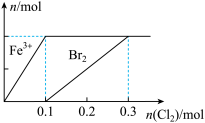

| A.氧化性强弱:Br2 > Fe3+ |
| B.由图可知,该FeBr2溶液的浓度为1 mol·L-1 |
| C.n(Cl2) =0. 12 mol时,溶液中的离子浓度有:c (Fe 3+)∶c( Br-)=1∶8 |
| D.n(FeBr2)∶n(Cl2) =1∶1时,反应的离子方程式为:2Fe2++2Br-+ 2Cl2=2Fe3++Br2 + 4Cl- |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】11.9g金属锡跟100mL12mol•L﹣1HNO3共热一段时间.完全反应后测定溶液中c(H+)为8mol•L﹣1,溶液体积仍为100mL.放出的气体在标准状况下体积约为8.96L.由此推断氧化产物可能是(Sn的相对原子质量为119)( )
| A.Sn(NO3)4 | B.Sn(NO3)2 | C.SnO2∙4H2O | D.SnO |
您最近一年使用:0次
【推荐3】将一定量的氯气通入50 mL10.00 mol/L的氢氧化钠浓溶液中,加热少许时间后,溶液中形成NaCl、NaClO、NaClO2共存体系(不考虑氯气和水的反应)。下列说法正确的是
| A.若反应中转移的电子为n mol,则0.25<n<0.5 |
| B.溶液中n(NaCl) :n(NaClO):n(NaCIO2)可能为3:1 :1 |
| C.与NaOH反应的氯气物质的量:0.25 mol<n(Cl2)<0. 75 mol |
D.当溶液中n(NaClO) :n(NaClO2)=5:1时,发生反应的离子方程式为7Cl2+14OH-=8Cl- +5ClO- +ClO +7H2O +7H2O |
您最近一年使用:0次

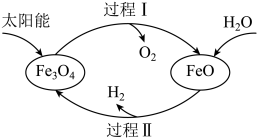
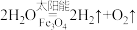
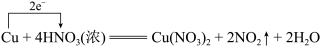
 ,含少量
,含少量 )时,生成的
)时,生成的 .下列说法正确的是
.下列说法正确的是 时,转移
时,转移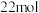 电子
电子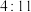
 的硫酸吸收
的硫酸吸收

