将1 mol氧气和一定量的HCl放入2L的密闭容器中,420℃时,在催化剂作用下发生反应:4HCl+O2 2Cl2+2H2O。5分钟后反应达到平衡,将容器中的混合气体通过过量NaOH溶液,消耗NaOH 2.0 mol;再将剩余气体干燥后通过焦性没食子酸的碱性溶液吸收O2,溶液增重19.2 g。
2Cl2+2H2O。5分钟后反应达到平衡,将容器中的混合气体通过过量NaOH溶液,消耗NaOH 2.0 mol;再将剩余气体干燥后通过焦性没食子酸的碱性溶液吸收O2,溶液增重19.2 g。
请回答下列问题:
(1)写出平衡时,混合气体通入NaOH溶液中所发生反应的离子方程式为_________ 。
(2)计算0~5分钟时,Cl2的平均生成速率是________ 。
(3)计算平衡时HCl的转化率是________ 。
 2Cl2+2H2O。5分钟后反应达到平衡,将容器中的混合气体通过过量NaOH溶液,消耗NaOH 2.0 mol;再将剩余气体干燥后通过焦性没食子酸的碱性溶液吸收O2,溶液增重19.2 g。
2Cl2+2H2O。5分钟后反应达到平衡,将容器中的混合气体通过过量NaOH溶液,消耗NaOH 2.0 mol;再将剩余气体干燥后通过焦性没食子酸的碱性溶液吸收O2,溶液增重19.2 g。请回答下列问题:
(1)写出平衡时,混合气体通入NaOH溶液中所发生反应的离子方程式为
(2)计算0~5分钟时,Cl2的平均生成速率是
(3)计算平衡时HCl的转化率是
9-10高一下·江苏扬州·期末 查看更多[1]
(已下线)09—10年扬州中学高一下学期期末考试化学卷
更新时间:2016-12-09 00:45:14
|
相似题推荐
计算题
|
较难
(0.4)
解题方法
【推荐1】一定量的氢气在氯气中充分燃烧,所得混合物用200mL 2.00mo/L的NaOH溶液(密度为1.12g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.05mol。
(1)求所得溶液中Cl-的物质的量_____ 。
(2)求原混合气体中氯气和氢气的物质的量之比_____ 。
(1)求所得溶液中Cl-的物质的量
(2)求原混合气体中氯气和氢气的物质的量之比
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐2】(1)有镁和铁的混合物共4.0克,与200毫升盐酸恰好完全反应,在标准状况下共收集到2.24L气体。假设反应后溶液体积不变,则铁的质量为_____ g;反应后溶液中Mg2+的物质的量浓度为_______ 。
(2)一定量氢气在氯气中燃烧,所得混合气体用 100 mL、2.00 moL·L-1NaOH 溶液恰好完全吸收,测得溶液中含有 NaClO 的物质的量为 0.05mol。试计算下列问题: 所得溶液中 Cl-的物质的量为_______ ;所用氯气和参加反应的氢气的物质的量之比n(C12):n(H2)为 _______ 。
(2)一定量氢气在氯气中燃烧,所得混合气体用 100 mL、2.00 moL·L-1NaOH 溶液恰好完全吸收,测得溶液中含有 NaClO 的物质的量为 0.05mol。试计算下列问题: 所得溶液中 Cl-的物质的量为
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
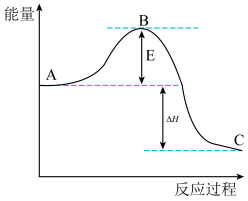
【推荐1】合成氨反应N2(g)+3H2(g) 2NH3(g),反应过程的能量变化如图所示。已知N2(g)与H2(g)反应生成17 g NH3(g),放出46.1 kJ的热量。
2NH3(g),反应过程的能量变化如图所示。已知N2(g)与H2(g)反应生成17 g NH3(g),放出46.1 kJ的热量。
请回答下列问题:
(1)该反应通常用铁作催化剂,加催化剂会使图中E变_____ (填“大”或“小”),E的大小对该反应的反应热有无影响?________ 。
(2)起始充入2mol·L-1 N2和5.5 mol·L-1 H2,经过50 min,NH3的浓度为1mol·L-1,则v(N2)=_____ 。
(3)已知NH3(g)= NH3 (l) ΔH=-Q kJ·mol-1,则N2(g)+3H2(g)= 2NH3 (l)的∆H=_________ 。
 2NH3(g),反应过程的能量变化如图所示。已知N2(g)与H2(g)反应生成17 g NH3(g),放出46.1 kJ的热量。
2NH3(g),反应过程的能量变化如图所示。已知N2(g)与H2(g)反应生成17 g NH3(g),放出46.1 kJ的热量。
请回答下列问题:
(1)该反应通常用铁作催化剂,加催化剂会使图中E变
(2)起始充入2mol·L-1 N2和5.5 mol·L-1 H2,经过50 min,NH3的浓度为1mol·L-1,则v(N2)=
(3)已知NH3(g)= NH3 (l) ΔH=-Q kJ·mol-1,则N2(g)+3H2(g)= 2NH3 (l)的∆H=
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐2】一定温度下,将3mol A气体和1mol B气体通入一密闭容器中,发生如下反应:3A(g)+B (g) xC(g)。请填写下列空白:
xC(g)。请填写下列空白:
(1)若容器体积固定为2L,反应1min时测得剩余1.8molA,C的浓度为0.4 mol·L-1。
①则1min内,B的平均反应速率为_____ ,x=____ ;
②若反应经2min达到平衡,平衡时C的浓度____ 0.8 mol·L-1(填“>”、“=”或“<”);
③若平衡混合物中C的体积分数为25%,则A的转化率是_____ ;
④若改变起始物质的加入量,欲使反应达到平衡时C的物质的量分数与原平衡相等,则起始加入的三种物质的物质的量n(A)、n(B)、n(C)之间应满足的条件____ (可用两个方程表示,其中一个用n(A)和 n(C),另一个用n(B)和n(C)表示)。
(2)若维持容器压强不变。
①达到平衡时C的体积分数______ 25%,(填“大于”、“等于”或“小于”);
②若改变起始物质的加入量,欲使反应达到平衡时C的物质的量是原平衡的2倍,则应加入_____ molA气体和_____ molB气
 xC(g)。请填写下列空白:
xC(g)。请填写下列空白:(1)若容器体积固定为2L,反应1min时测得剩余1.8molA,C的浓度为0.4 mol·L-1。
①则1min内,B的平均反应速率为
②若反应经2min达到平衡,平衡时C的浓度
③若平衡混合物中C的体积分数为25%,则A的转化率是
④若改变起始物质的加入量,欲使反应达到平衡时C的物质的量分数与原平衡相等,则起始加入的三种物质的物质的量n(A)、n(B)、n(C)之间应满足的条件
(2)若维持容器压强不变。
①达到平衡时C的体积分数
②若改变起始物质的加入量,欲使反应达到平衡时C的物质的量是原平衡的2倍,则应加入
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐3】CH3OH是一种重要的化工原料,广泛应用于化工生产,根据所学回答下列问题:
(1)工业上制备甲醇的反应方程式为: ,某温度下,将1molCO2和3molH2充入体积不变的2L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下表:
,某温度下,将1molCO2和3molH2充入体积不变的2L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下表:
①写出该反应体系中CO2的电子式___________ 。
②用H2表示前2h的平均反应速率v(H2)=___________ 。
③该温度下,CO2的平衡转化率为___________ 。
④在一定条件下,下列说法能说明该可逆反应达到平衡状态的是___________ (填字母)。
A.容器中气体密度不变 B.容器中气体平均摩尔质量不变
C. D.形成2molC=O键同时断裂3molH-H键
D.形成2molC=O键同时断裂3molH-H键
⑤在温度为T,压强为P的条件下,将CO2和H2按物质的量之比1∶3通入一恒压密闭容器中发生上述反应,达到平衡时,测得CO2的平衡转化率为50%,则该反应条件下的平衡常数为
___________ (用含P的表达式表示,其中用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(2)CH3OH制备丙烯的反应为: ,速率常数k与反应温度T的关系遵循Arrhenius方程,已知Arrhenius方程为:
,速率常数k与反应温度T的关系遵循Arrhenius方程,已知Arrhenius方程为: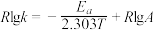 (其中k为速率常数,反应速率与其成正比;
(其中k为速率常数,反应速率与其成正比; 为活化能:
为活化能: ,A为常数)。
,A为常数)。

①在一定条件下,测得实验数据如上图曲线a所示。则该条件下,反应的活化能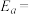
___________ 
②若实验时改变外界条件,测得实验数据为如上图曲线b所示,则可能改变的外界条件是___________ (填标号)
A.升高温度 B.增大压强 C.增大 D.更换适宜的催化剂
D.更换适宜的催化剂
(1)工业上制备甲醇的反应方程式为:
 ,某温度下,将1molCO2和3molH2充入体积不变的2L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下表:
,某温度下,将1molCO2和3molH2充入体积不变的2L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下表:| 时间/h | l | 2 | 3 | 4 | 5 | 6 |
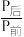 | 0.90 | 0.85 | 0.83 | 0.81 | 0.80 | 0.80 |
②用H2表示前2h的平均反应速率v(H2)=
③该温度下,CO2的平衡转化率为
④在一定条件下,下列说法能说明该可逆反应达到平衡状态的是
A.容器中气体密度不变 B.容器中气体平均摩尔质量不变
C.
 D.形成2molC=O键同时断裂3molH-H键
D.形成2molC=O键同时断裂3molH-H键⑤在温度为T,压强为P的条件下,将CO2和H2按物质的量之比1∶3通入一恒压密闭容器中发生上述反应,达到平衡时,测得CO2的平衡转化率为50%,则该反应条件下的平衡常数为

(2)CH3OH制备丙烯的反应为:
 ,速率常数k与反应温度T的关系遵循Arrhenius方程,已知Arrhenius方程为:
,速率常数k与反应温度T的关系遵循Arrhenius方程,已知Arrhenius方程为: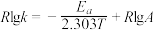 (其中k为速率常数,反应速率与其成正比;
(其中k为速率常数,反应速率与其成正比; 为活化能:
为活化能: ,A为常数)。
,A为常数)。
①在一定条件下,测得实验数据如上图曲线a所示。则该条件下,反应的活化能
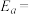

②若实验时改变外界条件,测得实验数据为如上图曲线b所示,则可能改变的外界条件是
A.升高温度 B.增大压强 C.增大
 D.更换适宜的催化剂
D.更换适宜的催化剂
您最近一年使用:0次
【推荐1】甲烷和水蒸气催化制氢主要有如下两个反应:
①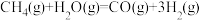 ΔH=+206kJ/mol
ΔH=+206kJ/mol
②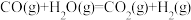 ΔH=-41kJ/mol
ΔH=-41kJ/mol
恒定压强为100kPa时,将n(CH4)∶n(H2O)=1∶3的混合气体投入反应器中,平衡时,各组分的物质的量分数与温度的关系如图所示。

已知投料比为n(CH4)∶n(H2O)=1∶3的混合气体,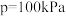 。600℃时,
。600℃时, 的平衡转化率为
的平衡转化率为_______ ,反应①的平衡常数的计算式为 =
=_______ ( 是以分压表示的平衡常数,分压=总压×物质的量分数)。
是以分压表示的平衡常数,分压=总压×物质的量分数)。
①
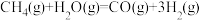 ΔH=+206kJ/mol
ΔH=+206kJ/mol②
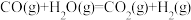 ΔH=-41kJ/mol
ΔH=-41kJ/mol恒定压强为100kPa时,将n(CH4)∶n(H2O)=1∶3的混合气体投入反应器中,平衡时,各组分的物质的量分数与温度的关系如图所示。

已知投料比为n(CH4)∶n(H2O)=1∶3的混合气体,
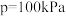 。600℃时,
。600℃时, 的平衡转化率为
的平衡转化率为 =
= 是以分压表示的平衡常数,分压=总压×物质的量分数)。
是以分压表示的平衡常数,分压=总压×物质的量分数)。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】设空气中N2、O2的体积分数分别为0.8和0.2。在沸腾炉中将硫铁矿用空气中充分煅烧: 4FeS2+11O2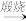 2Fe2O3+8SO2
2Fe2O3+8SO2
(1)所得气体中SO2的体积分数不超过_______ %(保留一位小数)。
(2)若从接触室出来的气体中SO2、O2、N2、SO3的体积比为0.5:1:20:x,则x=_______ ,此时反应中SO2的转化率为_______ %(保留一位小数)。
(3)在实际生产中,在接触室SO2与O2的体积比以1︰4较为适宜。若沸腾炉通入接触室的炉气中SO2、O2、N2的体积比为8:1:48,其流速为2.5m3/s, 则再往接触室里通入的空气的流速应为_______ m3/s(保留一位小数;气体体积在同温同压下测定)。
(4)从吸收塔出来的气体用一定量氨水吸收,得到的铵盐产品是(NH4)2SO3和NH4HSO3的混合物。取不同质量的铵盐,分别加入x mol/L的50.00mL NaOH溶液中,经沸水浴(此温度下铵盐自身不分解)加热使氨气全部逸出,干燥后用浓硫酸完全吸收。实验数据如下:
①该铵盐中(NH4)2SO3和NH4HSO3的物质的量之比为___________ 。
②试求x的值:________________
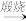 2Fe2O3+8SO2
2Fe2O3+8SO2 (1)所得气体中SO2的体积分数不超过
(2)若从接触室出来的气体中SO2、O2、N2、SO3的体积比为0.5:1:20:x,则x=
(3)在实际生产中,在接触室SO2与O2的体积比以1︰4较为适宜。若沸腾炉通入接触室的炉气中SO2、O2、N2的体积比为8:1:48,其流速为2.5m3/s, 则再往接触室里通入的空气的流速应为
(4)从吸收塔出来的气体用一定量氨水吸收,得到的铵盐产品是(NH4)2SO3和NH4HSO3的混合物。取不同质量的铵盐,分别加入x mol/L的50.00mL NaOH溶液中,经沸水浴(此温度下铵盐自身不分解)加热使氨气全部逸出,干燥后用浓硫酸完全吸收。实验数据如下:
| 实验次数 | 铵盐质量(g) | 浓硫酸增加的质量(g) |
| 第一次 | 1.570 | 0.340 |
| 第二次 | 3.140 | 0.680 |
| 第三次 | 4.710 | 0.510 |
| 第四次 | 6.280 | 0 |
①该铵盐中(NH4)2SO3和NH4HSO3的物质的量之比为
②试求x的值:
您最近一年使用:0次

 溶液恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500 mol。
溶液恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500 mol。



