关于化学反应速率的影响因素的说法中不正确的是
| A.改变压强,若不能引起浓度的变化,反应速率就不会受影响 |
| B.决定化学反应速率快慢的主要因素是反应物的性质 |
| C.任何一种加快反应速率的因素都是由于增加了活化分子的百分数 |
| D.反应速率加快的原因是有效碰撞次数增多 |
10-11高二上·江西九江·阶段练习 查看更多[1]
(已下线)2010年江西省九江一中高二上学期第一次月考(化学)
更新时间:2016-12-09 00:57:16
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列对化学反应速率增大原因的分析错误的是
| A.对有气体参加的化学反应,增大压强使容器容积减小,单位体积内活化分子数增多 |
| B.向反应体系中加入相同浓度的反应物,使活化分子百分数增大 |
| C.升高温度,使反应物分子中活化分子百分数增大 |
| D.加入适宜的催化剂,使反应物分子中活化分子百分数增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关化学反应原理的说法不正确的是
| A.强酸和强碱的中和反应的活化能接近于零,所以反应速率很高 |
| B.恒温恒容条件下加稀有气体,化学反应速率不变,化学平衡不移动 |
| C.过程的自发性既能用于判断过程的方向,也能用于判断过程发生的速率 |
| D.溶解度较小的BaSO4在一定条件下也可以转化为溶解度略大的BaCO3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】NO在催化剂条件下可被H2还原为无害物质,反应原理为:2H2(g) +2NO(g) N2(g)+2H2O(g) △H.在恒容密闭容器中按n(NO)∶n(H2)=1∶1充入,在不同温度下发生该反应,测得平衡时混合气体的平均相对分子质量(M)与温度(T)的关系如图所示。下列说法正确的是
N2(g)+2H2O(g) △H.在恒容密闭容器中按n(NO)∶n(H2)=1∶1充入,在不同温度下发生该反应,测得平衡时混合气体的平均相对分子质量(M)与温度(T)的关系如图所示。下列说法正确的是

 N2(g)+2H2O(g) △H.在恒容密闭容器中按n(NO)∶n(H2)=1∶1充入,在不同温度下发生该反应,测得平衡时混合气体的平均相对分子质量(M)与温度(T)的关系如图所示。下列说法正确的是
N2(g)+2H2O(g) △H.在恒容密闭容器中按n(NO)∶n(H2)=1∶1充入,在不同温度下发生该反应,测得平衡时混合气体的平均相对分子质量(M)与温度(T)的关系如图所示。下列说法正确的是 
| A.正反应活化能大于逆反应活化能 |
| B.增大压强,平衡正向移动,平衡常数增大 |
| C.a点平衡体系中氮气的体积分数为25% |
| D.逆反应速率:b>c |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】化学反应的方向和化学反应速率的研究可以指导化工生产。下列观点正确的是
A.2H2O 2H2↑+O2↑与2H2+O2 2H2↑+O2↑与2H2+O2 2H2O互为可逆反应 2H2O互为可逆反应 |
| B.向新制氯水中加入少量石灰石固体可提高其漂白能力 |
| C.向稀氨水中加入少量水,溶液的导电能力增强 |
D.恒容密闭容器中发生反应4NH3+5O2 4NO+6H2O,充入少量N2可加快反应速率 4NO+6H2O,充入少量N2可加快反应速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】二氧化硫是一种重要的化工原料,可以制取硫酸、焦亚硫酸钠等化工产品。其中,催化制取三氧化硫的热化学方程式为: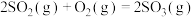 △H=-196.6 kJ·mol
△H=-196.6 kJ·mol 。二氧化硫也是形成酸雨的主要污染物,可以通过氨气水溶液进行吸收。实验室可以用浓硫酸与铜加热制取少量二氧化硫。关于二氧化硫转化成三氧化硫的反应,在恒温恒压的密闭容器中进行时,下列说法正确的是
。二氧化硫也是形成酸雨的主要污染物,可以通过氨气水溶液进行吸收。实验室可以用浓硫酸与铜加热制取少量二氧化硫。关于二氧化硫转化成三氧化硫的反应,在恒温恒压的密闭容器中进行时,下列说法正确的是
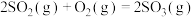 △H=-196.6 kJ·mol
△H=-196.6 kJ·mol 。二氧化硫也是形成酸雨的主要污染物,可以通过氨气水溶液进行吸收。实验室可以用浓硫酸与铜加热制取少量二氧化硫。关于二氧化硫转化成三氧化硫的反应,在恒温恒压的密闭容器中进行时,下列说法正确的是
。二氧化硫也是形成酸雨的主要污染物,可以通过氨气水溶液进行吸收。实验室可以用浓硫酸与铜加热制取少量二氧化硫。关于二氧化硫转化成三氧化硫的反应,在恒温恒压的密闭容器中进行时,下列说法正确的是| A.该反应中,反应物的键能之和<产物的键能之和 |
B.反应中每充入2 mol SO2和1 mol O2,充分反应后转移电子数目为 |
C.使用优质催化剂,体系中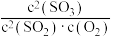 的值增大 的值增大 |
| D.升高温度,能加快反应速率,提高二氧化硫的平衡转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
| A.增大反应物的浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增加 |
B. 、 、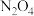 平衡混合气体加压后颜色加深,能用勒夏特列原理解释 平衡混合气体加压后颜色加深,能用勒夏特列原理解释 |
| C.化学反应的实质是活化分子有合适取向时的有效碰撞 |
| D.当反应达化学平衡时,各组分浓度相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在一氧化碳变换反应CO + H2O CO2 + H2中,有关反应条件改变使反应速率增大的原因分析
CO2 + H2中,有关反应条件改变使反应速率增大的原因分析不正确 的是
 CO2 + H2中,有关反应条件改变使反应速率增大的原因分析
CO2 + H2中,有关反应条件改变使反应速率增大的原因分析| A.使用催化剂,活化分子百分数增大,有效碰撞几率增加 |
| B.升高温度,活化分子百分数增大,有效碰撞几率增加 |
| C.增大压强,单位体积内活化分子数增多,有效碰撞几率增加 |
| D.增大c(CO),活化分子百分数增大,有效碰撞几率增加 |
您最近一年使用:0次

 标注。下列说法正确的是
标注。下列说法正确的是


