[Zn(CN)4]2–在水溶液中与HCHO发生如下反应:
4HCHO+[Zn(CN)4]2–+4H++4H2O===[Zn(H2O)4]2++4HOCH2CN
(1)Zn2+基态核外电子排布式为____________________ 。
(2)1 mol HCHO分子中含有σ键的数目为____________ mol。
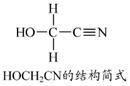
(3)HOCH2CN分子中碳原子轨道的杂化类型是______________ 。
(4)与H2O分子互为等电子体的阴离子为________________ 。
(5)[Zn(CN)4]2–中Zn2+与CN–的C原子形成配位键。不考虑空间构型,[Zn(CN)4]2–的结构可用示意图表示为_____________ 。
4HCHO+[Zn(CN)4]2–+4H++4H2O===[Zn(H2O)4]2++4HOCH2CN
(1)Zn2+基态核外电子排布式为
(2)1 mol HCHO分子中含有σ键的数目为
(3)HOCH2CN分子中碳原子轨道的杂化类型是
(4)与H2O分子互为等电子体的阴离子为
(5)[Zn(CN)4]2–中Zn2+与CN–的C原子形成配位键。不考虑空间构型,[Zn(CN)4]2–的结构可用示意图表示为

2016·江苏·高考真题 查看更多[10]
河南省安阳市汤阴县第一中学2019-2020学年高二下学期4月月考化学试卷山西省忻州市岢岚县中学2020-2021学年高二下学期4月月考化学试题四川省乐山沫若中学2020-2021学年高二上学期第一次月考化学试题江苏省启东中学2020-2021学年高二上学期期初考试化学试题天津市南开中学2020届高三教学质量监测理科综合化学部分2020届湖南省长沙市礼雅中学高中毕业班四月份网络教学质量监测卷理科综合化学部分山东省泰安市新泰市第二中学2019-2020学年高二下期中考试化学试题第2章 化学键与分子间作用力——C挑战区模拟高考(鲁科版选修3)2016年全国普通高等学校招生统一考试化学(江苏卷参考版)2016年全国普通高等学校招生统一考试化学(江苏卷精编版)
更新时间:2016-12-09 16:08:29
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF3气体和BN,如图所示:

请回答下列问题:
(1)由B2O3、CaF2和H2SO4制备BF3的化学方程式为_______ ;
(2)在BF3分子中,F-B-F的键角是_______ ,B原子的杂化轨道类型为_______ ,BF3和过量NaF作用可生成NaBF4,BF 的立体构型为
的立体构型为_______ ;与BF 互为等电子体的分子的化学式为
互为等电子体的分子的化学式为_______ (写一种)。

请回答下列问题:
(1)由B2O3、CaF2和H2SO4制备BF3的化学方程式为
(2)在BF3分子中,F-B-F的键角是
 的立体构型为
的立体构型为 互为等电子体的分子的化学式为
互为等电子体的分子的化学式为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)NH3分子中氮原子的轨道杂化类型是___________ ;C、N、O元素的第一电离能由大到小的顺序为___________ 。
(2)与NH 互为等电子体的一种分子为
互为等电子体的一种分子为___________ (填化学式)。
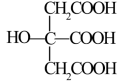
(3)柠檬酸的结构简式见图。1 mol柠檬酸分子中碳原子与氧原子形成的σ键的数目为___________ mol。
(2)与NH
 互为等电子体的一种分子为
互为等电子体的一种分子为(3)柠檬酸的结构简式见图。1 mol柠檬酸分子中碳原子与氧原子形成的σ键的数目为

您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氮及其化合物在生产、生活和科技等方面有重要的应用。请回答下列问题:
(1)氮元素基态原子的价电子排布图为______________ 。
(2)在氮分子中,氮原子之间存在着______ 个σ键和______ 个π键。
(3)叠氮酸(HN3)是一种弱酸,可部分电离出H+和N3﹣,请写出两种与N3﹣互为等电子体的分子_______ 、_______ 。
(4)氮元素的氢化物(NH3)是一种易液化的气体,请阐述原因是_____________________ 。
(5)NF3、NCl3、NBr3的沸点由高到低的顺序是___________________________ 。
(6)Mg3N2遇水发生剧烈反应,生成一种有刺激性气味的气体.该反应的化学方程式为_______ 。
(1)氮元素基态原子的价电子排布图为
(2)在氮分子中,氮原子之间存在着
(3)叠氮酸(HN3)是一种弱酸,可部分电离出H+和N3﹣,请写出两种与N3﹣互为等电子体的分子
(4)氮元素的氢化物(NH3)是一种易液化的气体,请阐述原因是
(5)NF3、NCl3、NBr3的沸点由高到低的顺序是
(6)Mg3N2遇水发生剧烈反应,生成一种有刺激性气味的气体.该反应的化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】硼、磷元素在化学中有很重要的地位,硼、磷及其化合物广泛应用于开发新型储氢材料、超导材料、富燃料材料、复合材料等高新材料领域。回答下列问题。
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得.
①基态Ti3+的未成对电子数有___ 个。
②LiBH4由Li+和BH4-构成,BH4-呈正四面体构型。LiBH4中不存在的作用力有___ (填标号)
A.离子键 B.共价键 C.金属键 D.配位键
(2)氨硼烷(NH3BH3)是一种新型储氢材料,其分子中存在配位键,则氨硼烷分子结构式为____ ,写出一种与氨硼烷互为等电子体的分子___ (填化学式)。
(3)硼酸(H3BO3)是一种片层状结构白色晶体,层内的H3BO3分子间通过氢键相连[如图]。
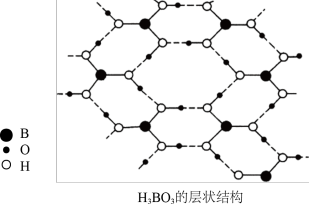
读图分析1mol H3BO3的晶体中有___ mol氢键。
(4)四(三苯基膦)钯分子结构如图:
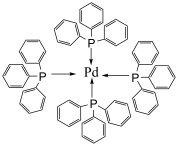
P原子以正四面体的形态围绕在钯原子中心上,钯原子的杂化轨道类型为___ ;判断该物质在水中___ (填写“易溶”或者“难溶”),并加以解释____ 。
(5)硼氢化钠是一种常用的还原剂。其晶胞结构如图所示:
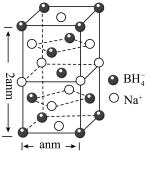
①该晶体中Na+的配位数为___ 。
②已知硼氢化钠晶体的密度为ρg/cm3,NA代表阿伏加 德罗常数的值,则a=___ (用含ρ、NA的最简式子表示)
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得.
①基态Ti3+的未成对电子数有
②LiBH4由Li+和BH4-构成,BH4-呈正四面体构型。LiBH4中不存在的作用力有
A.离子键 B.共价键 C.金属键 D.配位键
(2)氨硼烷(NH3BH3)是一种新型储氢材料,其分子中存在配位键,则氨硼烷分子结构式为
(3)硼酸(H3BO3)是一种片层状结构白色晶体,层内的H3BO3分子间通过氢键相连[如图]。

读图分析1mol H3BO3的晶体中有
(4)四(三苯基膦)钯分子结构如图:

P原子以正四面体的形态围绕在钯原子中心上,钯原子的杂化轨道类型为
(5)硼氢化钠是一种常用的还原剂。其晶胞结构如图所示:

①该晶体中Na+的配位数为
②已知硼氢化钠晶体的密度为ρg/cm3,NA代表阿伏加 德罗常数的值,则a=
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】对氨基苯甲酸和邻氨基苯甲酸分别用于防晒剂和制造药物,某小组以甲苯为主要原料进行合成,设计流程如下图。
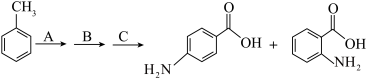
已知:i.羧基使苯环上与羧基处于间位的氢原子易被取代
ii .苯胺中的氨基易被氧化
iii.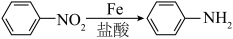
(1)基态N原子的电子有___________ 种运动状态。
(2)氨基苯甲酸中C=O中O原子的杂化方式是___________ 。
(3)组成氨基苯甲酸的4种元素的电负性由大到小的顺序是___________ 。
(4)对氨基苯甲酸和邻氨基苯甲酸的沸点分别是339.9℃和311.9℃,沸点不同的原因是___________ 。
(5)甲同学认为邻氨基苯甲酸可以形成“内盐”,请从化学键的角度解释“内盐”中离子键的形成过程___________ 。
(6)步骤A的反应条件___________ ;步骤C中生成1 mol对氨基苯甲酸电子转移___________ mol。

已知:i.羧基使苯环上与羧基处于间位的氢原子易被取代
ii .苯胺中的氨基易被氧化
iii.
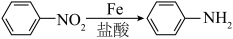
(1)基态N原子的电子有
(2)氨基苯甲酸中C=O中O原子的杂化方式是
(3)组成氨基苯甲酸的4种元素的电负性由大到小的顺序是
(4)对氨基苯甲酸和邻氨基苯甲酸的沸点分别是339.9℃和311.9℃,沸点不同的原因是
(5)甲同学认为邻氨基苯甲酸可以形成“内盐”,请从化学键的角度解释“内盐”中离子键的形成过程
(6)步骤A的反应条件
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知H和O可以形成H2O和H2O2两种化合物,试根据有关信息完成下列问题:
(1)水是维持生命活动所必需的一种物质。
①H2O内的O—H、水分子间的范德华力和氢键,从强到弱依次为____ 。
②用球棍模型表示的水分子结构是____ 。____ 杂化。H3O+中的H—O—H键角比H2O中的____ 。
(2)已知H2O2分子的结构如图所示:H2O2分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角93°52′,而两个O—H键与O—O键的夹角均为96°52′。
①H2O2分子的电子式是___ ,结构式是___ 。
②H2O2分子是含有___ 键和___ 键的___ (填“极性”或“非极性”)分子。
③H2O2能与水混溶,却不溶于CCl4。请予以解释:___ 。
(1)水是维持生命活动所必需的一种物质。
①H2O内的O—H、水分子间的范德华力和氢键,从强到弱依次为
②用球棍模型表示的水分子结构是

(2)已知H2O2分子的结构如图所示:H2O2分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角93°52′,而两个O—H键与O—O键的夹角均为96°52′。

①H2O2分子的电子式是
②H2O2分子是含有
③H2O2能与水混溶,却不溶于CCl4。请予以解释:
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】Cu可形成多种配合物,某同学在探究配合物的形成时做了以下实验,根据下列信息回答问题:
(1)向盛有硫酸铜水溶液的试管里逐滴加入氨水,首先出现蓝色沉淀,继续滴加氨水,蓝色沉淀溶解,得到深蓝色的透明溶液,请写出先后发生反应的离子方程式_______ 。
(2)再向深蓝色透明溶液加入乙醇,析出深蓝色的晶体。深蓝色晶体的化学式为_______ 。
(3)根据以上实验过程,判断NH3和H2O与Cu2+的配位能力:NH3_______ (填“>”“=”或“<”)H2O。
(4)已知Ti3+可形成配位数为6,颜色不同的两种配合物晶体,一种为紫色,另一种为绿色。两种晶体的组成皆为TiCl3·6H2O。为测定这两种晶体的化学式,某同学设计了如下实验:
a、分别取等质量的两种配合物晶体的样品配成待测溶液;
b、分别往待测溶液中滴入AgNO3溶液,均产生白色沉淀;
c、沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水溶液与AgNO3溶液反应得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的 。绿色晶体配合物的化学式为
。绿色晶体配合物的化学式为_______ ,由Cl所形成的化学键类型是_______ 。
(1)向盛有硫酸铜水溶液的试管里逐滴加入氨水,首先出现蓝色沉淀,继续滴加氨水,蓝色沉淀溶解,得到深蓝色的透明溶液,请写出先后发生反应的离子方程式
(2)再向深蓝色透明溶液加入乙醇,析出深蓝色的晶体。深蓝色晶体的化学式为
(3)根据以上实验过程,判断NH3和H2O与Cu2+的配位能力:NH3
(4)已知Ti3+可形成配位数为6,颜色不同的两种配合物晶体,一种为紫色,另一种为绿色。两种晶体的组成皆为TiCl3·6H2O。为测定这两种晶体的化学式,某同学设计了如下实验:
a、分别取等质量的两种配合物晶体的样品配成待测溶液;
b、分别往待测溶液中滴入AgNO3溶液,均产生白色沉淀;
c、沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水溶液与AgNO3溶液反应得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的
 。绿色晶体配合物的化学式为
。绿色晶体配合物的化学式为
您最近半年使用:0次
【推荐2】铂及其配合物在生活中有重要应用。
(1)顺铂有抗癌作用。机理:在铜转运蛋白的作用下,顺铂进入人体细胞发生水解,生成的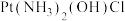 与DNA结合,破坏DNA的结构,阻止癌细胞增殖。如:
与DNA结合,破坏DNA的结构,阻止癌细胞增殖。如:

①基态Cu原子价层电子排布式为_______ 。
②鸟嘌呤与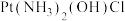 反应的产物中包含的化学键
反应的产物中包含的化学键_______ 。
A氢键 B.离子键 C.共价键 D.配位键
③在 ,配体与铂(Ⅱ)的结合能力:
,配体与铂(Ⅱ)的结合能力:
_______ ( 填“>”或“<”)。
填“>”或“<”)。
(2)顺铂和反铂互为同分异构体,两者的结构和性质如下。
①推测 的结构是
的结构是_______ (填“平面四边形”或“四面体形”)。
②顺铂在水中的溶解度大于反铂的原因是_______ 。
(3)铂晶胞为立方体,边长为a pm,结构如图:
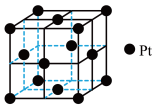
下列说法正确的是_______。
(1)顺铂有抗癌作用。机理:在铜转运蛋白的作用下,顺铂进入人体细胞发生水解,生成的
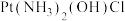 与DNA结合,破坏DNA的结构,阻止癌细胞增殖。如:
与DNA结合,破坏DNA的结构,阻止癌细胞增殖。如:
①基态Cu原子价层电子排布式为
②鸟嘌呤与
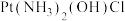 反应的产物中包含的化学键
反应的产物中包含的化学键A氢键 B.离子键 C.共价键 D.配位键
③在
 ,配体与铂(Ⅱ)的结合能力:
,配体与铂(Ⅱ)的结合能力:
 填“>”或“<”)。
填“>”或“<”)。(2)顺铂和反铂互为同分异构体,两者的结构和性质如下。
| 顺铂 | 反铂 | |
| 空间结构 |  | 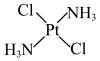 |
| 25℃时溶解度/g | 0.2577 | 0.0366 |
 的结构是
的结构是②顺铂在水中的溶解度大于反铂的原因是
(3)铂晶胞为立方体,边长为a pm,结构如图:

下列说法正确的是_______。
| A.该晶胞中含有的铂原子数目为4 |
| B.该晶体中,每个铂原子周围与它最近且等距离的铂原子有8个 |
C.该晶体的密度为 |
D.该晶体中铂原子之间的最近距离为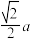 pm pm |
您最近半年使用:0次

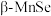 的结构中Se为面心立方最密堆积,晶胞结构如图所示。
的结构中Se为面心立方最密堆积,晶胞结构如图所示。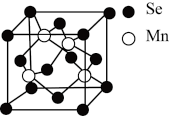

 (列出表达式即可)。
(列出表达式即可)。


