五种短周期元素A、B、C、D、E的原子序数依次增大,A和C同族,B和D 同族,C+和B3-具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的原子个数为1:1的化合物,是人们生活的必需品。回答下列问题:
(1) 五种元素中,原子半径最大的是______ ,非金属性最强的是______ (填元素符号)。
(2 )由A和D、E所形成的共价型化合物中,热稳定性差的是________ (用化学式表示)。
(3) A和E形成的化合物与A和B形成的化合物反应,产物的化学式为________ ,
其中存在的化学键类型为________ ,用电子式表示A和B其形成化合物过程________ 。
(4) D最高价氧化物的水化物的化学式为____________ 。
(5) 单质C在充足的单质E中燃烧,反应的化学方程式为________________ 。
(1) 五种元素中,原子半径最大的是
(2 )由A和D、E所形成的共价型化合物中,热稳定性差的是
(3) A和E形成的化合物与A和B形成的化合物反应,产物的化学式为
其中存在的化学键类型为
(4) D最高价氧化物的水化物的化学式为
(5) 单质C在充足的单质E中燃烧,反应的化学方程式为
15-16高一下·山西大同·期末 查看更多[2]
更新时间:2016-12-09 16:23:22
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】海水是巨大的资源宝库,海水淡化及其综合利用具有重要意义。
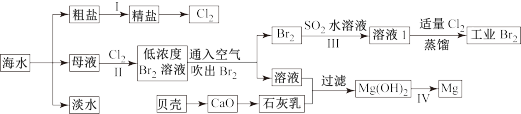
请回答下列问题:
Ⅰ.(1)步骤1中,粗盐中含有Ca2+、Mg2+、SO42-等杂质离子,粗盐精制过程中要使用Na2CO3溶液,请写出加入Na2CO3溶液后相关化学反应的离子方程式_________________ 。
(2)海水提溴,制得1mol Br2需要消耗_________ mol Cl2。步骤Ⅱ中需要向母液中加入稀硫酸酸化,其作用是___________________________ 。步骤Ⅲ若用Na2SO3水溶液吸收Br2,有关反应的离子方程式为_______________________________ 。
(3)为了从工业Br2中提纯溴,除去产物中残留的少量Cl2,可向其中加入__________ 溶液。
Ⅱ.(1)Mg在元素周期表中的位置:_____________ ,Mg(OH)2的电子式:____________ ,Mg(OH)2中所含元素的简单离子半径由小到大的顺序是____________________________ 。
(2)步骤Ⅳ由Mg(OH)2得到单质Mg,以下方法最合适的是_______________ (填序号)。
A.Mg(OH)2→MgCl2 Mg B. Mg(OH)2
Mg B. Mg(OH)2 MgO
MgO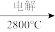 Mg
Mg
C. Mg(OH)2 MgO
MgO  Mg D. Mg(OH)2
Mg D. Mg(OH)2 无水MgCl2
无水MgCl2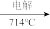 Mg
Mg
(3)判断Mg(OH)2是否洗涤干净的操作是__________________ 。
Ⅲ. 用Mg制成的格氏试剂(RMgBr)常用于有机合成,例如制备醇类化合物的合成路线如下:
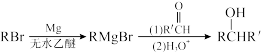 (R:烃基: R':烃基或H)依据上述信息,写出制备
(R:烃基: R':烃基或H)依据上述信息,写出制备 所需溴代烃的可能结构简式:
所需溴代烃的可能结构简式: ___________ 。

请回答下列问题:
Ⅰ.(1)步骤1中,粗盐中含有Ca2+、Mg2+、SO42-等杂质离子,粗盐精制过程中要使用Na2CO3溶液,请写出加入Na2CO3溶液后相关化学反应的离子方程式
(2)海水提溴,制得1mol Br2需要消耗
(3)为了从工业Br2中提纯溴,除去产物中残留的少量Cl2,可向其中加入
Ⅱ.(1)Mg在元素周期表中的位置:
(2)步骤Ⅳ由Mg(OH)2得到单质Mg,以下方法最合适的是
A.Mg(OH)2→MgCl2
 Mg B. Mg(OH)2
Mg B. Mg(OH)2 MgO
MgO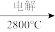 Mg
MgC. Mg(OH)2
 MgO
MgO  Mg D. Mg(OH)2
Mg D. Mg(OH)2 无水MgCl2
无水MgCl2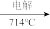 Mg
Mg(3)判断Mg(OH)2是否洗涤干净的操作是
Ⅲ. 用Mg制成的格氏试剂(RMgBr)常用于有机合成,例如制备醇类化合物的合成路线如下:
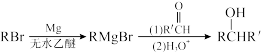 (R:烃基: R':烃基或H)依据上述信息,写出制备
(R:烃基: R':烃基或H)依据上述信息,写出制备 所需溴代烃的可能结构简式:
所需溴代烃的可能结构简式:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】A、B、C、D、E、F、G七种短周期主族元素的原子序数依次增大。A和E最外层电子数相同,短周期主族元素的原子中,E原子的半径最大;B、C和F在周期表中相邻,B、C同周期,C、F同主族,F原子的质子数是C原子质子数的2倍;A和C可形成两种常见的液态化合物X和Y(相对分子质量X<Y );D形成的分子为双原子分子。回答问题:
(1)D元素的名称为______ , F形成的离子的结构示意图为______ 。
(2)写出液态化合物Y的一种用途______ 。
(3)用某种金属易拉罐与A、C、E组成的化合物的水溶液反应,产生的气体可充填气球,请写出该反应的离子方程式______ ,使用这种气球存在的隐患是______ 。
(4)P和Q两种物质都是由A、C、E、F四种元素组成的盐,其水溶液都显酸性,等物质的量的P和Q恰好完全反应。写出该反应的离子方程式:______ 。
(5)A、B、G三种元素两两组合形成的化合物在空气中相遇形成白烟,反应的化学方程式为______ 。
(1)D元素的名称为
(2)写出液态化合物Y的一种用途
(3)用某种金属易拉罐与A、C、E组成的化合物的水溶液反应,产生的气体可充填气球,请写出该反应的离子方程式
(4)P和Q两种物质都是由A、C、E、F四种元素组成的盐,其水溶液都显酸性,等物质的量的P和Q恰好完全反应。写出该反应的离子方程式:
(5)A、B、G三种元素两两组合形成的化合物在空气中相遇形成白烟,反应的化学方程式为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】镁、铝及其化合物在制药、材料及航空航天等领域用途广泛,回答下列问题:
(1)下列状态的Mg中,电离最外层一个电子所需要的能量最大的是_____ (填序号)
a. b.
b.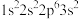 c.
c.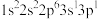 d.
d.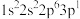
(2)Mg元素的第一电离能高于AI元素,原因是_____ 。
(3)MgO是一种耐火材料,熔点为2852℃,其熔融物中有 和
和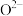 ,这两个离子的半径大小关系是
,这两个离子的半径大小关系是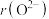
_____ 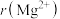 (填“>”或“<”);MgO的熔点高于NaCl的原因是
(填“>”或“<”);MgO的熔点高于NaCl的原因是_____ 。
(4)叶绿素a是自然界中常见的含镁化合物(结构如图),其结构中存在_____ (填标号)
(5)三氯化铝加热到177.8℃时,会升华为气态二聚氯化铝(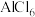 ,其中铝原子和氯原子均达8电子稳定结构),三氯化铝的晶体类型:
,其中铝原子和氯原子均达8电子稳定结构),三氯化铝的晶体类型:_____ ,请写出二聚氯化铝( )的结构式:
)的结构式:_____ ,其中铝原子轨道采用_____ 杂化。
(1)下列状态的Mg中,电离最外层一个电子所需要的能量最大的是
a.
 b.
b.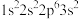 c.
c.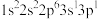 d.
d.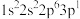
(2)Mg元素的第一电离能高于AI元素,原因是
(3)MgO是一种耐火材料,熔点为2852℃,其熔融物中有
 和
和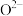 ,这两个离子的半径大小关系是
,这两个离子的半径大小关系是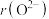
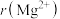 (填“>”或“<”);MgO的熔点高于NaCl的原因是
(填“>”或“<”);MgO的熔点高于NaCl的原因是(4)叶绿素a是自然界中常见的含镁化合物(结构如图),其结构中存在

(5)三氯化铝加热到177.8℃时,会升华为气态二聚氯化铝(
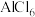 ,其中铝原子和氯原子均达8电子稳定结构),三氯化铝的晶体类型:
,其中铝原子和氯原子均达8电子稳定结构),三氯化铝的晶体类型: )的结构式:
)的结构式:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】通过简单地推理或计算填空。
(1)X原子有两个电子层,K 层电子数是L层电子数的一半,X是_______ (写元素符号)元素。
(2)若某元素形成的简单离子的电子层数和最外层电子数与 Ne原子相同,其可能的离子中半径最小的是__________ (填离子符号)。
(3)元素R能够与某非金属元素 W 形成化合物 RWn,已知 RWn 分子中各原子核外最外层电子总数为26,核外电子数总和为66 ,则 W 是___________ (写元素符号)元素,n=_____________ 。
(4)位于三个不同周期的四种短周期主族元素 A、B、C、D,其部分元素特征信息如下表:
①写出常温下D的单质与A、B、C形成的化合物的稀溶液反应的化学方程式:________________ 。
②D的最高价氧化物对应的水化物与 A、B、C形成的化合物的水溶液反应的离子方程式为________________________ 。
(1)X原子有两个电子层,K 层电子数是L层电子数的一半,X是
(2)若某元素形成的简单离子的电子层数和最外层电子数与 Ne原子相同,其可能的离子中半径最小的是
(3)元素R能够与某非金属元素 W 形成化合物 RWn,已知 RWn 分子中各原子核外最外层电子总数为26,核外电子数总和为66 ,则 W 是
(4)位于三个不同周期的四种短周期主族元素 A、B、C、D,其部分元素特征信息如下表:
| 元素编号 | 元素特征信息 |
| A | 其单质是密度最小的物质 |
| B | 阴离子带两个单位负电荷,其单质是空气的主要成分之一 |
| C | 在短周期主族元素中金属性最强 |
| D | 最高价氧化物对应水化物的酸性最强 |
①写出常温下D的单质与A、B、C形成的化合物的稀溶液反应的化学方程式:
②D的最高价氧化物对应的水化物与 A、B、C形成的化合物的水溶液反应的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】硫、氮的化合物及其相互转化在促进社会进步、资源利用和环境保护中具有重要价值。
(1)下列与氮氧化物无关的环境问题是______。
(2)工业上先用NaOH溶液吸收SO2,再用CaO使NaOH再生:NaOH溶液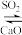 Na2SO3,使NaOH再生的原理是
Na2SO3,使NaOH再生的原理是___________ 。(用化学方程式表示)
(3)土壤中的硝酸盐会被细菌分解。有一种细菌是利用土壤中的硫化物来分解硝酸盐,其主要化学反应原理是:K2S + KNO3 +H2O =N2 +K2SO4 + KOH。
①K、S、N、O元素的原子半径从大到小的顺序是___________ 。
②上述反应中的各物质属于共价化合物是______ ;氧化剂是_______ 。
③配平上述反应方程式,并标出电子转移的方向和数目______ 。
④上述反应改变了土壤的成分,从而对农业生产产生一定的不利影响,请选择任一角度进行简要说明:________ 。
(4)氨水、NH4Cl、NH4HCO3、NH4HSO4是常见的氮肥。常温下等物质的量浓度的上述4种溶液中c( )最大的是______。
)最大的是______。
(5)某科研小组将微电池技术用于去除天然气中的H2S,装置如图所示,总反应是:2Fe+2H2S+O2=2FeS+2H2O。

①写出负极的电极反应式___________ 。
②一段时间后,单位时间内H2S的去除率降低,其可能的原因是________ 。
(1)下列与氮氧化物无关的环境问题是______。
| A.酸雨 | B.白色污染 | C.光化学烟雾 | D.温室效应 |
(2)工业上先用NaOH溶液吸收SO2,再用CaO使NaOH再生:NaOH溶液
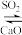 Na2SO3,使NaOH再生的原理是
Na2SO3,使NaOH再生的原理是(3)土壤中的硝酸盐会被细菌分解。有一种细菌是利用土壤中的硫化物来分解硝酸盐,其主要化学反应原理是:K2S + KNO3 +H2O =N2 +K2SO4 + KOH。
①K、S、N、O元素的原子半径从大到小的顺序是
②上述反应中的各物质属于共价化合物是
③配平上述反应方程式,并标出电子转移的方向和数目
④上述反应改变了土壤的成分,从而对农业生产产生一定的不利影响,请选择任一角度进行简要说明:
(4)氨水、NH4Cl、NH4HCO3、NH4HSO4是常见的氮肥。常温下等物质的量浓度的上述4种溶液中c(
 )最大的是______。
)最大的是______。| A.氨水 | B.NH4Cl | C.NH4HCO3 | D.NH4HSO4 |
(5)某科研小组将微电池技术用于去除天然气中的H2S,装置如图所示,总反应是:2Fe+2H2S+O2=2FeS+2H2O。

①写出负极的电极反应式
②一段时间后,单位时间内H2S的去除率降低,其可能的原因是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐3】下列表格是元素周期表的一部分。请按要求填空(用化学用语填写)
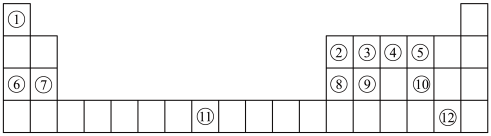
(1)元素①和⑥形成的化合物中存在的化学键类型为_______ 。
(2)用化学方程式表示④的简单氢化物的工业制法_______ 。
(3)写出由③④⑥形成的化合物的电子式_______ 。
(4)列举元素⑨形成的氧化物的一种用途_______ ,元素⑪在周期表中的位置_______ 。
(5)①⑤⑦⑧的简单离子半径由大到小的顺序为_______ 。
(6)写出⑧⑫的最高价氧化物的水化物发生反应的化学方程式为_______ 。
(7)X是由①④⑤⑧⑩形成的复盐,向含0.01 mol X的溶液中加入0.024 mol ,生成沉淀的物质的量的总和为
,生成沉淀的物质的量的总和为_______ 。

(1)元素①和⑥形成的化合物中存在的化学键类型为
(2)用化学方程式表示④的简单氢化物的工业制法
(3)写出由③④⑥形成的化合物的电子式
(4)列举元素⑨形成的氧化物的一种用途
(5)①⑤⑦⑧的简单离子半径由大到小的顺序为
(6)写出⑧⑫的最高价氧化物的水化物发生反应的化学方程式为
(7)X是由①④⑤⑧⑩形成的复盐,向含0.01 mol X的溶液中加入0.024 mol
 ,生成沉淀的物质的量的总和为
,生成沉淀的物质的量的总和为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,A与D同主族;C与E同主族;B、C同周期;B原子最外层电子数比其次外层电子数多2;A是周期表中半径最小的元素,C的最外层电子数是内层电子的3倍;F元素是同周期元素中原子半径最小的主族元素。A、B、C、D、E形成的化合物甲、乙、丙、丁的组成如下表所示:
回答下列问题:
(1)指出元素F在周期表中的位置__________________ 。
(2)化合物乙的电子式为_____________ ,用电子式表示形成化合物丁的过程_________________ 。
(3)写出丙与甲反应的离子方程式:___________________ 。
(4)固体氧化物燃料电池是以固体氧化锆—氧化钇为电解质,这种固体电解质在高温下允许O2–在其间通过,该电池的工作原理如图所示,其中多孔Pt电极a、b分别是气体C2、A2的载体。该电池的负极为_________ (填a或b);O2-流向________ 极(填“正”或“负”);该电池的正极反应式为______________ 。

| 化合物 | 甲 | 乙 | 丙 | 丁 |
| 化学式 | A2C | A2C2 | D2C2 | D2E |
(1)指出元素F在周期表中的位置
(2)化合物乙的电子式为
(3)写出丙与甲反应的离子方程式:
(4)固体氧化物燃料电池是以固体氧化锆—氧化钇为电解质,这种固体电解质在高温下允许O2–在其间通过,该电池的工作原理如图所示,其中多孔Pt电极a、b分别是气体C2、A2的载体。该电池的负极为

您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐2】表中A、B、C、D、E、F为短周期主族元素,它们的原子序数依次增大。
(1)C基态原子的价电子轨道表达式为_____ ,CA3分子空间构型为_____ 。B,C,D三种元素的第一电离能由大到小的顺序_____ (填元素符号)。
(2)F的简单氢化物的VSEPR模型名称为_____ ,其属于_____ (填“极性”或“非极性”)分子,其沸点比水低的原因是_____ 。
(3)火箭推动剂由C2A4和A2D2组成,加热反应时有C元素的单质生成,写出该化学反应方程式:_____ 。
(4)下列关于C2A4和B2A4的说法中正确的是_____(填序号)。
(5)由E和G元素组成的化合物是共价化合物,该化合物气态时以共价的二聚分子(E2G6)形式存在,分子中所有原子都达到8e-稳定结构,请画出该二聚分子的结构式_____ 。
| A.元素周期表中原子半径最小的元素 | B.原子最外层电子数是内层电子数的2倍 |
| C.元素原子的核外p电子总数比s电子总数少1 | D.基态原子的价电子排布式为nsnnp2n |
| E.同周期中简单离子的半径最小 | F.与D同主族,且原子序数为D的2倍 |
| G.元素的主族序数与周期数的差为4 |
(2)F的简单氢化物的VSEPR模型名称为
(3)火箭推动剂由C2A4和A2D2组成,加热反应时有C元素的单质生成,写出该化学反应方程式:
(4)下列关于C2A4和B2A4的说法中正确的是_____(填序号)。
| A.分子中都含σ键和π键 |
| B.C2A4比B2A4的沸点高 |
| C.都是含极性键和非极性键的非极性分子 |
| D.B2A4分子发生加成反应时σ键断裂 |
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】A、B、C、D、E是位于短周期的主族元素.已知:①热稳定性:HmD>HmC;
②Cm﹣、E(m﹣1)﹣具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍.依据上述信息用相应的化学用语回答下列问题:
(1)HmDm的电子式_____ .
(2)能证明Cm﹣、E(m﹣1)﹣的还原性强弱的离子方程式为____________ .
(3)将E的单质通入A与D形成的化合物的水溶液中,其离子方程式为:___________ .常温下,将等物质的量浓度的HmC溶液和A的最高价氧化物对应的水化物溶液等体积混合,写出该反应的离子方程式________________________ .
②Cm﹣、E(m﹣1)﹣具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍.依据上述信息用相应的化学用语回答下列问题:
(1)HmDm的电子式
(2)能证明Cm﹣、E(m﹣1)﹣的还原性强弱的离子方程式为
(3)将E的单质通入A与D形成的化合物的水溶液中,其离子方程式为:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】五种短周期元素A、B、C、D、E,原子序数依次增大,其中A、B同周期,且A、B原子核外均有两个未成对电子;A、D同主族,B、E同主族,且C的最外层电子比E的最外层电子少5个。根据以上信息,完成下列各题。
(1)写出下列化学用语:A:_____ B:_____ C:_____ D:_______ E:_______
(2)A的最高价氧化物的熔点_________ D的最高价氧化物的熔点(填“>”或“<”),原因是_______________________ ;B氢化物的沸点______ E氢化物的沸点(填“>”或“<”),原因是______________ 。
(3)选取上述五种元素,完成下列问题
①构成的原子晶体有___________________ ;
②含有非极性键的离子化合物__________________ (用电子式表示)
③含有极性键的非极性分子_______________ (用电子式表示)
(1)写出下列化学用语:A:
(2)A的最高价氧化物的熔点
(3)选取上述五种元素,完成下列问题
①构成的原子晶体有
②含有非极性键的离子化合物
③含有极性键的非极性分子
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐2】下表是元素周期表的一部分,回答下列有关问题:
(1)写出下列元素的元素符号:① ______ ,⑥______ ,⑦ _______ ,⑨______ 。
(2)画出下列微粒的结构示意图:④的原子:____________ ,⑧的离子:___________ 。
(3)表中的12种元素中,金属性最强的元素是________ ,非金属性最强的元素是_________ ,最不活泼的元素是_______ 。(均填元素符号)
(4)③④⑤⑦⑧五种元素中,离子半径最大的元素是______ (填元素符号)。元素③和⑦可以形成 _____________ (填“离子”或“共价”)化合物。
(5)表中某元素能形成两性氧化物,写出该氧化物溶于氢氧化钠溶液的离子方程式____________ 。
族 周期 | IA | IIA | IIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(2)画出下列微粒的结构示意图:④的原子:
(3)表中的12种元素中,金属性最强的元素是
(4)③④⑤⑦⑧五种元素中,离子半径最大的元素是
(5)表中某元素能形成两性氧化物,写出该氧化物溶于氢氧化钠溶液的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】在如图所示的物质转化关系中,A是用于制造汽车发动机的耐高温陶瓷材料,A由两种元素组成,且两种元素化合价的绝对值相等;常温下,C、F、K是无色无味的气体单质,D、H是固体单质,E是常见的两性氧化物,B、G是汽车尾气中的主要污染气体,所含元素均为第二周期元素,反应②常用于汽车尾气的处理。
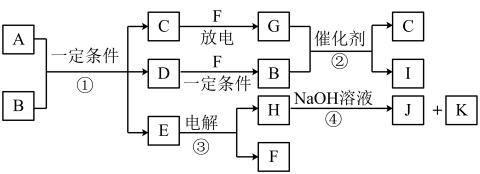
(1)C的电子式_______ 。
(2)A的化学式_______ 。
(3)反应③的化学方程式_______ 。
(4)反应④的离子方程式_______ 。

(1)C的电子式
(2)A的化学式
(3)反应③的化学方程式
(4)反应④的离子方程式
您最近一年使用:0次



