某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2 转变为H2、CO。其过程如下:
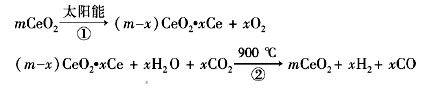
下列说法不正确的是
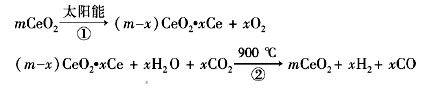

下列说法不正确的是
| A.该过程中CeO2没有消耗 |
| B.该过程实现了太阳能向化学能的转化 |
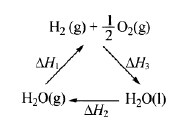
| C.右图中△H1=△H2+△H3 |
D.以CO和O2构成的碱性燃料电池的负极反应式为CO+4OH- - 2e- = +2H2O +2H2O |
更新时间:2016-12-09 16:35:19
|
相似题推荐
【推荐1】科学家研发的“界面光热技术”可用于海水淡化,其原理如图所示。下列说法正确的是


| A.该过程发生了化学变化 |
| B.水分子通过光热层时氢键断裂 |
| C.亲水多孔基底可用聚乙烯材料 |
| D.光热层可实现“光能→热能”的完全转化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列与化学反应能量变化相关的叙述正确的是
| A.干冰气化需要吸收大量的热,这个变化是吸热反应 |
| B.反应物的总能量低于生成物的总能量时,发生放热反应 |
| C.化学反应中的能量变化都表现为热量的变化 |
| D.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】人体内的血红蛋白(Hb)可与O2结合,更易与CO结合使人体中毒,涉及原理如下:
①
②
③
下列说法错误的是
①

②

③

下列说法错误的是
A. 的数值范围是>1 的数值范围是>1 |
| B.反应①、②在一定温度下均可能自发进行 |
| C.刚从平原到高原时,人体血液中c(HbO2)将降低,使人体因缺氧而不适 |
| D.将CO中毒的人转至高压氧仓中治疗,反应③平衡逆向移动而缓解症状 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某人设想利用①3FeCl2+4H2O 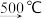 Fe3O4+6HCl+H2
Fe3O4+6HCl+H2
②Fe3O4+3/2Cl2+6HCl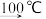 3FeCl3+3H2O +1/2O2
3FeCl3+3H2O +1/2O2
③3FeCl3 3FeCl2+3/2Cl2
3FeCl2+3/2Cl2
这3个反应的联合与循环,主要用来生产能解决环境和能源问题的某种气体,该气体是
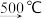 Fe3O4+6HCl+H2
Fe3O4+6HCl+H2②Fe3O4+3/2Cl2+6HCl
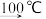 3FeCl3+3H2O +1/2O2
3FeCl3+3H2O +1/2O2③3FeCl3
 3FeCl2+3/2Cl2
3FeCl2+3/2Cl2这3个反应的联合与循环,主要用来生产能解决环境和能源问题的某种气体,该气体是
| A.O2 | B.Cl2 | C.H2 | D.HCl |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】通过以下反应均可获取H2。
①C(s) + H2O (g) = CO(g)+H2(g) ΔH1=+ 131.3kJ·mol-1
②CH4(g) + H2O (g) = CO(g)+3H2(g) ΔH2=+ 206.1kJ·mol-1
③CO (g) + H2O (g) = CO2(g)+H2(g) ΔH3
下列说法正确的是
①C(s) + H2O (g) = CO(g)+H2(g) ΔH1=+ 131.3kJ·mol-1
②CH4(g) + H2O (g) = CO(g)+3H2(g) ΔH2=+ 206.1kJ·mol-1
③CO (g) + H2O (g) = CO2(g)+H2(g) ΔH3
下列说法正确的是
| A.①中反应物的总能量大于生成物的总能量 |
| B.②中使用适当催化剂,降低了活化能,同时可以使ΔH2 减小 |
| C.若知反应C (s) + CO2(g) =2CO(g)的ΔH,结合ΔH1 可计算出ΔH3 |
| D.由①、②计算反应CH4 (g) = C(s)+2H2(g)的ΔH = -74.8kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列有关实验或操作能达到实验目的的是


| A.①证明Ksp(AgCl)>Ksp(AgI) |
| B.②装置蒸发氯化铝溶液制备无水氯化铝 |
| C.③装置用已知浓度的盐酸滴定未知浓度的NaOH溶液 |
| D.④验证二氯化锰对过氧化氢的分解能起到催化的作用 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】制硫酸时,接触室中发生反应: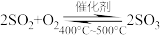 。下列有关说法不正确的是
。下列有关说法不正确的是
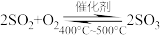 。下列有关说法不正确的是
。下列有关说法不正确的是| A.使用催化剂是为了增大反应速率,提高生产效率 |
| B.上述条件下达到化学平衡时,各组分浓度保持一定 |
| C.通过调控反应的条件,可以提高反应进行的程度 |
D.延长反应物在接触室内的时间,可使 全部转化为 全部转化为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】设NA为阿伏加 德罗常数的值,下列说法正确的是( )
| A.高温下,0.2molFe与足量水蒸气反应,生成的H2分子数目为0.3NA |
| B.室温下,pH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA |
| C.氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA |
D.5NH4NO3 2HNO3+4N2↑+9H2O反应,生成28gN2时,转移的电子数目为3.75NA 2HNO3+4N2↑+9H2O反应,生成28gN2时,转移的电子数目为3.75NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】一种碱性“二甲醚(CH3OCH3)直接燃料电池”具有启动快、能量密度高、效率好等优点。其电池总反应为 ,下列说法不正确的是
,下列说法不正确的是
 ,下列说法不正确的是
,下列说法不正确的是| A.电极正极可用多孔碳材料制成 |
B.电池负极发生的反应为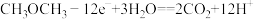 |
C.理论上,1 mol二甲醚放电量是1 mol甲醇( )放电量的2倍 )放电量的2倍 |
D.电池工作时, 向电池负极迁移 向电池负极迁移 |
您最近一年使用:0次