在体积均为1.0 L的两恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1 mol CO2和0.2 mol CO2,在不同温度下反应CO2(g)+C(s) 2CO(g)达到平衡,平衡时c(CO2) 随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是
2CO(g)达到平衡,平衡时c(CO2) 随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是

 2CO(g)达到平衡,平衡时c(CO2) 随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是
2CO(g)达到平衡,平衡时c(CO2) 随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是
| A.该反应的ΔH>0、ΔS<0 |
| B.体系的总压强p:p(Ⅰ)>p(Ⅲ) |
| C.平衡常数:K(Ⅰ)>K(Ⅱ) |
| D.T1K时,Ⅳ点所处的状态中v(正)<v(逆) |
16-17高二上·山西太原·阶段练习 查看更多[8]
更新时间:2016-11-15 15:50:34
|
相似题推荐
单选题
|
困难
(0.15)
【推荐1】在体积为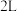 的恒容密闭容器中充入一定量的
的恒容密闭容器中充入一定量的 气体,发生反应
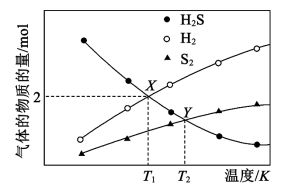
气体,发生反应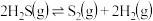 ,平衡时三种组分的物质的量与温度的关系如图所示,下列说法正确的是
,平衡时三种组分的物质的量与温度的关系如图所示,下列说法正确的是
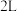 的恒容密闭容器中充入一定量的
的恒容密闭容器中充入一定量的 气体,发生反应
气体,发生反应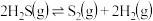 ,平衡时三种组分的物质的量与温度的关系如图所示,下列说法正确的是
,平衡时三种组分的物质的量与温度的关系如图所示,下列说法正确的是
A.反应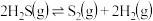 的Δ 的Δ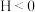 |
B. 点和 点和 点气体的压强之比为 点气体的压强之比为 |
C. 时,向 时,向 点容器中再充入 点容器中再充入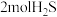 和 和 ,上述反应平衡正向移动 ,上述反应平衡正向移动 |
D. 时,若起始时向容器中充入 时,若起始时向容器中充入 气体,则平衡时 气体,则平衡时 的转化率小于 的转化率小于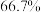 |
您最近半年使用:0次
单选题
|
困难
(0.15)
名校
【推荐2】工业上用 和
和 合成甲醇涉及以下反应:
合成甲醇涉及以下反应:
I.

II.

在催化剂作用下,将
 和
和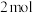
 的混合气体充入一恒容密闭容器中进行反应,达到平衡时,
的混合气体充入一恒容密闭容器中进行反应,达到平衡时, 的转化率和容器中混合气体的平均相对分子质量随温度变化如图。下列判断合理的是
的转化率和容器中混合气体的平均相对分子质量随温度变化如图。下列判断合理的是 在
在 总消耗量中占比。
总消耗量中占比。
 和
和 合成甲醇涉及以下反应:
合成甲醇涉及以下反应:I.


II.


在催化剂作用下,将

 和
和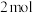
 的混合气体充入一恒容密闭容器中进行反应,达到平衡时,
的混合气体充入一恒容密闭容器中进行反应,达到平衡时, 的转化率和容器中混合气体的平均相对分子质量随温度变化如图。下列判断合理的是
的转化率和容器中混合气体的平均相对分子质量随温度变化如图。下列判断合理的是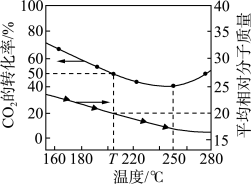
 在
在 总消耗量中占比。
总消耗量中占比。A.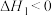 , ,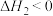 |
| B.250℃前以反应Ⅱ为主 |
C. ,平衡时甲醇的选择性为60% ,平衡时甲醇的选择性为60% |
D.为同时提高 的平衡转化率和平衡时甲醇的选择性,应选择的反应条件为高温、高压 的平衡转化率和平衡时甲醇的选择性,应选择的反应条件为高温、高压 |
您最近半年使用:0次
单选题
|
困难
(0.15)
名校
【推荐3】下列图示与对应的叙述相符的是
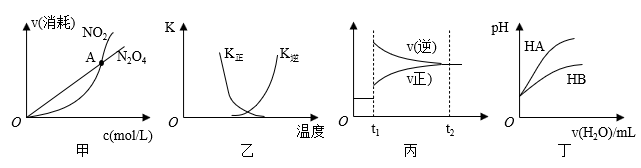

A.图甲表示在恒容密闭容器中,恒温条件下发生的可逆反应2NO2(g) N2O4(g),各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 N2O4(g),各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 |
B.图乙曲线表示反应2A(g)+B(g) 2C(g) ΔH>0,正、逆反应的平衡常数K随温度的变化 2C(g) ΔH>0,正、逆反应的平衡常数K随温度的变化 |
C.图丙表示对反应2X(g)+Y(g) Z(s)+3W(g) ΔH<0在t1时刻增大压强 Z(s)+3W(g) ΔH<0在t1时刻增大压强 |
| D.图丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH小于NaB溶液pH |
您最近半年使用:0次
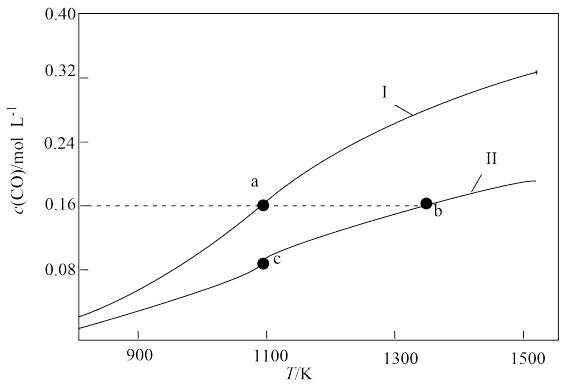
【推荐1】体积均为1.0L的甲、乙两个恒容密闭容器,向甲中加入0.1molCO2和0.3mol碳粉,向乙中加入0.4molCO,在不同温度下发生反应:CO2(g)+C(s) 2CO(g)。达到平衡时CO的物质的量浓度随温度的变化如图所示。下列说法正确的是
2CO(g)。达到平衡时CO的物质的量浓度随温度的变化如图所示。下列说法正确的是
 2CO(g)。达到平衡时CO的物质的量浓度随温度的变化如图所示。下列说法正确的是
2CO(g)。达到平衡时CO的物质的量浓度随温度的变化如图所示。下列说法正确的是
| A.曲线II对应的是乙容器 |
| B.a、b两点对应平衡体系中的压强之比:pa:pb<14:9 |
C.b点对应的平衡体系中,CO的体积分数小于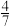 |
| D.900K时,起始时向容器乙中加入CO、CO2、碳粉各1mol,此时v正﹥v逆 |
您最近半年使用:0次
【推荐2】在体积均为1.0L的恒容密闭容器甲、乙中,起始投料量如表,在不同温度下发生反应:CO2(g)+C(s) 2CO(g)。CO的平衡浓度随温度的变化如图所示。下列说法正确的是
2CO(g)。CO的平衡浓度随温度的变化如图所示。下列说法正确的是

 2CO(g)。CO的平衡浓度随温度的变化如图所示。下列说法正确的是
2CO(g)。CO的平衡浓度随温度的变化如图所示。下列说法正确的是| 容器 | n(CO2)/mol | n(C)/mol | n(CO)/mol |
| 甲 | 0.1 | 0.3 | 0 |
| 乙 | 0 | 0 | 0.4 |

| A.曲线Ⅰ对应的是甲容器 |
| B.a、b两点所处状态的压强大小关系:9pa>14pb |
C.c点:CO的体积分数>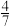 |
| D.900K时,若起始向容器乙中加入CO、CO2、C各1mol,则v(正)>v(逆) |
您最近半年使用:0次



