25. 实验室制备1,2二溴乙烷的反应原理如下:CH
3CH
2OH

CH
2=CH
2↑+H
2O,CH
2=CH
2+Br
2→BrCH
2CH
2Br。用少量的溴和足量的乙醇制备1,2二溴乙烷的装置如下图所示:
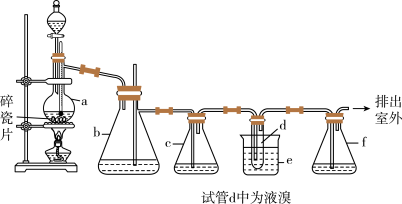
有关数据列表如下:
| 乙醇 | 1,2二溴乙烷 | 乙醚 |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)在装置c中应加入
________(选填序号),其目的是吸收反应中可能生成的酸性气体。
①水
②浓硫酸
③氢氧化钠溶液
④饱和碳酸氢钠溶液
(2)判断d管中制备二溴乙烷反应已结束的最简单方法是
________。
(3)将二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在水的
________(填“上”或“下”)层。
(4)若产物中有少量未反应的Br
2,最好用
________(填正确选项前的序号)洗涤除去。①水 ②氢氧化钠溶液 ③碘化钠溶液 ④乙醇
(5)反应过程中需用冷水冷却(装置e), 但不用冰水进行过度冷却,原因
__________________。