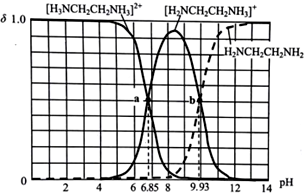
乙二胺(H2NCH2CH2NH2) 与NH3相似,水溶液呈碱性,25℃时,向10mL0.1mol·L-1乙二胺溶液中滴加0.1 mol·L-1盐酸,各组分的物质的量分数δ随溶液pH的变化曲线如图所示,下列说法错误的是

| A.混合溶液呈中性时,滴加盐酸的体积小于10mL |
| B.Kb2[H2NCH2CH2NH2] 的数量级为10-8 |
| C.a 点所处的溶液中:c(H+)+3c([H3NCH2CH2NH3]2+)=c(OH-) +(Cl-) |
| D.水的电离程度:a>b |
更新时间:2018-04-21 09:44:42
|
相似题推荐
单选题
|
困难
(0.15)
名校
解题方法
【推荐1】已知 ℃时,
℃时, 溶液的
溶液的 ,
, 的HA溶液中
的HA溶液中 ,则
,则 的HA溶液中水电离出的
的HA溶液中水电离出的 为
为
 ℃时,
℃时, 溶液的
溶液的 ,
, 的HA溶液中
的HA溶液中 ,则
,则 的HA溶液中水电离出的
的HA溶液中水电离出的 为
为A.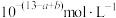 | B. |
C.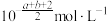 | D.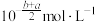 |
您最近一年使用:0次
单选题
|
困难
(0.15)
解题方法
【推荐2】室温下,向体积均为20 且浓度均为0.1
且浓度均为0.1 的
的 溶液、
溶液、 溶液中分别滴加同浓度的
溶液中分别滴加同浓度的 溶液,反应后溶液中水电离出的
溶液,反应后溶液中水电离出的 的负对数[
的负对数[ ]与滴加氢氧化钠溶液体积的关系如图所示。下列说法正确的是
]与滴加氢氧化钠溶液体积的关系如图所示。下列说法正确的是

 且浓度均为0.1
且浓度均为0.1 的
的 溶液、
溶液、 溶液中分别滴加同浓度的
溶液中分别滴加同浓度的 溶液,反应后溶液中水电离出的
溶液,反应后溶液中水电离出的 的负对数[
的负对数[ ]与滴加氢氧化钠溶液体积的关系如图所示。下列说法正确的是
]与滴加氢氧化钠溶液体积的关系如图所示。下列说法正确的是
A.室温时,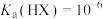 |
| B.a、b、c三点对应溶液均显中性 |
| C.b、d两点对应溶液的阴离子总浓度不同 |
D.c点对应溶液中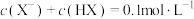 |
您最近一年使用:0次
单选题
|
困难
(0.15)
名校
解题方法
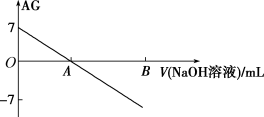
【推荐1】若用AG表示溶液的酸度,AG 的定义为 ,室温下实验室中用0.01 mol.L-1 的氢氧化钠溶液滴定20.00 mL 0.01 mol.L-1 醋酸,滴定过程如图所示,下列叙述正确的是
,室温下实验室中用0.01 mol.L-1 的氢氧化钠溶液滴定20.00 mL 0.01 mol.L-1 醋酸,滴定过程如图所示,下列叙述正确的是
 ,室温下实验室中用0.01 mol.L-1 的氢氧化钠溶液滴定20.00 mL 0.01 mol.L-1 醋酸,滴定过程如图所示,下列叙述正确的是
,室温下实验室中用0.01 mol.L-1 的氢氧化钠溶液滴定20.00 mL 0.01 mol.L-1 醋酸,滴定过程如图所示,下列叙述正确的是
| A.室温下,醋酸的电离常数约为10-5 |
| B.A点时加入氢氧化钠溶液的体积为20.00mL |
| C.若B点为40 mL,所得溶液中:2c(Na+)=c(CH3COO-)+c(CH3COOH) |
| D.滴定过程中一定存在:0.01 mol/L+c(OH-)=c(Na+)+c(H+)+c(CH3COOH) |
您最近一年使用:0次
单选题
|
困难
(0.15)
名校
解题方法
【推荐2】根据下列图示所得出的结论不正确的是
A.图甲是室温下20 mL 0.1 mol•L﹣1氨水中滴加盐酸,溶液中由水电离出的c(H+)随加入盐酸体积的变化关系,图中b、d两点溶液的pH值均为7 |
B.图乙是CO(g)+H2O(g)⇌CO2(g)+H2(g)的平衡常数与反应温度的关系曲线,说明该反应的△H<0 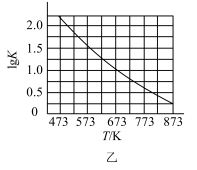 |
C.图丙是室温下用0.1000 mol•L﹣1 NaOH溶液滴定20.00 mL 0.1000 mol•L﹣1某一元酸HX的滴定曲线,该 滴定过程可以选择酚酞作为指示剂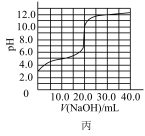 |
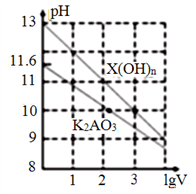
D.图丁是室温下用 Na2SO4除去溶液中 Ba2+达到沉淀溶解平衡时,溶液中 c(Ba2+)与 c(SO42﹣)的关系曲线,说明 Ksp(BaSO4)=1×10﹣10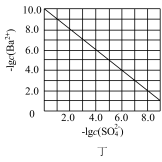 |
您最近一年使用:0次
单选题
|
困难
(0.15)
解题方法
【推荐1】 时,改变
时,改变 甲酸
甲酸 与丙酸
与丙酸 溶液的
溶液的 ,溶液中
,溶液中 分子的物质的量分数
分子的物质的量分数 随之改变[已知
随之改变[已知 ],
], 与
与 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是

 时,改变
时,改变 甲酸
甲酸 与丙酸
与丙酸 溶液的
溶液的 ,溶液中
,溶液中 分子的物质的量分数
分子的物质的量分数 随之改变[已知
随之改变[已知 ],
], 与
与 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
A.若弱酸 增大是通过向弱酸中加入 增大是通过向弱酸中加入 固体实现的,则图中M、N两点对应溶液中的 固体实现的,则图中M、N两点对应溶液中的 相等 相等 |
B.对于甲酸和丙酸,当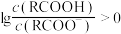 时,溶液都为酸性 时,溶液都为酸性 |
C.等浓度的 和 和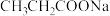 两种溶液的 两种溶液的 :前者>后者 :前者>后者 |
D.将 的 的 溶液与 溶液与 的 的 溶液等体积混合,所得溶液中: 溶液等体积混合,所得溶液中: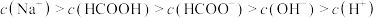 |
您最近一年使用:0次
单选题
|
困难
(0.15)
名校
【推荐2】连二次硝酸(H2N2O2)是一种二元酸,常温下,用0.01mol·L-1的NaOH溶液滴定10mL0.01mol·L-1的H2N2O2溶液,测得溶液pH与NaOH溶液体积的关系如图。常温下,下列各点所对应溶液中微粒物质的量浓度关系正确的是


A.a点:c(N2O )+c(HN2O )+c(HN2O )-c(Na+)=9.9×10-7mol·L-1 )-c(Na+)=9.9×10-7mol·L-1 |
B.b点:c(Na+)>c(N2O )+c(HN2O )+c(HN2O )+c(H2N2O2) )+c(H2N2O2) |
C.c点:c(Na+)>c(HN2O )>c(H2N2O2) >c(N2O )>c(H2N2O2) >c(N2O ) ) |
D.d点:c(H2N2O2)+c(HN2O )+c(H+)=c(OH-) )+c(H+)=c(OH-) |
您最近一年使用:0次
单选题
|
困难
(0.15)
名校
解题方法
【推荐3】将Cl2缓慢通入1L0.1mol·L-1Na2CO3溶液中,反应过程中无CO2逸出,用数字传感器测得溶液中pH与c(HClO)的变化如图所示。已知Ka1(H2CO3)=10-6.3,Ka2(H2CO3)=10-10.3。下列说法错误的是

| A.曲线①表示溶液中pH的变化 |
| B.整个过程中,水的电离程度逐渐减小 |
C.a点溶液中:c(H+)=2c( )+c( )+c( )+c(OH-) )+c(OH-) |
D.pH=10.3时:c(Na+)>3c( )+2c(ClO-)+c(HClO) )+2c(ClO-)+c(HClO) |
您最近一年使用:0次

 溶液中逐滴加入
溶液中逐滴加入 的
的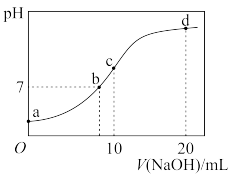
 所示溶液中:
所示溶液中: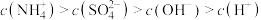
 所示溶液中:
所示溶液中: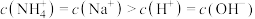
 所示溶液中:
所示溶液中:
 以后的溶液中可能出现:
以后的溶液中可能出现: