在25℃时,密闭容器中X、Y、Z三种气体的起始浓度和平衡浓度如下表,下列说法错误的是
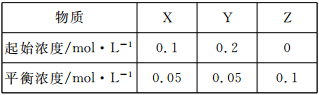

| A.反应达到平衡时,X的转化率为50% |
B.反应可表示为X+3Y 2Z,平衡常数为1600 2Z,平衡常数为1600 |
| C.其他条件不变时,增大压强可使平衡常数增大 |
| D.改变温度可以改变该反应的平衡常数 |
更新时间:2016-12-09 17:33:30
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】工业上可利用如下反应合成甲醇:CO(g)+2H2(g) CH3OH(g),该反应在不同温度时的平衡常数如下表所示。下列说法正确的是( )
CH3OH(g),该反应在不同温度时的平衡常数如下表所示。下列说法正确的是( )
 CH3OH(g),该反应在不同温度时的平衡常数如下表所示。下列说法正确的是( )
CH3OH(g),该反应在不同温度时的平衡常数如下表所示。下列说法正确的是( )| 温度(℃) | 250 | 300 | 350 |
| K | 2.041 | 0.270 | 0.012 |
| A.正反应ΔH>0 |
| B.300 ℃时在某一密闭容器中进行该反应,某时刻测得三种气体的浓度均为0.5 mol·L-1,则此时平衡向逆反应方向移动 |
| C.恒温恒压下,向容器中充入少量N2,平衡将正向移动 |
| D.恒温恒容下,向容器中再充入少量CO(g),达到新平衡时,H2的转化率减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】25℃时,恒容密闭容器中只含有X,发生反应: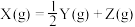 ,X的起始压强为
,X的起始压强为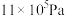 ,X分解的速率方程为:
,X分解的速率方程为: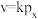 ,其中k定温下为常数。生成的Y可快速建立平衡:
,其中k定温下为常数。生成的Y可快速建立平衡: ,平衡常数
,平衡常数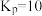 。下列说法正确的是
。下列说法正确的是
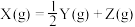 ,X的起始压强为
,X的起始压强为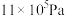 ,X分解的速率方程为:
,X分解的速率方程为: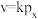 ,其中k定温下为常数。生成的Y可快速建立平衡:
,其中k定温下为常数。生成的Y可快速建立平衡: ,平衡常数
,平衡常数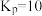 。下列说法正确的是
。下列说法正确的是A.当X分解的速率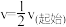 时,W的压强为 时,W的压强为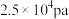 |
B.若升高温度,Z和W的物质的量之比为 ,则 ,则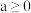 |
| C.相同时间内,X的平均速率是Y的平均速率的2倍 |
| D.若缩小体积,则单位时间内X的转化率减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】可逆反应A(g) + 3B(g)  2C(g);△H < 0。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1 molA和3 molB,在一定条件到下达平衡时放出热量为Q1 kJ;在相同的条件下,向乙容器中加入2 molC达到平衡后吸收热量为Q2 kJ,已知Q1=3Q2。下列叙述错误的是
2C(g);△H < 0。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1 molA和3 molB,在一定条件到下达平衡时放出热量为Q1 kJ;在相同的条件下,向乙容器中加入2 molC达到平衡后吸收热量为Q2 kJ,已知Q1=3Q2。下列叙述错误的是
 2C(g);△H < 0。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1 molA和3 molB,在一定条件到下达平衡时放出热量为Q1 kJ;在相同的条件下,向乙容器中加入2 molC达到平衡后吸收热量为Q2 kJ,已知Q1=3Q2。下列叙述错误的是
2C(g);△H < 0。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1 molA和3 molB,在一定条件到下达平衡时放出热量为Q1 kJ;在相同的条件下,向乙容器中加入2 molC达到平衡后吸收热量为Q2 kJ,已知Q1=3Q2。下列叙述错误的是| A.甲中A的转化率为75% |
| B.甲、乙中C的体积分数相同 |
| C.平衡后再向乙中加入0.25 mol A、0.75 mol B、1.5 mol C,平衡向生成C的方向移动 |
D.乙中的热化学反应方程式为2C(g) A(g)+3B(g);△H=+3Q2 kJ·mol-1 A(g)+3B(g);△H=+3Q2 kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s) 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。
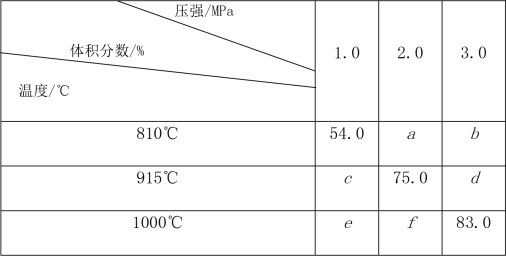
①b>f ②915℃,2.0MPa时E的转化率为60% ③该反应的ΔS<0 ④K(1000℃)<K(810℃)
上述①~④中正确的有( )
 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。
①b>f ②915℃,2.0MPa时E的转化率为60% ③该反应的ΔS<0 ④K(1000℃)<K(810℃)
上述①~④中正确的有( )
| A.4个 | B.3个 | C.2个 | D.1个 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某温度下,反应X(g)+3Y(g) 2Z(g)的平衡常数为1 600。此温度下,在容积一定的密闭容器中加入一定量的X和Y,反应到某时刻测得各组分的浓度如下:
2Z(g)的平衡常数为1 600。此温度下,在容积一定的密闭容器中加入一定量的X和Y,反应到某时刻测得各组分的浓度如下:
下列说法正确的是
 2Z(g)的平衡常数为1 600。此温度下,在容积一定的密闭容器中加入一定量的X和Y,反应到某时刻测得各组分的浓度如下:
2Z(g)的平衡常数为1 600。此温度下,在容积一定的密闭容器中加入一定量的X和Y,反应到某时刻测得各组分的浓度如下:| 物质 | X | Y | Z |
浓度/(mol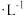 ) ) | 0.06 | 0.08 | 0.08 |
下列说法正确的是
| A.此时v(正)<v(逆) |
| B.平衡时Y的浓度为0.05 mol·L-1 |
| C.平衡时X的转化率为40% |
| D.增大压强使平衡向正反应方向移动,平衡常数增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】在800℃时,体积为1升的密闭容器中,下列可逆反应达到化学平衡状态:CO(g)+H2O(g)CO2(g)+H2(g),已知CO和H2O(g)的初始浓度为0.01mol·L-1时,H2平衡浓度为0.005mol·L-1.若此时再加入0.02mol·L-1的H2O(g),重新达到平衡时,H2平衡浓度为
| A.0.025 mol·L-1 | B.0.0075 mol·L-1 | C.0.005 mol·L-1 | D.0.015 mol·L-1 |
您最近一年使用:0次



