粉煤灰中含有SiO2、Al2O3、Fe2O3等,某实验室对其进行处理的流程如图所示:
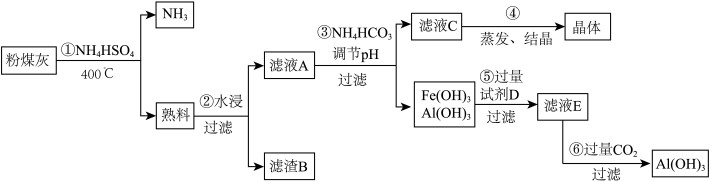
回答下列问题:
(1)第①步得到的“熟料”中可溶性的成分主要是NH4Fe(SO4)2、NH4Al(SO4)2等,写出生成NH4Fe(SO4)2的化学方程式_____________ 。在NH4Al(SO4)2溶液中加入Ba(OH)2溶液使硫酸根离子恰好完全沉淀,写出反应的离子方程式:____________ 。
(2)滤渣B的主要成分为_____________ 。
(3)已知Ksp[Fe(OH)3]=4×10-38,Ksp[Al(OH)3]=1×10-33。为实现步骤③的实验目的,应使溶液中c(Fe3+)、c(Al3+)均小于或等于1×10-9 mol/L,可认为完全沉淀,则溶液A至少应调节到pH=_____________ 。用NH4HCO3调节pH的实验原理为_____________ (用离子方程式表示)。
(4)实验室进行第④步操作时,所需的仪器是酒精灯、石棉网、三脚架、__________ 、_____________ 。

回答下列问题:
(1)第①步得到的“熟料”中可溶性的成分主要是NH4Fe(SO4)2、NH4Al(SO4)2等,写出生成NH4Fe(SO4)2的化学方程式
(2)滤渣B的主要成分为
(3)已知Ksp[Fe(OH)3]=4×10-38,Ksp[Al(OH)3]=1×10-33。为实现步骤③的实验目的,应使溶液中c(Fe3+)、c(Al3+)均小于或等于1×10-9 mol/L,可认为完全沉淀,则溶液A至少应调节到pH=
(4)实验室进行第④步操作时,所需的仪器是酒精灯、石棉网、三脚架、
更新时间:2017-02-17 14:53:36
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】镍、钴及其化合物在工业上有广泛的应用。以含镍废料(主要成分为NiO,含少量FeO、Fe2O3、CoO、BaO和SiO2)为原料制备NixOy,和碳酸钴(CoCO3)的工艺流程如图。
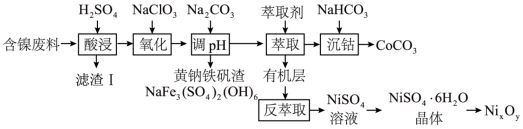
已知:Ksp[Co(OH)2]=2×10-15,请回答以下问题:
(1)“滤渣I”主要成分是___________ 。
(2)“氧化”时反应的离子方程式是___________ ,为证明添加NaClO3已足量,可用___________ (写化学式)溶液进行检验。
(3)“调pH”过程中生成黄钠铁钒沉淀,该反应的离子方程式为___________ 。
(4)“萃取”和“反萃取”可简单表示为:2HX+Ni2+ NiX2+2H+。在萃取过程中加入适量氨水,其作用是
NiX2+2H+。在萃取过程中加入适量氨水,其作用是___________ 。“反萃取”需要往有机层中加___________ (填试剂)。
(5)若起始时c(Co2+)=0.02mol∙L-1,“沉钴”过程中应控制pH___________ (填范围)。
(6)资料显示,硫酸镍结晶水合物的形态与温度有如表关系。
由NiSO4溶液获得稳定的NiSO4•6H2O晶体的操作依次是蒸发浓缩、___________ 、过滤、洗涤、干燥。

已知:Ksp[Co(OH)2]=2×10-15,请回答以下问题:
(1)“滤渣I”主要成分是
(2)“氧化”时反应的离子方程式是
(3)“调pH”过程中生成黄钠铁钒沉淀,该反应的离子方程式为
(4)“萃取”和“反萃取”可简单表示为:2HX+Ni2+
 NiX2+2H+。在萃取过程中加入适量氨水,其作用是
NiX2+2H+。在萃取过程中加入适量氨水,其作用是(5)若起始时c(Co2+)=0.02mol∙L-1,“沉钴”过程中应控制pH
(6)资料显示,硫酸镍结晶水合物的形态与温度有如表关系。
| 温度 | 低于30.8°C | 30.8°C~53.8°C | 53.8°C~280°C | 高于280°C |
| 晶体形态 | NiSO4•7H2O | NiSO4•6H2O | 多种结晶水合物 | NiSO4 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】某工厂利用制革工业污泥[含Cr(III)]制取CrOH(H2O)5SO4的工艺流程如下:
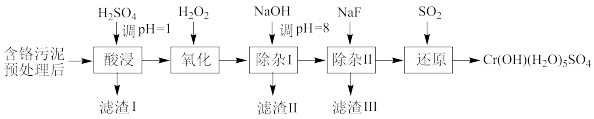
已知:酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+等。
(1)酸浸时,为了提高浸取率可采取的措施有_______ 。
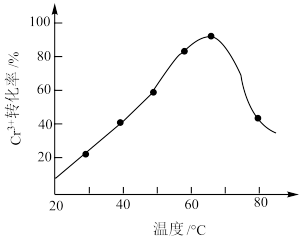
(2)H2O2的作用是将滤液中的Cr3+转化为Cr2O ,控制其他条件不变,在相同时间内,测得温度对Cr3+转化率的影响如图所示。请分析温度超过70°C时,Cr3+转化率下降的原因是
,控制其他条件不变,在相同时间内,测得温度对Cr3+转化率的影响如图所示。请分析温度超过70°C时,Cr3+转化率下降的原因是_______ 。
(3)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
①滤渣II的主要成分为_______ (填化学式)。
②用NaOH调节溶液的pH不能超过8,其理由是_______ 。
(4)在“除杂II”中,当溶液中镁离子和钙离子沉淀完全时,所得溶液中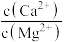 =
=_______ 。(已知:Ksp(CaF2)=1.48×10-10,Ksp(MgF2)=7.40×10-11)
(5)上述流程中,加入NaOH溶液后,溶液呈碱性,Cr2O 气转化为CrO
气转化为CrO ,写出上述流程中的“还原”过程生成CrOH(H2O)5SO4沉淀的离子方程式
,写出上述流程中的“还原”过程生成CrOH(H2O)5SO4沉淀的离子方程式_______ 。

已知:酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+等。
(1)酸浸时,为了提高浸取率可采取的措施有
(2)H2O2的作用是将滤液中的Cr3+转化为Cr2O
 ,控制其他条件不变,在相同时间内,测得温度对Cr3+转化率的影响如图所示。请分析温度超过70°C时,Cr3+转化率下降的原因是
,控制其他条件不变,在相同时间内,测得温度对Cr3+转化率的影响如图所示。请分析温度超过70°C时,Cr3+转化率下降的原因是
(3)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
| 阳离子 | Fe3+ | Al3+ | Mg2+ | Ca2+ |
| 开始沉淀时的pH | 1.5 | 3.4 | 8.9 | 11.9 |
| 沉淀完全时的pH | 2.8 | 4.7(>8溶解) | 10.9 | 14 |
②用NaOH调节溶液的pH不能超过8,其理由是
(4)在“除杂II”中,当溶液中镁离子和钙离子沉淀完全时,所得溶液中
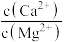 =
=(5)上述流程中,加入NaOH溶液后,溶液呈碱性,Cr2O
 气转化为CrO
气转化为CrO ,写出上述流程中的“还原”过程生成CrOH(H2O)5SO4沉淀的离子方程式
,写出上述流程中的“还原”过程生成CrOH(H2O)5SO4沉淀的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】工业上常以高硫锰矿(主要成分为MnS及少量的FeS2、钙盐及钠盐)为原料生产硫酸锰,焙烧过程中产生大量的硫的氧化物,一种改进型工艺流程如下:
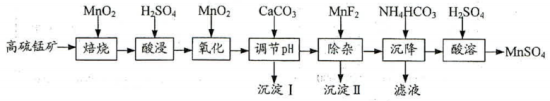
(1)“焙烧”加入Mn02的主要目的_____________________ 。
(2)“氧化”时反应的离子方程式_____________________ 。
(3)“沉淀I”的化学式是_____________________ 。
(4)在“除杂”时溶液的pH不能过低的可能原因是_____________________ 。
(5)确定“沉降”所得固体已洗涤干净的实验操作是_____________________ 。
(6)“沉降”后的滤液中阳离子主要是_____________________ 。

(1)“焙烧”加入Mn02的主要目的
(2)“氧化”时反应的离子方程式
(3)“沉淀I”的化学式是
(4)在“除杂”时溶液的pH不能过低的可能原因是
(5)确定“沉降”所得固体已洗涤干净的实验操作是
(6)“沉降”后的滤液中阳离子主要是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】硫酸亚铁晶体 是一种重要的食品或饲料添加剂.工业上采用硫铁矿焙烧去硫后的烧渣(主要成分为
是一种重要的食品或饲料添加剂.工业上采用硫铁矿焙烧去硫后的烧渣(主要成分为 、
、 、
、 、
、 ,不考虑其他杂质)制取硫酸亚铁晶体的流程如图所示:
,不考虑其他杂质)制取硫酸亚铁晶体的流程如图所示:
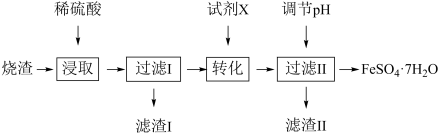
(1)烧渣要进行粉碎,目的是______________ 。
(2)滤渣I的主要成分是____________ (填化学式) 。
(3)“转化”是为了将溶液中的 转化为
转化为 。方法是向溶液中加入过量铁粉,其反应的离子方程式为
。方法是向溶液中加入过量铁粉,其反应的离子方程式为_____________ 。
(4)若检验滤液Ⅱ中不存在 ,可选择的操作方法是
,可选择的操作方法是_______________________ 。
(5)要得到 晶体的一系列具体操作是
晶体的一系列具体操作是_________ 、__________ 、过滤、洗涤、干燥,“过滤”所用到的玻璃仪器除了漏斗外还有__________ 、____________ 。
(6) 晶体应密封保存,主要目的是
晶体应密封保存,主要目的是________________ 。
 是一种重要的食品或饲料添加剂.工业上采用硫铁矿焙烧去硫后的烧渣(主要成分为
是一种重要的食品或饲料添加剂.工业上采用硫铁矿焙烧去硫后的烧渣(主要成分为 、
、 、
、 、
、 ,不考虑其他杂质)制取硫酸亚铁晶体的流程如图所示:
,不考虑其他杂质)制取硫酸亚铁晶体的流程如图所示:
(1)烧渣要进行粉碎,目的是
(2)滤渣I的主要成分是
(3)“转化”是为了将溶液中的
 转化为
转化为 。方法是向溶液中加入过量铁粉,其反应的离子方程式为
。方法是向溶液中加入过量铁粉,其反应的离子方程式为(4)若检验滤液Ⅱ中不存在
 ,可选择的操作方法是
,可选择的操作方法是(5)要得到
 晶体的一系列具体操作是
晶体的一系列具体操作是(6)
 晶体应密封保存,主要目的是
晶体应密封保存,主要目的是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】碱式氧化镍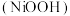 为镍氢电池的正极材料。黄钠铁矾的化学式为
为镍氢电池的正极材料。黄钠铁矾的化学式为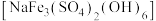 被用做净水剂。用含镍废渣(主要成分为
被用做净水剂。用含镍废渣(主要成分为 、
、 ,还含有少量的
,还含有少量的 、
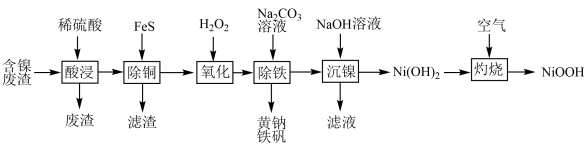
、 等杂质)为主要原料联合制取碱式氧化镍和黄钠铁矾的工艺流程如图所示。
等杂质)为主要原料联合制取碱式氧化镍和黄钠铁矾的工艺流程如图所示。
已知:部分金属硫化物的溶度积常数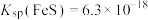 ;
;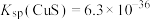 ;
;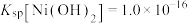 ,回答下列问题:
,回答下列问题:
(1)Fe元素在周期表的位置__________________________ 。
(2)“酸浸”后所得废渣的主要成分为__________ (填“化学式”);除铜步骤的离子方程式为_________________ 。
(3)“氧化”时,若用稀硝酸代替过氧化氢氧化 ,从反应产物的角度分析,稀硝酸代替过氧化氢的缺点是
,从反应产物的角度分析,稀硝酸代替过氧化氢的缺点是______________________ 。
(4)加入 溶液调节pH为3.7生成黄钠铁矾的离子方程式
溶液调节pH为3.7生成黄钠铁矾的离子方程式___________________ 。
(5)“沉镍”时,要使镍尽可能沉淀完全需调节溶液pH至少为___________ 。
(6)“灼烧”反应过程中氧化剂与还原剂的物质的量之比为_____________ 。
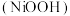 为镍氢电池的正极材料。黄钠铁矾的化学式为
为镍氢电池的正极材料。黄钠铁矾的化学式为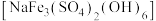 被用做净水剂。用含镍废渣(主要成分为
被用做净水剂。用含镍废渣(主要成分为 、
、 ,还含有少量的
,还含有少量的 、
、 等杂质)为主要原料联合制取碱式氧化镍和黄钠铁矾的工艺流程如图所示。
等杂质)为主要原料联合制取碱式氧化镍和黄钠铁矾的工艺流程如图所示。
已知:部分金属硫化物的溶度积常数
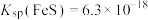 ;
; ;
;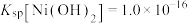 ,回答下列问题:
,回答下列问题:(1)Fe元素在周期表的位置
(2)“酸浸”后所得废渣的主要成分为
(3)“氧化”时,若用稀硝酸代替过氧化氢氧化
 ,从反应产物的角度分析,稀硝酸代替过氧化氢的缺点是
,从反应产物的角度分析,稀硝酸代替过氧化氢的缺点是(4)加入
 溶液调节pH为3.7生成黄钠铁矾的离子方程式
溶液调节pH为3.7生成黄钠铁矾的离子方程式(5)“沉镍”时,要使镍尽可能沉淀完全需调节溶液pH至少为
(6)“灼烧”反应过程中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】工业利用闪锌矿(主要成分 ,还含有
,还含有 、
、 、石英及
、石英及 、
、 等杂质)富氧酸浸提取锌,同时实现环保除铁的工艺流程如下:
等杂质)富氧酸浸提取锌,同时实现环保除铁的工艺流程如下:
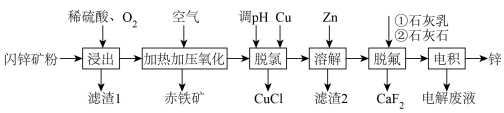
已知:①酸性条件下,亚铜离子易发生歧化反应;
② 易形成胶体。
易形成胶体。
回答下列问题:
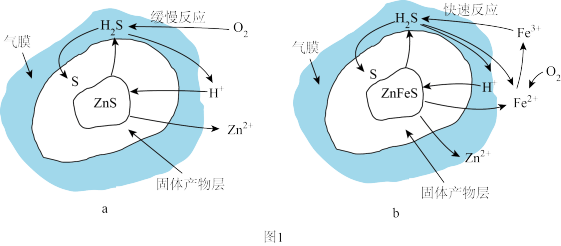
(1)“浸出”过程原理如图1a所示, “浸出”的总反应的化学方程式为
“浸出”的总反应的化学方程式为___________ 。对比人造闪锌矿浸出原理(如图1b所示),可知“浸出”过程中 的作用为
的作用为___________ 。
(2)“滤渣1”主要成分为___________ 。
(3)“加热加压氧化”发生反应的离子方程式为___________ 。
(4)“电积”时, 、
、 会腐蚀电极板,需提前除净。
会腐蚀电极板,需提前除净。
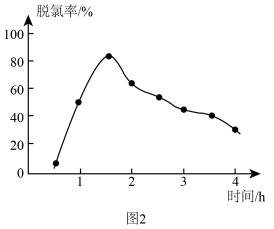
①“脱氯”时,脱氯率随时间变化如图2,约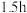 后脱氯率减小的原因可能为
后脱氯率减小的原因可能为___________ 。
②“脱氟时,先按物质的量之比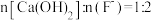 加入
加入 脱氟,充分反应后,
脱氟,充分反应后,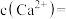
___________  [已知
[已知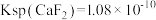 ,且不考虑
,且不考虑 沉淀];后加入石灰石,目的为
沉淀];后加入石灰石,目的为___________ 。
(5)写出“电积”生成锌的电极反应式___________ 。
 ,还含有
,还含有 、
、 、石英及
、石英及 、
、 等杂质)富氧酸浸提取锌,同时实现环保除铁的工艺流程如下:
等杂质)富氧酸浸提取锌,同时实现环保除铁的工艺流程如下:
已知:①酸性条件下,亚铜离子易发生歧化反应;
②
 易形成胶体。
易形成胶体。回答下列问题:
(1)“浸出”过程原理如图1a所示,
 “浸出”的总反应的化学方程式为
“浸出”的总反应的化学方程式为 的作用为
的作用为
(2)“滤渣1”主要成分为
(3)“加热加压氧化”发生反应的离子方程式为
(4)“电积”时,
 、
、 会腐蚀电极板,需提前除净。
会腐蚀电极板,需提前除净。①“脱氯”时,脱氯率随时间变化如图2,约
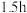 后脱氯率减小的原因可能为
后脱氯率减小的原因可能为
②“脱氟时,先按物质的量之比
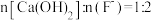 加入
加入 脱氟,充分反应后,
脱氟,充分反应后,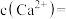
 [已知
[已知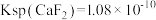 ,且不考虑
,且不考虑 沉淀];后加入石灰石,目的为
沉淀];后加入石灰石,目的为(5)写出“电积”生成锌的电极反应式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】以硫酸渣(含Fe2O3、SiO2等)为原料制备铁黄(FeOOH)的一种工艺流程如图:
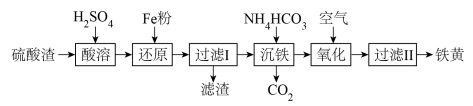
(1)“酸溶”中加快溶解的方法为___ (任意写出一种)。
(2)“还原”过程中的离子方程式为___ 。
(3)写出“滤渣”中主要成分的化学式___ 。
(4)①“沉铁”过程中生成Fe(OH)2的化学方程式为___ 。
②若用CaCO3“沉铁”,则生成FeCO3沉淀。当反应完成时,溶液中 =
=___ 。[已知Ksp(CaCO3)=2.8×10-9,Ksp(FeCO3)=2×10-11]
(5)“氧化”时,用NaNO2浓溶液代替空气氧化Fe(OH)2浆液,能缩短氧化时间,但缺点是___ 。
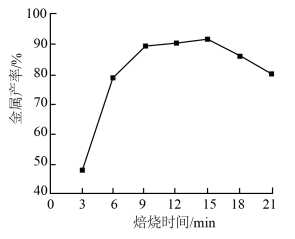
(6)焦炭还原硫酸渣炼铁能充分利用铁资源,在1225℃、 =1.2时,焙烧时间与金属产率的关系如图,时间超过15min金属产率下降的原因是
=1.2时,焙烧时间与金属产率的关系如图,时间超过15min金属产率下降的原因是___ 。

(1)“酸溶”中加快溶解的方法为
(2)“还原”过程中的离子方程式为
(3)写出“滤渣”中主要成分的化学式
(4)①“沉铁”过程中生成Fe(OH)2的化学方程式为
②若用CaCO3“沉铁”,则生成FeCO3沉淀。当反应完成时,溶液中
 =
=(5)“氧化”时,用NaNO2浓溶液代替空气氧化Fe(OH)2浆液,能缩短氧化时间,但缺点是
(6)焦炭还原硫酸渣炼铁能充分利用铁资源,在1225℃、
 =1.2时,焙烧时间与金属产率的关系如图,时间超过15min金属产率下降的原因是
=1.2时,焙烧时间与金属产率的关系如图,时间超过15min金属产率下降的原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】二氧化锗 可用于制备半导体材料,某实验小组以铁矾渣
可用于制备半导体材料,某实验小组以铁矾渣 主要成分为FeO、CaO、GeO和
主要成分为FeO、CaO、GeO和 等
等 为原料制取二氧化锗的工艺流程如下所示。
为原料制取二氧化锗的工艺流程如下所示。
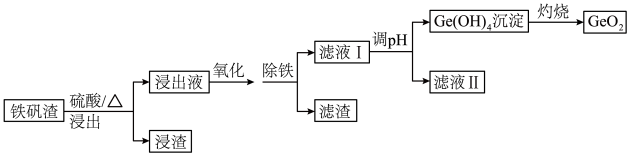
已知:25℃时,部分金属阳离子转化为氢氧化物沉淀时的pH如下表所示。
请回答下列问题:
(1)由下图可知,“浸出”时,所用硫酸的最佳质量分数为______ ,浸渣的主要成分为______ (填化学式 。
。

(2)“氧化”时,可选用的试剂为________ (填字母)。
A.KMnO4 B.NaOH C.H2O2 D.I2
(3)“氧化”时,若以适量稀硝酸作氧化剂,则Ge2+被氧化的离子方程式为_________ 。
(4)“除铁”时,可选用Na2CO3为除铁剂,其原理用离子方程式表示为___________ 。
(5)若Ge4+沉淀完全时的浓度为1×10-5mol/L,根据表中数据计算25℃时Ge(OH)4的Ksp=_____ 。
(6)利用惰性电极电解酸性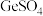 溶液也可制得
溶液也可制得 ,则阳极的电极反应式为
,则阳极的电极反应式为_________ 。
 可用于制备半导体材料,某实验小组以铁矾渣
可用于制备半导体材料,某实验小组以铁矾渣 主要成分为FeO、CaO、GeO和
主要成分为FeO、CaO、GeO和 等
等 为原料制取二氧化锗的工艺流程如下所示。
为原料制取二氧化锗的工艺流程如下所示。
已知:25℃时,部分金属阳离子转化为氢氧化物沉淀时的pH如下表所示。
离子 |  | 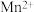 | 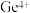 |
开始沉淀时的pH |  |  |  |
沉淀完全时的pH |  |  | 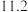 |
(1)由下图可知,“浸出”时,所用硫酸的最佳质量分数为
 。
。
(2)“氧化”时,可选用的试剂为
A.KMnO4 B.NaOH C.H2O2 D.I2
(3)“氧化”时,若以适量稀硝酸作氧化剂,则Ge2+被氧化的离子方程式为
(4)“除铁”时,可选用Na2CO3为除铁剂,其原理用离子方程式表示为
(5)若Ge4+沉淀完全时的浓度为1×10-5mol/L,根据表中数据计算25℃时Ge(OH)4的Ksp=
(6)利用惰性电极电解酸性
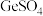 溶液也可制得
溶液也可制得 ,则阳极的电极反应式为
,则阳极的电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】以菱锰矿 主要成分
主要成分 ,还含有
,还含有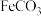 、
、 等杂质
等杂质 为原料制备二氧化锰的工艺流程如下:
为原料制备二氧化锰的工艺流程如下:
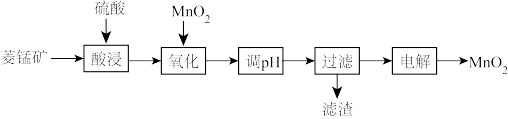
已知部分金属离子开始沉淀及沉淀完全时的pH如下表所示:
(1)①“酸浸”时 发生反应的离子方程式为
发生反应的离子方程式为________________________________________ 。
②“酸浸”过程中加入过量硫酸的目的除了加快酸浸的速率、_____________ 、___________ 。
③要提高“酸浸”的速率,还可以采取的方法是________________________________________ 。
(2)“氧化”时发生反应的离子方程式为________________________________________ 。
(3)“调pH”的目的是除去溶液中的杂质金属离子,“调pH”的范围应为_______________ 。
(4)当溶液中c(Al3+)≤10-5mol/L时,则认为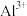 沉淀完全,则
沉淀完全,则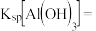
______________ 。
 主要成分
主要成分 ,还含有
,还含有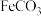 、
、 等杂质
等杂质 为原料制备二氧化锰的工艺流程如下:
为原料制备二氧化锰的工艺流程如下: 
已知部分金属离子开始沉淀及沉淀完全时的pH如下表所示:
| 金属离子 | 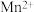 |  |  | 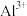 |
| 开始沉淀时的pH |  | 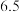 | 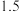 |  |
| 沉淀完全时的pH |  | 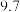 |  | 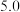 |
(1)①“酸浸”时
 发生反应的离子方程式为
发生反应的离子方程式为②“酸浸”过程中加入过量硫酸的目的除了加快酸浸的速率、
③要提高“酸浸”的速率,还可以采取的方法是
(2)“氧化”时发生反应的离子方程式为
(3)“调pH”的目的是除去溶液中的杂质金属离子,“调pH”的范围应为
(4)当溶液中c(Al3+)≤10-5mol/L时,则认为
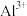 沉淀完全,则
沉淀完全,则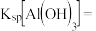
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
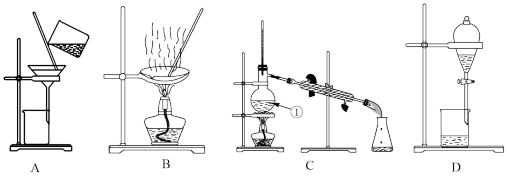
(1)从氯化钠溶液中得到氯化钠固体,选择装置_______ (填代表装置图的字母,下同);
(2)除去自来水中的等杂质,选择装置_______ ;
(3)检验自来水中 是否除净的方法为:取少量锥形瓶中的水于洁净试管中,滴加
是否除净的方法为:取少量锥形瓶中的水于洁净试管中,滴加_______ 、_______ (写化学式)溶液,不产生白色沉淀表明 已除净;
已除净;
(4)从碘水中富集 ,选择装置
,选择装置_______ ,该方法的名称为_______ 。
(5)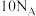 个
个 气体分子在标准状况下的体积为
气体分子在标准状况下的体积为_______ ,将这些标况下 气体溶于635mL水中,所得盐酸的密度为
气体溶于635mL水中,所得盐酸的密度为 。试计算:
。试计算:
①所得盐酸的质量分数和物质的量浓度分别是_______ 、_______ 。
②取出这种盐酸100 mL,稀释至1.18L,所得稀盐酸的物质的量浓度是_______ 。
③取②稀释后的稀盐酸50mL,与65g锌粒充分反应生成的 在标准状况下的体积是
在标准状况下的体积是_______ L(假设气体没有损失)。

(1)从氯化钠溶液中得到氯化钠固体,选择装置
(2)除去自来水中的等杂质,选择装置
(3)检验自来水中
 是否除净的方法为:取少量锥形瓶中的水于洁净试管中,滴加
是否除净的方法为:取少量锥形瓶中的水于洁净试管中,滴加 已除净;
已除净;(4)从碘水中富集
 ,选择装置
,选择装置(5)
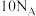 个
个 气体分子在标准状况下的体积为
气体分子在标准状况下的体积为 气体溶于635mL水中,所得盐酸的密度为
气体溶于635mL水中,所得盐酸的密度为 。试计算:
。试计算:①所得盐酸的质量分数和物质的量浓度分别是
②取出这种盐酸100 mL,稀释至1.18L,所得稀盐酸的物质的量浓度是
③取②稀释后的稀盐酸50mL,与65g锌粒充分反应生成的
 在标准状况下的体积是
在标准状况下的体积是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】已知 H2O2、KMnO4、NaClO、K2Cr2O7均具有强氧化性。将溶液中的Cu2+、Fe2+、Fe3+沉淀为氢氧化物,需溶液的pH分别为6.4、9.6、3.7。现有含FeCl2杂质的氯化铜晶体(CuCl2∙2H2O),为制取纯净的CuCl2∙2H2O,首先将其制成水溶液,然后按图示步骤进行提纯:
(1)本实验最适合的氧化剂X是___________(填序号)。
(2)物质Y可以选择以下___________。
(3)本实验用加碱沉淀法能不能达到目的?___________ (填“能”或“不能”)。
(4)加氧化剂的目的是___________ 。
(5)最后蒸发结晶要想得到CuCl2∙2H2O晶体,应如何操作?___________ 。
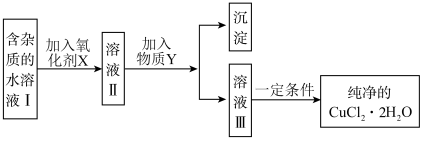
(1)本实验最适合的氧化剂X是___________(填序号)。
| A.K2Cr2O7 | B.NaClO | C. H2O2 | D.KMnO4 |
(2)物质Y可以选择以下___________。
| A.CuO | B.CuSO4 | C.Cu(OH)2 | D.KOH |
(3)本实验用加碱沉淀法能不能达到目的?
(4)加氧化剂的目的是
(5)最后蒸发结晶要想得到CuCl2∙2H2O晶体,应如何操作?
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,溶于水成绿色,难溶于乙醇,见光分解,是一些有机反应的催化剂。制备三草酸合铁酸钾主要有两步,制备FeC2O4黄色沉淀,并在K2C2O4、H2C2O4并存时氧化FeC2O4制得产品:
(NH4)2Fe(SO4)2·6H2O+H2C2O4 FeC2O4·2H2O↓+(NH4)2SO4+H2SO4+4H2O
FeC2O4·2H2O↓+(NH4)2SO4+H2SO4+4H2O
2 FeC2O4·2H2O+H2O2+3K2C2O4+H2C2O4 2K3Fe(C2O4)3·3H2O
2K3Fe(C2O4)3·3H2O
(1) K3[Fe(C2O4)3]·3H2O (三草酸合铁酸钾)铁元素化合价为______ 。
(2)实验时需要滴加1mol·L-1H2SO4溶液,配制该溶液需要的玻璃仪器有玻璃棒、胶头滴管、容量瓶、______ 和______ 。
(3)用如图装置制备FeC2O4·2H2O时,药品添加的顺序是:______ (填序号),加热溶解后再滴入草酸。
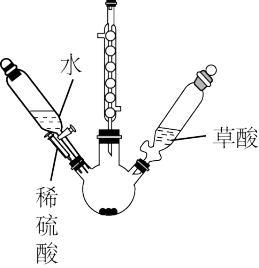
A.先加入硫酸,再滴入水 B.先滴入水,再加入硫酸
(4)制备三草酸合铁酸钾,保持温度为40℃左右,原因是______ 。观察到______ 现象时,反应结束,此时加热至沸,主要的目的是______ (用化学方程式表示)。然后冷却至室温,加入______ (填化学式)和硝酸钾固体,搅拌,洗出亮绿色晶体。
(NH4)2Fe(SO4)2·6H2O+H2C2O4
 FeC2O4·2H2O↓+(NH4)2SO4+H2SO4+4H2O
FeC2O4·2H2O↓+(NH4)2SO4+H2SO4+4H2O2 FeC2O4·2H2O+H2O2+3K2C2O4+H2C2O4
 2K3Fe(C2O4)3·3H2O
2K3Fe(C2O4)3·3H2O(1) K3[Fe(C2O4)3]·3H2O (三草酸合铁酸钾)铁元素化合价为
(2)实验时需要滴加1mol·L-1H2SO4溶液,配制该溶液需要的玻璃仪器有玻璃棒、胶头滴管、容量瓶、
(3)用如图装置制备FeC2O4·2H2O时,药品添加的顺序是:

A.先加入硫酸,再滴入水 B.先滴入水,再加入硫酸
(4)制备三草酸合铁酸钾,保持温度为40℃左右,原因是
您最近一年使用:0次



