用软锰矿(MnO2)、黄铁矿(FeS2)酸浸生产硫酸锰(MnSO4),并进一步电解制取二氧化锰(EMD)的工艺流程如下:
I. 将软锰矿、黄铁矿和硫酸按一定比例放入反应釜中,搅拌,加热保温反应一定时间。
II. 向反应釜中加入MnO2、CaCO3试剂,再加入Na2S溶液除掉浸出液中的重金属。
III. 过滤,向滤液中加入净化剂进一步净化,再过滤,得到精制MnSO4溶液。
IV. 将精制MnSO4溶液送入电解槽,电解制得EMD。
请回答下列问题:
(1)步骤I中搅拌、加热的目的是_____ 。完成酸浸过程中反应的离子方程式:
( ) FeS2+( ) MnO2+( ) ___ =( ) Mn2++( ) Fe2++S+SO42-+( ) __
(2) 加入CaCO3将浸出液pH调至pH=5,从而除掉铁,请解释用CaCO3除铁的原 :_______ 。(结合离子方程式解释)
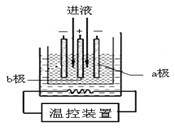
(3)步骤IV中用如图所示的电解装置电解精制的MnSO4溶液,生成EMD的是_______ 极(填“a”或“b”),生成EMD的电极反应式是____ 。
(4)EMD可用作碱性锌锰电池的材料。已知碱性锌锰电池的反应式为:Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2。
下列关于碱性锌锰电池的说法正确的是_____ (填字母序号)。[来源
A.碱性锌锰电池是二次电池
B.碱性锌锰电池将化学能转化为电能
C.正极反应为:2MnO2+2H2O+2e-=2MnOOH+2OH-
D.碱性锌锰电池工作时,电子由MnO2经外电路流向Zn极
I. 将软锰矿、黄铁矿和硫酸按一定比例放入反应釜中,搅拌,加热保温反应一定时间。
II. 向反应釜中加入MnO2、CaCO3试剂,再加入Na2S溶液除掉浸出液中的重金属。
III. 过滤,向滤液中加入净化剂进一步净化,再过滤,得到精制MnSO4溶液。
IV. 将精制MnSO4溶液送入电解槽,电解制得EMD。
请回答下列问题:
(1)步骤I中搅拌、加热的目的是
(2) 加入CaCO3将浸出液pH调至pH=5,从而除掉铁,请解释用CaCO3除铁的原 :
(3)步骤IV中用如图所示的电解装置电解精制的MnSO4溶液,生成EMD的是

(4)EMD可用作碱性锌锰电池的材料。已知碱性锌锰电池的反应式为:Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2。
下列关于碱性锌锰电池的说法正确的是
A.碱性锌锰电池是二次电池
B.碱性锌锰电池将化学能转化为电能
C.正极反应为:2MnO2+2H2O+2e-=2MnOOH+2OH-
D.碱性锌锰电池工作时,电子由MnO2经外电路流向Zn极
更新时间:2017-02-17 06:59:02
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】现有M、Q、R、T、W、X、Y、Z八种前四周期常见元素,原子序数依次递增。其中,M具有一种没有中子的同位素;Q是植物生长三要素之一;R是地壳中含量最多的元素,且W与R的最外层电子数相同;T、Y、Z是金属元素,其中T的原子半径是短周期中最大的,能与X形成离子化合物TX;Y既不是主族元素、也不是副族元素,其合金被称为“黑色金属”;Z的单质在空气中被锈蚀后会生成翠绿色的化合物。请回答下列问题:
(1)Y在周期表中的位置___________ ;
(2)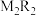 的电子式为
的电子式为___________ ;M、Q能形成一种阳离子,该阳离子能与W的简单离子能形成一种2:1的离子化合物,请写出该化合物的电子式___________ 。
(3)非金属性X___________ W(填“>”“=”或“<”),请用化学方程式说明该事实___________ ;
(4)写出Z的单质在浓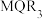 溶液中反应的离子方程式
溶液中反应的离子方程式___________ ,若Z的单质过量,则产物气体的成分可能是___________ 。
(1)Y在周期表中的位置
(2)
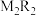 的电子式为
的电子式为(3)非金属性X
(4)写出Z的单质在浓
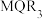 溶液中反应的离子方程式
溶液中反应的离子方程式
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】合理处理金属垃圾既可以保护环境又可以节约资源。利用废旧镀锡铜线制备胆矾并回收锡的流程如下:
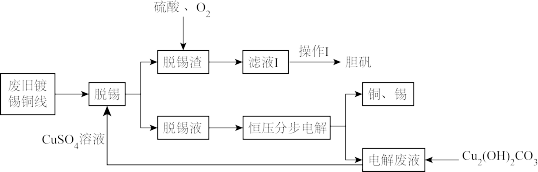
已知Sn2+容易水解。
回答下列问题:
(1)加快“脱锡”速率的措施有_______ (写出一点)。“操作I” 包含_______ 、_______ 、过滤、洗涤、干燥。
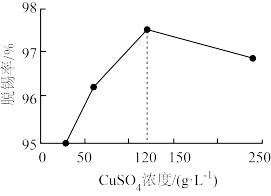
(2)“脱锡”过程中加入少量稀硫酸调控溶液pH,其目的是_______ ;硫酸铜浓度与脱锡率的关系如图所示,当浓度大于120g·L-1时,脱锡率下降的原因_______ 。
(3)“脱锡液”中含有的离子主要为Cu2+、Sn2+、H+、SO ,以石墨为电极,通过控制溶液pH、电解时电压,可以依次回收铜、锡。电解时阳极反应式为
,以石墨为电极,通过控制溶液pH、电解时电压,可以依次回收铜、锡。电解时阳极反应式为_______ ; 当阴极出现_______ 的现象时,说明电解回收锡结束。
(4)“脱锡渣”溶于硫酸的离子方程式为_______ 。
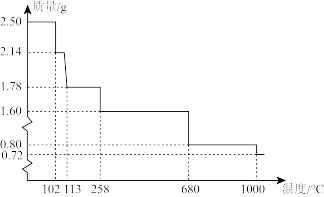
(5)称量纯净的胆矾2.50g进行热重分析,实验测得胆矾的热重曲线如图所示。则120℃时所得固体的化学式为_______ 。

已知Sn2+容易水解。
回答下列问题:
(1)加快“脱锡”速率的措施有
(2)“脱锡”过程中加入少量稀硫酸调控溶液pH,其目的是

(3)“脱锡液”中含有的离子主要为Cu2+、Sn2+、H+、SO
 ,以石墨为电极,通过控制溶液pH、电解时电压,可以依次回收铜、锡。电解时阳极反应式为
,以石墨为电极,通过控制溶液pH、电解时电压,可以依次回收铜、锡。电解时阳极反应式为(4)“脱锡渣”溶于硫酸的离子方程式为
(5)称量纯净的胆矾2.50g进行热重分析,实验测得胆矾的热重曲线如图所示。则120℃时所得固体的化学式为

您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
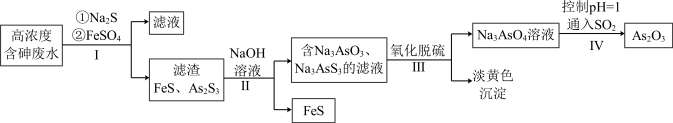
【推荐3】利用高浓度含砷废水(主要成分为H3AsO3)制取As2O3的工艺流程如下图所示。
已知:As2S3(s)+3S2-(aq) 2AsS33-(aq)
2AsS33-(aq)
(1)H3AsO3中As元素的化合价为______ ;H3AsO3的第一步电离方程式为:________ 。
(2)步骤I加入FeSO4的作用是______________________ 。
(3)步骤Ⅱ发生反应的化学方程式为___________________ 。步骤III“氧化脱硫”过程中被氧化的元素是___________ (填元素符号)。
(4)步骤IV发生反应的离子方程式为________________________ 。
(5)利用反应AsO43-+2I-+2H+ AsO33-+I2+H2O设计成原电池,起始时在甲、乙两池中分别加入图示药品并连接装置(a、b均为石墨电极)。
AsO33-+I2+H2O设计成原电池,起始时在甲、乙两池中分别加入图示药品并连接装置(a、b均为石墨电极)。
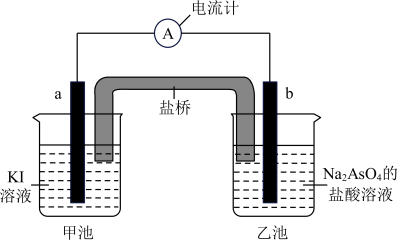
①起始时,b电极的电极反应式为__________________ 。
②一段时间后电流计指针不发生偏转。欲使指针偏转方向与起始时相反,可采取的措施是______________________________ (举一例)。

已知:As2S3(s)+3S2-(aq)
 2AsS33-(aq)
2AsS33-(aq)(1)H3AsO3中As元素的化合价为
(2)步骤I加入FeSO4的作用是
(3)步骤Ⅱ发生反应的化学方程式为
(4)步骤IV发生反应的离子方程式为
(5)利用反应AsO43-+2I-+2H+
 AsO33-+I2+H2O设计成原电池,起始时在甲、乙两池中分别加入图示药品并连接装置(a、b均为石墨电极)。
AsO33-+I2+H2O设计成原电池,起始时在甲、乙两池中分别加入图示药品并连接装置(a、b均为石墨电极)。
①起始时,b电极的电极反应式为
②一段时间后电流计指针不发生偏转。欲使指针偏转方向与起始时相反,可采取的措施是
您最近半年使用:0次
【推荐1】I.据报道,我国在南海北部神狐海域进行的可燃冰(甲烷的水合物)试采获得成功。甲烷是一种重要的化工原料。
(1)甲烷重整是提高甲烷利用率的重要方式,除部分氧化外还有以下两种:
水蒸气重整:CH4(g)+H2O(g) CO(g)+3H2(g) △H1=+205.9kJ·mol-1①
CO(g)+3H2(g) △H1=+205.9kJ·mol-1①
CO(g)+H2O(g) CO2(g)+H2(g) △H2=-41.2kJ·mol-1②
CO2(g)+H2(g) △H2=-41.2kJ·mol-1②
二氧化碳重整:CH4(g)+CO2(g) 2CO(g)+2H2(g) △H3③
2CO(g)+2H2(g) △H3③
则反应①自发进行的条件是____ ,△H3=____ kJ·mol-1。
II.氮的固定一直是科学家研究的重要课题,合成氨则是人工固氮比较成熟的技术,其原理为N2(g)+3H2(g) 2NH3(g)。
2NH3(g)。
(2)在不同温度、压强和相同催化剂条件下,初始N2、H2分别为0.1mol、0.3mol时,平衡后混合物中氮的体积分数(φ)如图所示。
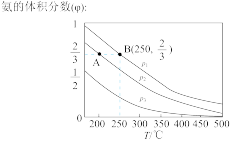
①其中,p1、p2和p3由大到小的顺序是____ ,其原因是____ 。
②若分别用VA(N2)和VB(N2)表示从反应开始至达平衡状态A、B时的化学反应速率,则VA(N2)____ VB(N2)(填“>”“<”或“=”)。
③若在250℃、p1为104Pa条件下,反应达到平衡时容器的体积为1L,则该条件下B点N2的分压p(N2)为_____ Pa(分压=总压×物质的量分效,保留一位小数)。
III.以连二硫酸根(S2O )为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
)为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
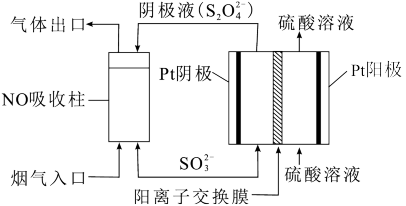
(3)①阴极区的电极反应式为____ 。
②NO吸收转化后的主要产物为NH ,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标况下的体积为
,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标况下的体积为____ mL。
(1)甲烷重整是提高甲烷利用率的重要方式,除部分氧化外还有以下两种:
水蒸气重整:CH4(g)+H2O(g)
 CO(g)+3H2(g) △H1=+205.9kJ·mol-1①
CO(g)+3H2(g) △H1=+205.9kJ·mol-1①CO(g)+H2O(g)
 CO2(g)+H2(g) △H2=-41.2kJ·mol-1②
CO2(g)+H2(g) △H2=-41.2kJ·mol-1②二氧化碳重整:CH4(g)+CO2(g)
 2CO(g)+2H2(g) △H3③
2CO(g)+2H2(g) △H3③则反应①自发进行的条件是
II.氮的固定一直是科学家研究的重要课题,合成氨则是人工固氮比较成熟的技术,其原理为N2(g)+3H2(g)
 2NH3(g)。
2NH3(g)。(2)在不同温度、压强和相同催化剂条件下,初始N2、H2分别为0.1mol、0.3mol时,平衡后混合物中氮的体积分数(φ)如图所示。

①其中,p1、p2和p3由大到小的顺序是
②若分别用VA(N2)和VB(N2)表示从反应开始至达平衡状态A、B时的化学反应速率,则VA(N2)
③若在250℃、p1为104Pa条件下,反应达到平衡时容器的体积为1L,则该条件下B点N2的分压p(N2)为
III.以连二硫酸根(S2O
 )为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
)为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
(3)①阴极区的电极反应式为
②NO吸收转化后的主要产物为NH
 ,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标况下的体积为
,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标况下的体积为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】烟气的主要污染物为 和
和 ,是造成大气污染的重要因素,其治理方法主要有液体吸收法,固体吸收法,氧化反应法,电解法等。
,是造成大气污染的重要因素,其治理方法主要有液体吸收法,固体吸收法,氧化反应法,电解法等。
(1)一种基于吸收剂区分的同时脱硫脱硝反应的装置如图所示。反应器I吸收 ,反应器II吸收
,反应器II吸收 ,隔绝空气反应一段时间。
,隔绝空气反应一段时间。

①当观察到反应器I中悬浊液变澄清时,反应的离子方程式_______ 。
②反应器II中所发生的反应为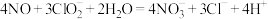 ,盛有
,盛有
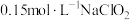 溶液最多能吸收
溶液最多能吸收 (标准状况下)的体积为
(标准状况下)的体积为_______
③已知: 溶液中含氯组分的百分含量(δ)随
溶液中含氯组分的百分含量(δ)随 变化如图1所示,其他条件相同,
变化如图1所示,其他条件相同, 溶液中脱硝效率随溶液初始
溶液中脱硝效率随溶液初始 的变化如图2所示。
的变化如图2所示。
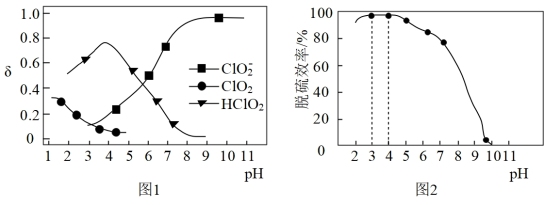
脱硝过程中,起脱硝作用的有效成分为_______ (填化学式)。将NaClO2溶液的pH从4调节至3的过程中,脱硝效率几乎不变的原因是_______ 。
(2)隔膜电解同时脱硫脱硝的装置如图所示,其中电极A、B均为惰性电极,电解液为稀硫酸。为了提高脱除效率,将阴极室的溶液pH调至4~7,则阴极上的电极反应为_______ 。

 和
和 ,是造成大气污染的重要因素,其治理方法主要有液体吸收法,固体吸收法,氧化反应法,电解法等。
,是造成大气污染的重要因素,其治理方法主要有液体吸收法,固体吸收法,氧化反应法,电解法等。(1)一种基于吸收剂区分的同时脱硫脱硝反应的装置如图所示。反应器I吸收
 ,反应器II吸收
,反应器II吸收 ,隔绝空气反应一段时间。
,隔绝空气反应一段时间。
①当观察到反应器I中悬浊液变澄清时,反应的离子方程式
②反应器II中所发生的反应为
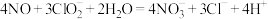 ,盛有
,盛有
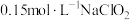 溶液最多能吸收
溶液最多能吸收 (标准状况下)的体积为
(标准状况下)的体积为③已知:
 溶液中含氯组分的百分含量(δ)随
溶液中含氯组分的百分含量(δ)随 变化如图1所示,其他条件相同,
变化如图1所示,其他条件相同, 溶液中脱硝效率随溶液初始
溶液中脱硝效率随溶液初始 的变化如图2所示。
的变化如图2所示。
脱硝过程中,起脱硝作用的有效成分为
(2)隔膜电解同时脱硫脱硝的装置如图所示,其中电极A、B均为惰性电极,电解液为稀硫酸。为了提高脱除效率,将阴极室的溶液pH调至4~7,则阴极上的电极反应为

您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】锡酸钠(Na2SnO3·xH2O)主要用作电镀铜锡合金和碱性镀锡的基本原料。锡精矿除含SnO2外,还含有少量WO3、S、As、Fe,—种由锡精矿制备锡酸钠的工艺流程如下:
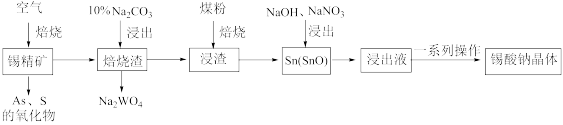
已知:①焙烧后,S、As变为挥发性氧化物而被除去,Fe变为Fe3O4;
②Na2SnO3•xH2O。易溶于水,其在水中的溶解度随着温度的升高而降低。
请回答下列问题:
(1)Sn元素的原子序数为50,其在周期表中的位置为_____________ 。
(2)从“焙烧渣”中除去Fe3O4最简单的方法为_____________ 。加入煤粉焙烧可将SnO2还原为Sn或SnO,Sn或SnO。在碱性条件下均能被NaNO3氧化为Na2SnO3,已知NaNO3的还原产物为NH3,则NaNO3氧化Sn的化学方程式为___________________ 。
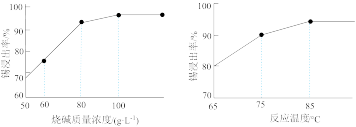
(3)如图为加入NaOH溶液和NaNO3溶液浸出时锡的浸出率与NaOH质量浓度和反应温度间的关系图,则“碱浸”的最适宜条件为_____________ 、___________ ,
(4)从浸出液中获得锡酸钠晶体的“一系列操作”具体是指___________ 、洗涤、干燥。
(5)采用热重分析法测定锡酸钠晶体样品所含结晶水数,将样品加热到140℃时,失掉全部结晶水,失重约20.2%。锡酸钠晶体的化学式为__________ 。
(6)以纯锡为阳极材料,以NaOH和Na2SnO3为电解液,待镀金属为阴极材料,可实现在待镀金属上的持续镀锡,镀锡时阳极的电极反应式为______________ 。

已知:①焙烧后,S、As变为挥发性氧化物而被除去,Fe变为Fe3O4;
②Na2SnO3•xH2O。易溶于水,其在水中的溶解度随着温度的升高而降低。
请回答下列问题:
(1)Sn元素的原子序数为50,其在周期表中的位置为
(2)从“焙烧渣”中除去Fe3O4最简单的方法为
(3)如图为加入NaOH溶液和NaNO3溶液浸出时锡的浸出率与NaOH质量浓度和反应温度间的关系图,则“碱浸”的最适宜条件为

(4)从浸出液中获得锡酸钠晶体的“一系列操作”具体是指
(5)采用热重分析法测定锡酸钠晶体样品所含结晶水数,将样品加热到140℃时,失掉全部结晶水,失重约20.2%。锡酸钠晶体的化学式为
(6)以纯锡为阳极材料,以NaOH和Na2SnO3为电解液,待镀金属为阴极材料,可实现在待镀金属上的持续镀锡,镀锡时阳极的电极反应式为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献。
I.某探究活动小组在实验室模拟侯氏制碱法。试回答下列有关问题:
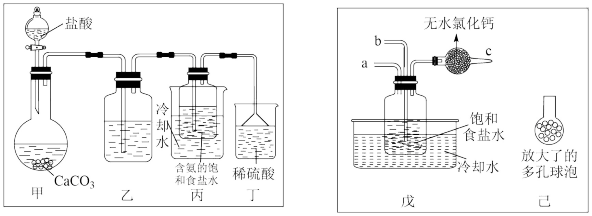
【方案一】一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如图所示(图中夹持、固定用的仪器未画出)。
(1)已知乙装置中的除杂试剂是____________ ,反应的离子方程式为__________________ 。
(2)丙中发生反应的化学方程式为:__________________ 。实验结束后,分离出 的操作是
的操作是______ (填分离操作的名称)。
【方案二】另一位同学用图中戊装置(其它装置未画出)进行实验。
(3)实验时,须先从a管通入______ 气体,再从b管中通入其他气体;
(4)有同学建议在戊装置的b管下端连接己装置,理由是________________________ 。
(5)制得 后获得纯碱的化学方程式为
后获得纯碱的化学方程式为______ ,实验室进行此操作的装置可以是图中的______ 。
A. B.
B. C.
C. D.
D.
II.工业纯碱中可能混有少量NaCl,同学们探究纯碱样品中是否含有NaCl
(6)根据实验结论补充实验操作和现象
I.某探究活动小组在实验室模拟侯氏制碱法。试回答下列有关问题:
【方案一】一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如图所示(图中夹持、固定用的仪器未画出)。

(1)已知乙装置中的除杂试剂是
(2)丙中发生反应的化学方程式为:
 的操作是
的操作是【方案二】另一位同学用图中戊装置(其它装置未画出)进行实验。
(3)实验时,须先从a管通入
(4)有同学建议在戊装置的b管下端连接己装置,理由是
(5)制得
 后获得纯碱的化学方程式为
后获得纯碱的化学方程式为A.
 B.
B. C.
C. D.
D.
II.工业纯碱中可能混有少量NaCl,同学们探究纯碱样品中是否含有NaCl
(6)根据实验结论补充实验操作和现象
实验操作 | 现象 | 结论 |
| ①取样品加水溶解,加入 | ② | 样品中有NaCl |
| ③向上述溶液中 | ④ |
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】已知岩脑砂的主要成分为NH4Cl,实验室可通过过量氨气和氯气反应制NH4Cl。
I.实验室制NH4Cl

(1)写出B中反应的离子方程式_________________________________ 。
(2)为使氨气和氯气在D中充分混合并反应,上述装置的连接顺序为a→d→c_____ 、______ ←j←i←h←g←b;写出D中反应的化学方程式_________________________________ 。
(3)若要检验NH4Cl,除蒸馏水、稀HNO3、AgNO3溶液、红色石蕊试纸外还需要的试剂为___________ 。
Ⅱ:天然岩脑砂中NH4Cl,纯度的测定(杂质不影响NH4Cl纯度测定)
已知:2NH4 C1+3CuO 3Cu+2HCl↑+N2↑+3H2O
3Cu+2HCl↑+N2↑+3H2O
实验步骤:①准确称取1.19g岩脑砂。②将岩脑砂与足量氧化铜混合加热(装置如下)。

(1)连接仪器,检查装置气密性:先将K中装入水,然后加热G,______________________ ,则气密性良好。
(2)H中浓硫酸的作用是_________________________________ 。
(3)实验结束后,恢复至原温,通过K测得气体体积为224mL(换算为标准状况),则天然岩脑砂中NH4C1的纯度为___________ 。(保留三位有效数字)
(4)某同学通过测I的增重来计算天然岩脑砂中NH4C1的质量分数,则所得NH4C1的纯度___________ 。(填“偏高”、“偏低”、“无影响”)
I.实验室制NH4Cl

(1)写出B中反应的离子方程式
(2)为使氨气和氯气在D中充分混合并反应,上述装置的连接顺序为a→d→c
(3)若要检验NH4Cl,除蒸馏水、稀HNO3、AgNO3溶液、红色石蕊试纸外还需要的试剂为
Ⅱ:天然岩脑砂中NH4Cl,纯度的测定(杂质不影响NH4Cl纯度测定)
已知:2NH4 C1+3CuO
 3Cu+2HCl↑+N2↑+3H2O
3Cu+2HCl↑+N2↑+3H2O实验步骤:①准确称取1.19g岩脑砂。②将岩脑砂与足量氧化铜混合加热(装置如下)。

(1)连接仪器,检查装置气密性:先将K中装入水,然后加热G,
(2)H中浓硫酸的作用是
(3)实验结束后,恢复至原温,通过K测得气体体积为224mL(换算为标准状况),则天然岩脑砂中NH4C1的纯度为
(4)某同学通过测I的增重来计算天然岩脑砂中NH4C1的质量分数,则所得NH4C1的纯度
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】工业上采用软锰矿(主要成分为MnO2)来制取硫酸锰,工艺流程如下:
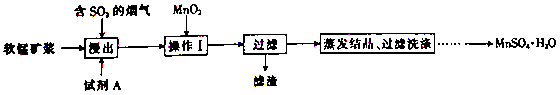
已知:浸出液中的金属离子主要是Mn2+,还含有少量的Fe2+。回答下列问题:
(1)实验室进行过滤操作时用到的玻璃仪器有玻璃棒、烧杯和______ 。
(2)浸出后,锰主要以Mn2+的形式存在,写出MnO2与SO2反应的离子方程式:____________ 。
(3)浸出过程的副反应之一是部分SO2被氧化为硫酸,致使浸出液的pH下降,这将不利于软锰矿浆继续吸收SO2。欲消除生成的硫酸,可选用的试剂A是______ (填字母)。
A.MnCO3 B.MnO2 C.Mn(OH)2 D.MnSO4
(4)操作I的目的是__________ 和调节溶液的pH至3~4。检验过滤后的滤液中是否含有Fe3+的操作是_______________ 。

已知:浸出液中的金属离子主要是Mn2+,还含有少量的Fe2+。回答下列问题:
(1)实验室进行过滤操作时用到的玻璃仪器有玻璃棒、烧杯和
(2)浸出后,锰主要以Mn2+的形式存在,写出MnO2与SO2反应的离子方程式:
(3)浸出过程的副反应之一是部分SO2被氧化为硫酸,致使浸出液的pH下降,这将不利于软锰矿浆继续吸收SO2。欲消除生成的硫酸,可选用的试剂A是
A.MnCO3 B.MnO2 C.Mn(OH)2 D.MnSO4
(4)操作I的目的是
您最近半年使用:0次



