用Zn(主要含有Fe、Al、Pb杂质)和硫酸来制取H2,利用制氢废液制备硫酸锌晶体(ZnSO4·7H2O)、Al2O3和Fe2O3,流程如下:
已知Al3+、Fe3+、Zn2+的氢氧化物完全沉淀的pH分别为5.2、4.1和8.5,ZnSO4·7H2O晶体易溶于水,易风化。回答下列问题:
(1)调节pH=2的目的是______________ ,调节pH=2,可加入_________ (填化学式)。
(2)写出生成沉淀3的化学方程式:______________________ 。
(3)加热浓缩ZnSO4溶液出现极薄品膜时,要停止加热的主要原因是_____________ 。
(4)某同学用如图所示的装置抽滤。
①有关抽滤的说法正确的是__________ 。
A.抽滤的目的主要是得到较干燥的沉淀
B.滤纸的直径应略小于漏斗内径,又能盖住全部小孔
C.图中有一处出错
D.抽滤结束,从吸滤瓶的支管口倒出滤液
②抽滤,洗涤沉淀的具体操作是___________________________ 。
(5)为得到干燥的ZnSO4·7H2O产品,选择干燥方法是________ 。
A.加热烘干 B.用浓H2SO4干燥
C.用酒精洗干 D.在空气中自然干燥
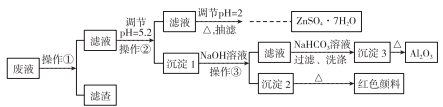
已知Al3+、Fe3+、Zn2+的氢氧化物完全沉淀的pH分别为5.2、4.1和8.5,ZnSO4·7H2O晶体易溶于水,易风化。回答下列问题:
(1)调节pH=2的目的是
(2)写出生成沉淀3的化学方程式:
(3)加热浓缩ZnSO4溶液出现极薄品膜时,要停止加热的主要原因是
(4)某同学用如图所示的装置抽滤。
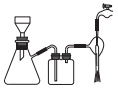
①有关抽滤的说法正确的是
A.抽滤的目的主要是得到较干燥的沉淀
B.滤纸的直径应略小于漏斗内径,又能盖住全部小孔
C.图中有一处出错
D.抽滤结束,从吸滤瓶的支管口倒出滤液
②抽滤,洗涤沉淀的具体操作是
(5)为得到干燥的ZnSO4·7H2O产品,选择干燥方法是
A.加热烘干 B.用浓H2SO4干燥
C.用酒精洗干 D.在空气中自然干燥
2017·浙江·一模 查看更多[1]
(已下线)2017届浙江省高三“超级全能生”3月联考(选考科目)化学试卷
更新时间:2017-04-01 09:00:37
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】定量分析钾铬矾晶体[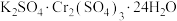 ,相对分子质量为998]的热分解过程。取
,相对分子质量为998]的热分解过程。取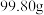 钾铬矾样品不断加热,样品受热分解过程的热重曲线(固体质量随温度变化的曲线)如图所示。已知:
钾铬矾样品不断加热,样品受热分解过程的热重曲线(固体质量随温度变化的曲线)如图所示。已知: 为两性氧化物。
为两性氧化物。
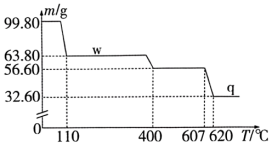
(1) 时固体w的化学式为
时固体w的化学式为______________________ 。
(2)在 时得到固体产物q及气体R,气体R能全部被盐酸酸化的
时得到固体产物q及气体R,气体R能全部被盐酸酸化的 溶液吸收并得到白色沉淀。固体q可部分溶于水,过滤后得到固体e和滤液f,向滤液f中加入盐酸酸化的
溶液吸收并得到白色沉淀。固体q可部分溶于水,过滤后得到固体e和滤液f,向滤液f中加入盐酸酸化的 溶液也得到白色沉淀;将固体e置于适量的
溶液也得到白色沉淀;将固体e置于适量的 溶液中恰好反应得到澄清溶液,则固体q的成分是
溶液中恰好反应得到澄清溶液,则固体q的成分是______________________ (填化学式),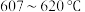 时发生反应的化学方程式为
时发生反应的化学方程式为______________________ 。
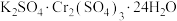 ,相对分子质量为998]的热分解过程。取
,相对分子质量为998]的热分解过程。取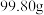 钾铬矾样品不断加热,样品受热分解过程的热重曲线(固体质量随温度变化的曲线)如图所示。已知:
钾铬矾样品不断加热,样品受热分解过程的热重曲线(固体质量随温度变化的曲线)如图所示。已知: 为两性氧化物。
为两性氧化物。
(1)
 时固体w的化学式为
时固体w的化学式为(2)在
 时得到固体产物q及气体R,气体R能全部被盐酸酸化的
时得到固体产物q及气体R,气体R能全部被盐酸酸化的 溶液吸收并得到白色沉淀。固体q可部分溶于水,过滤后得到固体e和滤液f,向滤液f中加入盐酸酸化的
溶液吸收并得到白色沉淀。固体q可部分溶于水,过滤后得到固体e和滤液f,向滤液f中加入盐酸酸化的 溶液也得到白色沉淀;将固体e置于适量的
溶液也得到白色沉淀;将固体e置于适量的 溶液中恰好反应得到澄清溶液,则固体q的成分是
溶液中恰好反应得到澄清溶液,则固体q的成分是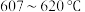 时发生反应的化学方程式为
时发生反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】某中学化学兴趣小组为了调查当地某一湖泊的水质污染情况,在注入湖泊的3个主要水源的入口处采集水样,并进行了分析,给出了如下实验信息:其中一处水源含有A、B两种物质,一处含有C、D两种物质,一处含有E物质,A、B、C、D、E为五种常见化合物,均由下表中的离子形成,其中C中有两种阳离子,C常用作净水剂。
为了鉴别上述化合物。分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中都能产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)写出A、B的化学式:A_______ ,B_______ 。
(2)将含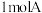 的溶液与含
的溶液与含 的溶液反应后蒸干,仅得到一种化合物,该化合物的化学式为
的溶液反应后蒸干,仅得到一种化合物,该化合物的化学式为_______ 。
(3)在A溶液中加入足量澄清石灰水,其离子方程式为_______ 。
(4)若向含溶质 的C溶液中逐滴加入
的C溶液中逐滴加入 溶液,生成沉淀质量最大为
溶液,生成沉淀质量最大为_______  。
。
| 阳离子 |     |
| 阴离子 |     |
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中都能产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)写出A、B的化学式:A
(2)将含
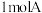 的溶液与含
的溶液与含 的溶液反应后蒸干,仅得到一种化合物,该化合物的化学式为
的溶液反应后蒸干,仅得到一种化合物,该化合物的化学式为(3)在A溶液中加入足量澄清石灰水,其离子方程式为
(4)若向含溶质
 的C溶液中逐滴加入
的C溶液中逐滴加入 溶液,生成沉淀质量最大为
溶液,生成沉淀质量最大为 。
。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】我国芒硝( )储量居世界第一,由芒硝制备
)储量居世界第一,由芒硝制备 具有重要价值。
具有重要价值。
I.以芒硝和石灰石为原料生产 、
、 和轻质
和轻质 的主要流程如图。
的主要流程如图。
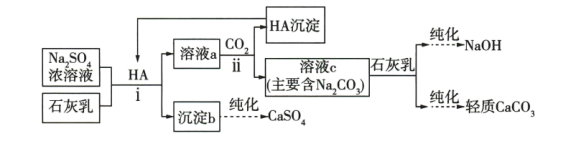
(1)i、ii中涉及的分离操作是_______ 。
(2)原料石灰石经反应:____ 、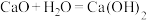 ,可获得流程中所需的
,可获得流程中所需的 和石灰乳。
和石灰乳。
(3) 是一种弱酸,在上述流程中可以循环使用。已知温度相同时,溶解度:
是一种弱酸,在上述流程中可以循环使用。已知温度相同时,溶解度: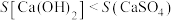 。
。
①从平衡移动的角度解释HA在i中反应中起到的作用:_______ 。
②本流程中还利用了 的性质是
的性质是_______ 。
(4)溶液c中会含有少量 ,但不会影响钠的利用率,原因是
,但不会影响钠的利用率,原因是_____ (用化学方程式表示)。
II.利用电解法制备 (如图所示)。
(如图所示)。
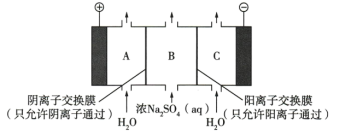
(5)产生 的电极反应是
的电极反应是_______ , 在
在_______ (填“A”或“C”)区生成。
 )储量居世界第一,由芒硝制备
)储量居世界第一,由芒硝制备 具有重要价值。
具有重要价值。I.以芒硝和石灰石为原料生产
 、
、 和轻质
和轻质 的主要流程如图。
的主要流程如图。
(1)i、ii中涉及的分离操作是
(2)原料石灰石经反应:
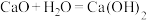 ,可获得流程中所需的
,可获得流程中所需的 和石灰乳。
和石灰乳。(3)
 是一种弱酸,在上述流程中可以循环使用。已知温度相同时,溶解度:
是一种弱酸,在上述流程中可以循环使用。已知温度相同时,溶解度: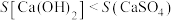 。
。①从平衡移动的角度解释HA在i中反应中起到的作用:
②本流程中还利用了
 的性质是
的性质是(4)溶液c中会含有少量
 ,但不会影响钠的利用率,原因是
,但不会影响钠的利用率,原因是II.利用电解法制备
 (如图所示)。
(如图所示)。
(5)产生
 的电极反应是
的电极反应是 在
在
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】A、B、C、D均为中学化学常见的纯净物且都含有一种相同元素,A是单质,B是A的氧化物。它们有如图反应关系:
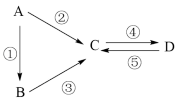
(1)若B是淡黄色固体,②③的反应中均有一种相同的反应物且摩尔质量为18 ,D俗称小苏打。则C的化学式为
,D俗称小苏打。则C的化学式为___________ ,由D和少量澄清石灰水反应可得到苏打,写出该反应的离子方程式___________ 。
(2)若B是红棕色固体,反应③在盐酸中完成,则反应②中加入物质的化学式为___________ ;若C、D组成元素相同,且无其他元素参与相互转化,则C转化为D的离子方程式为___________ ;在D中滴入氢氧化钠溶液,一段时间内观察到的现象是___________ 。

(1)若B是淡黄色固体,②③的反应中均有一种相同的反应物且摩尔质量为18
 ,D俗称小苏打。则C的化学式为
,D俗称小苏打。则C的化学式为(2)若B是红棕色固体,反应③在盐酸中完成,则反应②中加入物质的化学式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】A、B、C、D、E、F为常见的原子序数依次增大的短周期元素,B、C、D、E、F的简单离子的电子层结构相同,A和E同主族,且原子的最外层电子数的关系为A+D=B+F=8。请回答:
(1)试写出由上述元素组成的分子中含有4个原子核且为18电子结构的物质的化学式_______ 。
(2)含F的阳离子溶液中加过量E的最高价氧化物对应水化物的溶液,其离子方程式是_______ 。
(3)已知B2A4与BA3具有相似的性质,B2A4通过炽热的氧化铜粉末,粉末由黑色变为红色,且产物对大气无污染,其化学反应方程式是_______ 。
(4)已知某化合物EB3与水可以反应生成两种气体单质和一种碱,试写出其化学方程式_______ ;若0.1mol该化合物完全反应,转移电子的物质的量为_______ 。
(1)试写出由上述元素组成的分子中含有4个原子核且为18电子结构的物质的化学式
(2)含F的阳离子溶液中加过量E的最高价氧化物对应水化物的溶液,其离子方程式是
(3)已知B2A4与BA3具有相似的性质,B2A4通过炽热的氧化铜粉末,粉末由黑色变为红色,且产物对大气无污染,其化学反应方程式是
(4)已知某化合物EB3与水可以反应生成两种气体单质和一种碱,试写出其化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】A、B、C、D均为中学化学中常见的单质或化合物,它们之间的关系如图所示(部分产物已略去)。
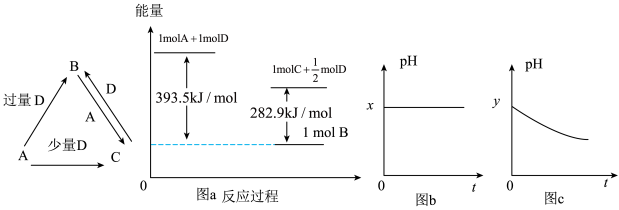
(1)若A为金属单质,D是某强酸的稀溶液,则反应C+D→B的离子方程式为____________________ 。
(2)若A、B为盐,D为强碱,A的水溶液显酸性,则①C的化学式为_________________ ;②反应B+A→C的离子方程式为______________________ ;
(3)若A为强碱,D为气态氧化物。常温时,将B的水溶液露置于空气中,其pH随时间t变化可能如上图的图b或图c所示(不考虑D的溶解和水的挥发)。
①若图b符合事实,则D为____________ (填化学式),此时图b中x___________ 7(填“﹥”“﹤”“﹦”)②若图c符合事实,则其pH变化的原因是________________ (用离子方程式表示)。
(4)若A为非金属单质,D是空气的主要成分之一。它们之间转化时能量变化如上图a,请写出A+D→C的热化学方程式:________________________________ 。

(1)若A为金属单质,D是某强酸的稀溶液,则反应C+D→B的离子方程式为
(2)若A、B为盐,D为强碱,A的水溶液显酸性,则①C的化学式为
(3)若A为强碱,D为气态氧化物。常温时,将B的水溶液露置于空气中,其pH随时间t变化可能如上图的图b或图c所示(不考虑D的溶解和水的挥发)。
①若图b符合事实,则D为
(4)若A为非金属单质,D是空气的主要成分之一。它们之间转化时能量变化如上图a,请写出A+D→C的热化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐3】IA、B、C、D均为中学化学中常见的物质,它们之间转化关系如下图(部分产物已略去):
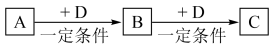
试回答:
(1)若D是具有氧化性的单质,则属于主族的金属A为___________ (填元素符号)
(2)若D是金属,C溶液在储存时应加入少最D,其理由是(用必要的文字和离子方程式表示)_____________________ ;
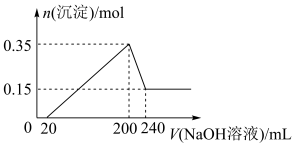
(3)若A、B、C为含同一种金属元素的无机化合物.在溶液中A和C反应生成B。请写出B转化为C的所有可能的离子力程式_________________________________________ 。化合物B经过一系列反应可以得到单质E,将一定质量的Mg和E的混合物投入500mL稀硫酸中,固体全部溶解并产生气体。待反应完全后.向所得溶液中加入NaOH溶液,生成沉淀的物质的是与加入溶液的体积关系如下图所示。则固体混合物中Mg的质量为_____________ ;NaOH溶液的物质的量浓度为___________ 。
II某一离子反应体系有反应物和产物共以下六种: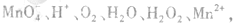
已知该反应中的H2O2只发生如下过程:
(1)该反应中的还原剂是___________ 。
(2)该反应中发生还原反应的过程是_____ →_____ 。
(3)溶液随着酸性的增强氧化性不断增强,应选择__________ (选填“稀硫酸”或“浓盐酸”)进行KMnO4溶液的酸化。
(4)如反应转移了0.6mol电子,则产生的气体在标准状况下体积为__________ 。

试回答:
(1)若D是具有氧化性的单质,则属于主族的金属A为
(2)若D是金属,C溶液在储存时应加入少最D,其理由是(用必要的文字和离子方程式表示)
(3)若A、B、C为含同一种金属元素的无机化合物.在溶液中A和C反应生成B。请写出B转化为C的所有可能的离子力程式

II某一离子反应体系有反应物和产物共以下六种:
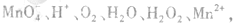
已知该反应中的H2O2只发生如下过程:

(1)该反应中的还原剂是
(2)该反应中发生还原反应的过程是
(3)溶液随着酸性的增强氧化性不断增强,应选择
(4)如反应转移了0.6mol电子,则产生的气体在标准状况下体积为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】次磷酸(H3PO2)是一种精细化工产品,是一元中强酸,具有较强还原性。回答下列问题:
(1)H3PO2及其与足量氢氧化钠反应生成的NaH2PO2均可将溶液中的Ag+还原为Ag,从而可用于化学镀银。
①在H3PO2中,磷元素的化合价为________ 在酸性环境中,利用(H3PO2)进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,则氧化产物为:________ (填化学式)。
②NaH2PO2是________ (填“正盐”或“酸式盐”),其溶液中离子浓度由大到小的顺序应为________
(2)次磷酸(H3PO2)可以通过电解的方法制备.工作原理如下图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):

①写出阳极的电极反应式________
②分析产品室可得到H3PO2的原因________ (结合一定的文字分析)
(1)H3PO2及其与足量氢氧化钠反应生成的NaH2PO2均可将溶液中的Ag+还原为Ag,从而可用于化学镀银。
①在H3PO2中,磷元素的化合价为
②NaH2PO2是
(2)次磷酸(H3PO2)可以通过电解的方法制备.工作原理如下图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):

①写出阳极的电极反应式
②分析产品室可得到H3PO2的原因
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐2】碳酸锰是制取其他含锰化合物的原料,也可用作脱硫的催化剂等。一种焙烧氯化铵和菱锰矿粉制备高纯度碳酸锰的工艺流程如图所示
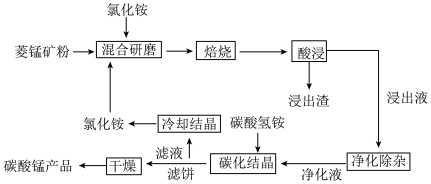
已知①菱锰矿粉的主要成分是MnCO3,还有少量的Fe、Al、Ca、Mg等元素
②常温下,相关金属离子在浓度为0.1mol/L时形成M(OH)n沉淀的pH范围如表
回答下列问题:
(1)“混合研磨”的作用为_______________________
(2)“焙烧”时发生的主要反应的化学方程式为_________________________________
(3)分析图1、图2,焙烧氯化铵、菱锰矿粉的最佳条件是_____________________________

(4)净化除杂流程如下
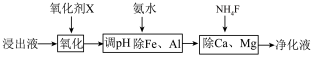
①已知几种物质氧化能力的强弱顺序为(NH4)2S2O8>KMnO4>MnO2>Fe3+,则氧化剂X宜选择__________
A.(NH4)2S2O8 B.MnO2 C.KMnO4
②调节pH时,pH可取的范围为_________________
(5)“碳化结晶”过程中不能用碳酸铵代替碳酸氢铵,可能的原因是__________________

已知①菱锰矿粉的主要成分是MnCO3,还有少量的Fe、Al、Ca、Mg等元素
②常温下,相关金属离子在浓度为0.1mol/L时形成M(OH)n沉淀的pH范围如表
| 金属离子 | Al3+ | Fe3+ | Fe2+ | Ca2+ | Mn2+ | Mg2+ |
| 开始沉淀的pH | 3.8 | 1.5 | 6.3 | 10.6 | 8.8 | 9.6 |
| 沉淀完全的pH | 5.2 | 2.8 | 8.3 | 12.6 | 10.8 | 11.6 |
回答下列问题:
(1)“混合研磨”的作用为
(2)“焙烧”时发生的主要反应的化学方程式为
(3)分析图1、图2,焙烧氯化铵、菱锰矿粉的最佳条件是

(4)净化除杂流程如下

①已知几种物质氧化能力的强弱顺序为(NH4)2S2O8>KMnO4>MnO2>Fe3+,则氧化剂X宜选择
A.(NH4)2S2O8 B.MnO2 C.KMnO4
②调节pH时,pH可取的范围为
(5)“碳化结晶”过程中不能用碳酸铵代替碳酸氢铵,可能的原因是
您最近一年使用:0次


 反应的化学方程式为
反应的化学方程式为 由铜和浓硫酸反应制得,化学方程式为
由铜和浓硫酸反应制得,化学方程式为

