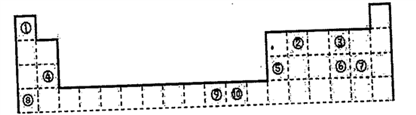
下表为长式周期表的一部分,其中的编号代表对应的元素。
(1)写出元素⑤的原子轨道表示式______________ 。
(2)写出元素⑨的基态原子的价电子排布式_________ 。
(3)表中属于ds区的元素是_________ (填编号)
(4)元素⑩形成的单质是由____ 键形成的晶体,该晶体采取的堆积方式是_______ ,晶体中⑩元素原子的配位数是_________ 。
(5)元素④、⑤、⑥、⑦的离子半径由小到大的顺序是_______ (用离子符号表示)
(6)写出元素①和元素⑧形成化合物的电子式_________________ 。
(7)元素⑨与⑩的第二电离能分别为:I⑨=1753kJ/mol,I⑩=1959kJ/mol,第二电离能I⑨⑩的原因是____________________________ 。
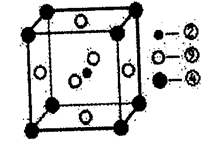
(8)科学家发现,②、④、⑨三种元素的原子形成的晶体具有超导性,其晶胞的结构特点如下图所示(图中②、④、⑨分别位于晶胞的体心、顶点、面心),则该化合物的化学式为______ (用对应的元素符号表示)。
(1)写出元素⑤的原子轨道表示式
(2)写出元素⑨的基态原子的价电子排布式
(3)表中属于ds区的元素是
(4)元素⑩形成的单质是由
(5)元素④、⑤、⑥、⑦的离子半径由小到大的顺序是
(6)写出元素①和元素⑧形成化合物的电子式
(7)元素⑨与⑩的第二电离能分别为:I⑨=1753kJ/mol,I⑩=1959kJ/mol,第二电离能I⑨⑩的原因是
(8)科学家发现,②、④、⑨三种元素的原子形成的晶体具有超导性,其晶胞的结构特点如下图所示(图中②、④、⑨分别位于晶胞的体心、顶点、面心),则该化合物的化学式为
更新时间:2017-04-26 16:57:29
|
相似题推荐
填空题
|
较难
(0.4)
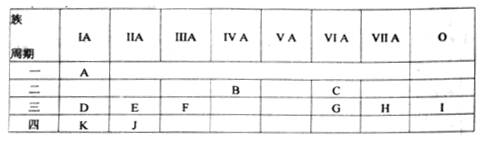
【推荐1】下表是元素周期表的一部分,列出11种元素在周期表中的位置,填写下列空白。
(1)第三周期元素中,原子半径最大的元素是(稀有气体除外)______ ,离子半径最小的是____ (写元素符号)。
(2)J的简单离子的结构示意图__________ 。
(3)D、E、F、K四元素的最高价氧化物对应水化物,按碱性依次减弱顺序排列为(写化学式)____ 。
(4)比较G、H两元素的最高价氧化物对应水化物的酸性______ (写化学式,下同)。比较C、G两元素的气态氢化物稳定性_________ 。
(1)第三周期元素中,原子半径最大的元素是(稀有气体除外)
(2)J的简单离子的结构示意图
(3)D、E、F、K四元素的最高价氧化物对应水化物,按碱性依次减弱顺序排列为(写化学式)
(4)比较G、H两元素的最高价氧化物对应水化物的酸性
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】硒的原子序数为34,是硫的同主族元素,硒的单质及其化合物用途非常广泛。
(1)硒位于周期表第___ ,周期___ 族。Se2Cl2常用作分析试剂,其电子式为_____ 。
(2)硒化铟是一种可应用于未来超算设备的新型半导体材料。已知铟(In)与铝同族且比铝多两个电子层。下列说法正确的是_____ (填字母)。
A.原子半径:In>Se B.In的金属性比Se强
C.In的金属性比Al弱 D.硒化铟的化学式为InSe2
(3)工业上常从电冶铜的阳极泥中提取纳米硒。向浆化的阳极泥中通入氯气,Cu2Se被溶液中的HClO氧化为H2SeO3及CuCl2,反应中HClO与Cu2Se的物质的量之比为___ 。用氨水中和亚硒酸后得到亚硒酸铵,再向( NH4)2SeO3溶液中加入Na2S2O3可得到纳米硒,同时生成亚硫酸盐,(NH4)2SeO3与Na2S2O3反应生成纳米硒的离子方程式为______ 。
(1)硒位于周期表第
(2)硒化铟是一种可应用于未来超算设备的新型半导体材料。已知铟(In)与铝同族且比铝多两个电子层。下列说法正确的是
A.原子半径:In>Se B.In的金属性比Se强
C.In的金属性比Al弱 D.硒化铟的化学式为InSe2
(3)工业上常从电冶铜的阳极泥中提取纳米硒。向浆化的阳极泥中通入氯气,Cu2Se被溶液中的HClO氧化为H2SeO3及CuCl2,反应中HClO与Cu2Se的物质的量之比为
您最近一年使用:0次
填空题
|
较难
(0.4)
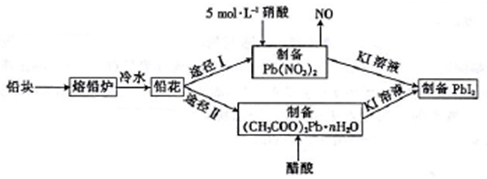
【推荐3】铅及并化合物在工业生产中具有非常广泛的用途,根据以下流程回答相关问题。
(1)铅是碳的同族元素,且比碳多4个电子层,则铅位于元素周期表第___ 周期__ 族。
(2)反位条件的控制在工业生产中有着极其重要的作用。把铅块制成铅花的目的是_______ 。途径I中不用14 mol·L-1的浓硝酸制备硝酸铅的原因是______________________ 。
(3)写出(CH3COO)2Pb溶液[(CH3COO)2Pb 为弱电解质]与KI溶液反应的离子方程式:_________ 。
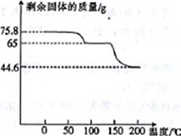
(4)取75.8 g (CH3COO)2Pb • nH2O样品在N2气氛中加热,测得剩余固体质量随温度的变化如图所示(样品在75℃时已完全失去结晶水)。
①(CH3COO)2Pb • nH2O中n=______ 。
②150~200℃间分解产物为PbO和一种有机物M,M能与水反应生成乙酸,则该温度区间内分解反应的化学方程式为________________________________ 。
(5)T℃时,取一定量的PbI2固体,用蒸馏水配制成饱和溶液。准确移取25.00mL PbI2饱和溶液,分次加入阳离子交换树脂RH(发生反应:2RH+Pb2+==R2Pb+2H+)中,用250 mL洁净的锥形瓶接受流出液,用蒸馏水淋洗树脂至流出液呈中性。将洗涤液一并盛放到锥形瓶中,加入酚酞,用0.0025 mol·L-1的NaOH溶液滴定,重复上述操作2次,当达到滴定终点时,平均消耗氢氧化钠溶液20.00 mL。则T℃时PbI2的Ksp=_______________________ 。
(1)铅是碳的同族元素,且比碳多4个电子层,则铅位于元素周期表第
(2)反位条件的控制在工业生产中有着极其重要的作用。把铅块制成铅花的目的是
(3)写出(CH3COO)2Pb溶液[(CH3COO)2Pb 为弱电解质]与KI溶液反应的离子方程式:
(4)取75.8 g (CH3COO)2Pb • nH2O样品在N2气氛中加热,测得剩余固体质量随温度的变化如图所示(样品在75℃时已完全失去结晶水)。
①(CH3COO)2Pb • nH2O中n=
②150~200℃间分解产物为PbO和一种有机物M,M能与水反应生成乙酸,则该温度区间内分解反应的化学方程式为
(5)T℃时,取一定量的PbI2固体,用蒸馏水配制成饱和溶液。准确移取25.00mL PbI2饱和溶液,分次加入阳离子交换树脂RH(发生反应:2RH+Pb2+==R2Pb+2H+)中,用250 mL洁净的锥形瓶接受流出液,用蒸馏水淋洗树脂至流出液呈中性。将洗涤液一并盛放到锥形瓶中,加入酚酞,用0.0025 mol·L-1的NaOH溶液滴定,重复上述操作2次,当达到滴定终点时,平均消耗氢氧化钠溶液20.00 mL。则T℃时PbI2的Ksp=
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】已知原子序数依次增大的X、Y、Z、D、E、F六种前四周期元素。X是宇宙中最丰富的元素;Y和Z基态原子的未成对电子数均等于周期序数;D的氧化物是典型的两性氧化物;E是所在周期中电负性最大的元素;F的单质是一种紫红色金属,在潮湿空气中该金属表面会慢慢生成一种绿色固体。请回答下列问题(用元素符号或化学式表示):
(1)X元素位于周期表的________ 区。
(2)基态D原子的价电子轨道表示式是______ ,其第一电离能反常地低于同周期前一种元素,原因是_______ 。
(3)YZ2分子的电子式是__________ ,该分子的空间构型是_____________ 。
(4)甲是由X、Y、Z三种原子构成的含有16个电子的分子,甲中Y原子的杂化类型是_______ ,它能溶于水的原因是______________ 。
(5)金属F与XE的热浓溶液反应产物之一是X3[FE4],该反应的化学方程式是______________ 。
(6)F与Z形成的一种晶胞结构如图,其中F原子均匀地分散在立方体内部,原子a、b、d的坐标参数依次为(0,0,0)、( ,
, ,
, )、(3m,3m,3m),则m=
)、(3m,3m,3m),则m=________ 。已知该晶体的密度为ρg/cm3, NA是阿伏伽德罗常数值,则原子b和d之间的核间距是__________ nm(列出计算式即可)。
(1)X元素位于周期表的
(2)基态D原子的价电子轨道表示式是
(3)YZ2分子的电子式是
(4)甲是由X、Y、Z三种原子构成的含有16个电子的分子,甲中Y原子的杂化类型是
(5)金属F与XE的热浓溶液反应产物之一是X3[FE4],该反应的化学方程式是
(6)F与Z形成的一种晶胞结构如图,其中F原子均匀地分散在立方体内部,原子a、b、d的坐标参数依次为(0,0,0)、(
 ,
, ,
, )、(3m,3m,3m),则m=
)、(3m,3m,3m),则m=
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】X、Y、Z、W、U五种元素,均位于周期表的前四周期,它们的核电荷数依次增加,且核电荷数之和为57.Y原子的L层p轨道中有2个电子,Z的原子核外有三个未成对电子,W与Y原子的价电子数相同,U原子的K层电子数与最外层电子数之比为2:1,其d轨道处于全充满状态.
(1)U2+的外围电子排布式为________ .
(2)X、Y、Z 可以形成化学式为XYZ的分子.该分子中各原子均达到稀有气体稳定结构,则该分子中Y采取的杂化轨道类型为__________ .
(3)比较Y和W的第一电离能,较大的是__________ (填元素符号).
(4)X与Z形成的最简单化合物Q的分子构型为__________ ;
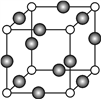
(5)U+与Z3﹣形成的晶胞结构如图所示,阴、阳离子间的核间距为acm.与同一个Z3﹣相连的U+有________ 个,该晶体的密度为__________ g·cm﹣3.(设NA表示阿伏伽德罗常数)
(1)U2+的外围电子排布式为
(2)X、Y、Z 可以形成化学式为XYZ的分子.该分子中各原子均达到稀有气体稳定结构,则该分子中Y采取的杂化轨道类型为
(3)比较Y和W的第一电离能,较大的是

(4)X与Z形成的最简单化合物Q的分子构型为
(5)U+与Z3﹣形成的晶胞结构如图所示,阴、阳离子间的核间距为acm.与同一个Z3﹣相连的U+有
您最近一年使用:0次
【推荐3】钒(V)、 锰(Mn)、铁(Fe)、 砷(As)、硒(Se)均为第四周期的元素,完成下列问题。
(1)钒有+2、+3、+4、+5等几种化合价。这几种价态中,最稳定的是______ 。
(2)基态Fe2+的价层电子的轨道表示式为________ ,检验Fe3+可以用KSCN溶液,写出SCN-的一种等电子体分子_______ 。
(3)部分电离能数据如下:
Mn: =717kJ/mol ,
=717kJ/mol , =1509kJ/mol ,
=1509kJ/mol , =3248kJ/mol ,
=3248kJ/mol ,
Fe: =759kJ/mol,
=759kJ/mol, =1562kJ/mol ,
=1562kJ/mol , =2957kJ/mol ,
=2957kJ/mol ,
根据数据可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难,其原因是____________________ 。
(4)沸点:NH3__________ AsH3(填“>”、“<”或“=”),原因是_____________________ 。
(5)H2SeO4和H2SeO3是硒的两种含氧酸,请根据结构与性质的关系,解释H2SeO4比H2SeO3酸性强的原因___________________________________ 。
(6)科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如下:

胆矾的化学式用配合物的形式表示为____________ 。
(1)钒有+2、+3、+4、+5等几种化合价。这几种价态中,最稳定的是
(2)基态Fe2+的价层电子的轨道表示式为
(3)部分电离能数据如下:
Mn:
 =717kJ/mol ,
=717kJ/mol , =1509kJ/mol ,
=1509kJ/mol , =3248kJ/mol ,
=3248kJ/mol ,Fe:
 =759kJ/mol,
=759kJ/mol, =1562kJ/mol ,
=1562kJ/mol , =2957kJ/mol ,
=2957kJ/mol ,根据数据可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难,其原因是
(4)沸点:NH3
(5)H2SeO4和H2SeO3是硒的两种含氧酸,请根据结构与性质的关系,解释H2SeO4比H2SeO3酸性强的原因
(6)科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如下:

胆矾的化学式用配合物的形式表示为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大。其中A原子核外有三个未成对电子;A与B可形成离子化合物B3A2;C元素是地壳中含量最高的金属元素;D原子核外的M层中有两对成对电子;E原子核外最外层只有1个电子,其余各层电子均充满。请根据以上信息,回答下列问题(答题时,A、B、C、D、E用所对应的元素符号表示):
(1)A、B、C、D的第一电离能由小到大的顺序为____________________________________ 。
(2)B的氯化物的熔点远高于C的氯化物的熔点,理由是________________________ ;
(3)A的最高价含氧酸根离子中,其中心原子采取____________ 杂化,D的低价氧化物分子的空间构型是___________________________ 。
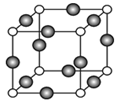
(4)A、E形成某种化合物的晶胞结构如图所示,则其化学式为________________ ;(每个球均表示1个原子) 若相邻A原子和E原子间的距离为a nm,阿伏伽德罗常数为NA,则该晶体的密度为_____________ g/cm3(用含a、NA的符号表示)。
(1)A、B、C、D的第一电离能由小到大的顺序为
(2)B的氯化物的熔点远高于C的氯化物的熔点,理由是
(3)A的最高价含氧酸根离子中,其中心原子采取
(4)A、E形成某种化合物的晶胞结构如图所示,则其化学式为

您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】2022年2月我国科学家在《科学》杂志发表反型钙钛矿太阳能电池研究方面的最新科研成果论文,为钙钛矿电池研究开辟新方向。
(1)基态钛原子的py原子轨道上的电子数为_______ 个。 与钛同周期的第ⅡA族和ⅢA族两种元素中第一电离能较大的是_______ (写 元素符号)。。
(2)Ti的配合物有多种。在Ti(CO)6、T(H2O) 和TiF
和TiF 三种微粒的配体中,所含原子电负性由大到小排序后,排第3位的元素是
三种微粒的配体中,所含原子电负性由大到小排序后,排第3位的元素是_______ (写元素符号), Ti(H2O) 中∠H-O-H
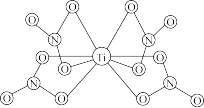
中∠H-O-H_______ (填大于、小于或等于)单个水分子中∠H-O-H,原因为_______ ; Ti(NO3)4的球棍结构如图,Ti 的配位数是_______ ,N原子的杂化方式为_______ , 与NO 互为等电子体的分子为
互为等电子体的分子为_______ (写分子式)
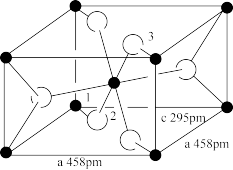
(3)钛白粉学名为二氧化钛,它是一种染料及颜料,其化学式为TiO2,如图为TiO2的晶胞结构图,回答:已知微粒1、2的坐标分别为(0,0, 0)和(0.31, 0.31, 0), 则微粒3的坐标为_______ ; 设阿伏加德罗常数的值为NA,TiO2的密度为_______ g·cm-3(列出计算式)。
(1)基态钛原子的py原子轨道上的电子数为
(2)Ti的配合物有多种。在Ti(CO)6、T(H2O)
 和TiF
和TiF 三种微粒的配体中,所含原子电负性由大到小排序后,排第3位的元素是
三种微粒的配体中,所含原子电负性由大到小排序后,排第3位的元素是 中∠H-O-H
中∠H-O-H 互为等电子体的分子为
互为等电子体的分子为
(3)钛白粉学名为二氧化钛,它是一种染料及颜料,其化学式为TiO2,如图为TiO2的晶胞结构图,回答:已知微粒1、2的坐标分别为(0,0, 0)和(0.31, 0.31, 0), 则微粒3的坐标为

您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】环烷酸金属(Cu、Ni、Co、Sn、Zn)盐常作为合成聚氨酯过程中的有效催化剂。回答下列问题:
(1)基态Cu原子的价电子排布___________ 。
(2)镍的氨合离子 中存在的化学键有
中存在的化学键有___________ 。
A.离子键 B.共价键 C.配位键 D.氢键 E. 键 F.
键 F. 键
键
(3)Ni、Co的第五电离能: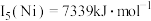 ,
,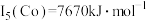 ,
,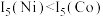 ,其原因是
,其原因是___________ 。
(4)锡元素可形成白锡、灰锡、脆锡三种单质。其中灰锡晶体与金刚石结构相似,但灰锡不如金刚石稳定,其原因是___________ 。
(5)硒化锌晶胞结构如图所示,其晶 胞参数为a pm。
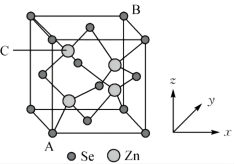
①相邻的 与
与 之间的距离为
之间的距离为___________ pm。
②已知原子坐标:A点为(0,0,0),B点为(1,1,1),则C点的原子坐标___________ 。
③若硒化锌晶体的密度为 ,则阿伏加德罗常数
,则阿伏加德罗常数
___________ (用含a、 的计算式表示)。
的计算式表示)。
(1)基态Cu原子的价电子排布
(2)镍的氨合离子
 中存在的化学键有
中存在的化学键有A.离子键 B.共价键 C.配位键 D.氢键 E.
 键 F.
键 F. 键
键(3)Ni、Co的第五电离能:
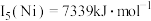 ,
,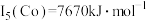 ,
,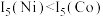 ,其原因是
,其原因是(4)锡元素可形成白锡、灰锡、脆锡三种单质。其中灰锡晶体与金刚石结构相似,但灰锡不如金刚石稳定,其原因是
(5)硒化锌晶胞结构如图所示,其晶 胞参数为a pm。

①相邻的
 与
与 之间的距离为
之间的距离为②已知原子坐标:A点为(0,0,0),B点为(1,1,1),则C点的原子坐标
③若硒化锌晶体的密度为
 ,则阿伏加德罗常数
,则阿伏加德罗常数
 的计算式表示)。
的计算式表示)。
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】为纪念1905年爱因斯坦连续发表6篇论文导致物理学大变革100周年,今年被定为国际物理年,本题涉及的“热电效应”机理也是爱因斯坦首先阐释的,即他提出的被后人称为“爱因斯坦振荡器”的独立振荡原子与温度关系的模型。
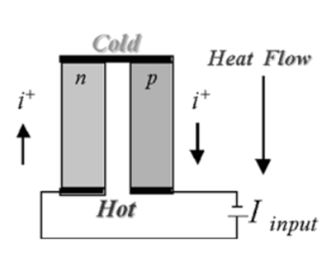
(1)如图是热电效应之一的图解。给出图中所有英文单词(或词组)及物理学符号的意义,并为此图写一篇不超过200字(包括标点符号等)的说明文_______ 。
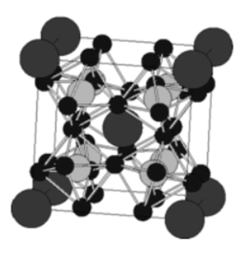
(2)如图是化学家合成的能实现热电效应的一种晶体的晶胞模型。图中的大原子是稀土原子,如镧;小原子是周期系第五主族元素,如锑;中等大小的原子是周期系VIII族元素,如铁,按如下结构图写出这种热电晶体的化学式_______ 。给出计算过程_______ 。提示:晶胞的6个面的原子数相同。设晶体中锑的氧化态为-1,镧的氧化态为+3,问:铁的平均氧化态多大_______ ?
(1)如图是热电效应之一的图解。给出图中所有英文单词(或词组)及物理学符号的意义,并为此图写一篇不超过200字(包括标点符号等)的说明文

(2)如图是化学家合成的能实现热电效应的一种晶体的晶胞模型。图中的大原子是稀土原子,如镧;小原子是周期系第五主族元素,如锑;中等大小的原子是周期系VIII族元素,如铁,按如下结构图写出这种热电晶体的化学式

您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】(1)一种铜金合金晶体具有面心立方最密堆积结构,在晶胞中Cu原子处于面心,Au原子处于顶点,则该合金中Cu原子与Au原子数量之比为__________ ;该晶体中原子之间的作用力是________ 。
(2)上述晶体具有储氢功能,氢原子可进入由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与CaF2(如图1)的结构相似,该晶体储氢后的化学式应为____________ 。
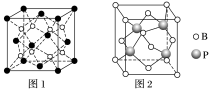
(3)立方BP(磷化硼)的晶胞结构如图2所示,晶胞中含B原子数目为________ 。
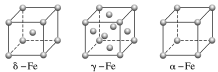
(4)铁有δ、γ、α三种同素异形体,γ晶体晶胞中所含有的铁原子数为________ ,δ、α两种晶胞中铁原子的配位数之比为________ 。
(2)上述晶体具有储氢功能,氢原子可进入由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与CaF2(如图1)的结构相似,该晶体储氢后的化学式应为

(3)立方BP(磷化硼)的晶胞结构如图2所示,晶胞中含B原子数目为
(4)铁有δ、γ、α三种同素异形体,γ晶体晶胞中所含有的铁原子数为

您最近一年使用:0次