下列实验方案正确且能达到预期目的的是
选项 | 实验方案 | 实验目的或结论 |
A | 将H2SO4酸化的H2O2滴入Fe(NO3)2溶液中,溶液变黄色 | 氧化性:H2O2比Fe3+强 |
B | 将SO2通入酸性高锰酸钾溶液中 | SO2具有漂白性 |
C | 取a g铝箔与足量氢氧化钠溶液充分反应,逸出的气体通过浓硫酸后,测其体积为V L(标况) | 测定铝箔中氧化铝的含量 |
D | 比较不同反应的反应热数据大小 | 判断反应速率大小 |
| A.A | B.B | C.C | D.D |
更新时间:2017-05-27 22:12:54
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】类比推理是研究物质性质的常用方法,可预测许多物质的性质,但类比是相对的,不能违背客观实际。下列说法中正确的是
A. 与水反应生成 与水反应生成 和 和 ,推测 ,推测 与水反应生成 与水反应生成 和 和 |
B. 与 与 反应生成 反应生成 ,则 ,则 与 与 反应生成 反应生成 |
C. 溶液与 溶液与 反应生成 反应生成 和 和 ,则 ,则 溶液与 溶液与 反应生成 反应生成 和 和 |
D.少量 通入 通入 溶液中产生白色沉淀,则少量 溶液中产生白色沉淀,则少量 通入 通入 溶液也产生白色沉淀 溶液也产生白色沉淀 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】类比推理是化学学习中的一种重要方法。下列类推结论中,正确的是
| 类比对象 | 结论 | |
| A | 2Na2O2+2CO2=== 2Na2CO3+O2 | 2Na2O2+2SO2===2 Na2SO3+O2 |
| B | Cl2+2Fe2+ ===2Fe3++2Cl- | I2+2Fe2+ ===2Fe3++2I- |
| C | Cl2+H2O===HCl+HClO | I2+H2O===HI+HIO |
| D | Ca(ClO)2+CO2+H2O==CaCO3↓+2HClO | Ca(ClO)2+SO2+H2O==CaSO3↓+2HClO |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】现有Fe、Al、Si三种单质的混合物,取一半投入足量的NaOH溶液中,将剩余的一半投入足量的稀硫酸中,若经测量两次实验产生的气体质量相等,则原混合物中Fe、Al、Si三种单质的物质的量之比可能为( )
| A.6:4:3 | B.1:1:1 | C.2:3:4 | D.3:7:6 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】对下列各种溶液中所含离子的判断合理的是
| A.向无色溶液中加氯水变橙色,溶液中可能含: SO42-、Br-、OH-、Ba2+ |
| B.25℃时在水电离出的c(H+)=1.0×10-11mol/L的溶液中可能含:Mg2+、Cu2+、SO42-、NO3- |
| C.某溶液,加铝粉有氢气放出,则溶液中可能含:K+、Na+、H+、NO3- |
| D.在c(Fe3+)=1.0 mol/L的溶液中可能含:K+、Na+、SCN-、HCO3- |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】若 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.标准状况下, 所含质子数为 所含质子数为 |
B.等物质的量的 和 和 含有的氧原子数均为 含有的氧原子数均为 |
C.常温下,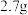 铝与足量的 铝与足量的 溶液反应,失去的电子数为 溶液反应,失去的电子数为 |
D.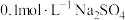 溶液中所含钠离子数为 溶液中所含钠离子数为 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】一些烷烃的燃烧热如下表:
下列表达正确的是
| 化合物 | 燃烧热/kJ·mol-1 | 化合物 | 燃烧热/kJ·mol-1 |
| 甲烷 | 890.3 | 正丁烷 | 2878.0 |
| 乙烷 | 1560.8 | 异丁烷 | 2869.6 |
| 丙烷 | 2221.5 | 2-甲基丁烷 | 3531.3 |
| A.乙烷燃烧的热化学方程式为:2C2H6(g)+7O2(g)=4CO2(g)+6H2O(g)ΔH=-1560.8kJ·mol-1 |
| B.稳定性:正丁烷>异丁烷 |
| C.正戊烷的燃烧热大于3531.3kJ·mol-1 |
| D.相同质量的烷烃,碳的质量分数越大,燃烧放出的热量越多 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】下列有关热化学方程式的叙述正确的是
| A.已知甲烷的燃烧热为890.3 kJ﹒mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)=2CO2(g)+2H2O(g) ΔH=-890.3kJ/mol |
| B.已知C(石墨,s)=C(金刚石,s)ΔH>0,则金刚石比石墨稳定 |
| C.已知中和热为ΔH=-57.4kJ/mol,则1mol稀硫酸和足量稀NaOH溶液反应的反应热就是中和热 |
| D.已知S(g)+O2(g)=SO2(g) ΔH1;S(s)+O2(g)=SO2(g) ΔH2,则ΔH1<ΔH2; |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】下列热化学方程式说法正确的是
| A.由C(s,石墨)═C(s,金刚石) ΔH>0可知,石墨比金刚石稳定 |
| B.CO的燃烧热是283.0kJ•mol-1,则2CO(g)+O2(g)═2CO2(g) ΔH= -283.0kJ•mol-1 |
| C.常温常压,强酸与强碱的稀溶液发生中和反应的中和热为57.3kJ•mol-1,则 HF(aq)+NaOH(aq)═NaF(aq)+H2O(l) ΔH= -57.3kJ•mol-1 |
| D.已知C(s)+O2(g)═CO2(g) ΔH1,C(s)+1/2O2(g)═CO(g) ΔH2, 则ΔH1>ΔH2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】室温下,下列探究方案能达到探究目的的是
| 序号 | 探究方案 | 探究目的 |
| ① | 用不同浓度、等体积的 溶液分别与相同浓度相同体积的 溶液分别与相同浓度相同体积的 溶液反应,观察现象 溶液反应,观察现象 | 探究浓度对反应速率的影响 |
| ② | 用pH计测定同浓度NaClO和NaF溶液的pH,比较溶液pH大小 | 比较HClO与HF的酸性强弱 |
| ③ | 向 和 和 混合溶液中滴加少量 混合溶液中滴加少量 溶液,观察沉淀颜色变化 溶液,观察沉淀颜色变化 | 比较CuS和ZnS的溶度积( )的大小 )的大小 |
| ④ | 向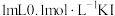 溶液中加入 溶液中加入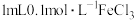 溶液,充分反应后,再加KSCN,观察溶液颜色变化 溶液,充分反应后,再加KSCN,观察溶液颜色变化 | 探究 是否完全反应 是否完全反应 |
| A.① | B.② | C.③ | D.④ |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列装置或操作能达到目的的是( )
 ① ① | 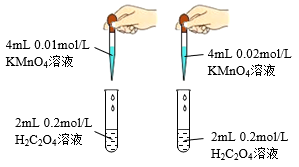 ② ② |
 ③ ③ | 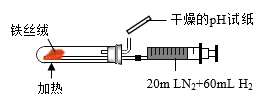 ④ ④ |
| A.装置①用滴定法测定盐酸的浓度 |
| B.装置②依据单位时间内颜色变化来比较浓度对反应速率的影响 |
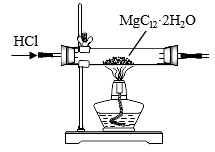
| C.装置③用于制取无水MgCl2 |
| D.装置④可用于合成氨并检验氨气的生成 |
您最近一年使用:0次

 溶于足量稀硝酸中:
溶于足量稀硝酸中:
 溶液与足量NaOH溶液混合:
溶液与足量NaOH溶液混合:
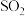 通入NaClO溶液中:
通入NaClO溶液中:
 溶液与0.3mol/L
溶液与0.3mol/L 溶液等体积混合:
溶液等体积混合:



