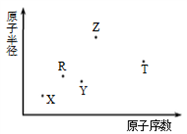
短周期主族元素X、Y、Z、R、T的原子半径与原子序数关系如图所示。其中X是原子半径最小的元素,R原子最外层电子数是电子层数的2倍,Y与Z能形成Z2Y、Z2Y2型离子化合物, T与Y 是同一主族元素。
(1)RX4的空间构型_____________ ,R在元素周期表中的位置_______________ 。
(2)比较X2Y、X2T稳定性强弱_________________ (填化学式)
(3)判断RY2是________ 化合物(填“离子”或“共价”)写出RY2电子式____________ ,
(4)写出一个能判断R、T非金属性强弱的化学方程式________________________________ 。
(5)写出氯碱工业上制取Z、Y、X的离子方程式_________________________________________ 。

(1)RX4的空间构型
(2)比较X2Y、X2T稳定性强弱
(3)判断RY2是
(4)写出一个能判断R、T非金属性强弱的化学方程式
(5)写出氯碱工业上制取Z、Y、X的离子方程式
更新时间:2017-06-13 21:37:36
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】A、B、C、D、E、F为短周期原子序数依次增大的主族元素,B最外层电子数是内层电子数的3倍,C在短周期元素中原子半径最大,E的最高正价与最低负价代数和为4,A、B常温下能形成两种液态化合物A2B和A2B2,D元素的单质常用来制造太阳能电池。请用化学用语回答下列问题:
(1)D元素在周期表中的位置为_____ ;B、D两种元素的最简单氢化物中,稳定性较强的氢化物的结构式是_____ ,D、E两种元素的最高价氧化物对应的水化物中,酸性较弱的是_____ (填化学式)。
(2)用电子式表示C2E的形成过程____ 。
(3)B、C、E形成的简单离子半径从大到小的顺序为_____ (用离子符号表示)。
(4)写出D的最高价氧化物与C的最高价氧化物对应水化物反应的离子方程式:_____ 。
(5)等物质的量的EB2与F的单质通入品红溶液将失去漂白性,反应的离子方程式为:_____ 。
(6)非金属性强弱大小关系E____ F(填写“大于”或“小于”),下列表述中不能证明这一事实的是_____ (填字母)。
a.E的氢化物比F的氢化物水溶液酸性弱
b.F的氧化物对应的水化物的酸性强于E的氧化物对应的水化物的酸性
c.F的单质能将E的单质从其钠盐溶液中置换出来
d.F的简单阴离子的还原性比E的简单阴离子的还原性弱
e.铁与F的单质反应生成+3价铁,而与E的单质反应生成+2铁
(1)D元素在周期表中的位置为
(2)用电子式表示C2E的形成过程
(3)B、C、E形成的简单离子半径从大到小的顺序为
(4)写出D的最高价氧化物与C的最高价氧化物对应水化物反应的离子方程式:
(5)等物质的量的EB2与F的单质通入品红溶液将失去漂白性,反应的离子方程式为:
(6)非金属性强弱大小关系E
a.E的氢化物比F的氢化物水溶液酸性弱
b.F的氧化物对应的水化物的酸性强于E的氧化物对应的水化物的酸性
c.F的单质能将E的单质从其钠盐溶液中置换出来
d.F的简单阴离子的还原性比E的简单阴离子的还原性弱
e.铁与F的单质反应生成+3价铁,而与E的单质反应生成+2铁
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】X、Y、Z、W是原子序数由小到大顺序排列的四种短周期元素,其中X、Z、W可分别与氢元素组成共价化合物 、
、 和
和 ;Y与氧元素可组成离子化合物
;Y与氧元素可组成离子化合物 和
和 。
。
(1)写出 的电子式:
的电子式:_______ ,其中含有的化学键类型是__________ 。
(2)Z元素在元素周期表中的位置是第________ 周期第_______ 族。X和Z形成的一种二元化合物会导致温室效应,其相对分子质量在170~190之间,且Z的质量分数约为70%,该化合物的化学式为____ 。
(3) 、
、 和
和 三种化合物,其中一种与另外两种都能反应,该化合物是
三种化合物,其中一种与另外两种都能反应,该化合物是______ (填化学式)。
(4)由X、W组成的化合物分子中,X、W原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出该反应的化学方程式:_______________ 。
 、
、 和
和 ;Y与氧元素可组成离子化合物
;Y与氧元素可组成离子化合物 和
和 。
。(1)写出
 的电子式:
的电子式:(2)Z元素在元素周期表中的位置是第
(3)
 、
、 和
和 三种化合物,其中一种与另外两种都能反应,该化合物是
三种化合物,其中一种与另外两种都能反应,该化合物是(4)由X、W组成的化合物分子中,X、W原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出该反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】元素周期表揭示了化学元素间的内在联系,部分元素在周期表中的位置如图所示:
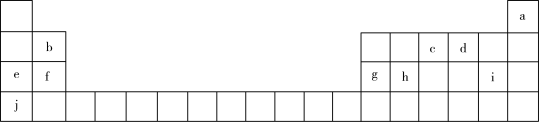
(1)元素h的原子结构示意图为_______ 。
(2)元素e的单质着火时,应该用_______ 来灭火。该单质需密封保存,其中一个目的是与水隔离,原因是_______ (用离子反应方程式表示)。
(3)元素g的氢氧化物化学式为_______ ,其用于中和胃酸的原理是_______ (用离子反应方程式表示)。
(4)写出元素f与元素i形成的化合物的电子式_______ 。
(5)元素b、e、f的最高价氧化物对应的水化物碱性由强到弱的顺序是_______ (用化学式表示)。
(6)实验室检验元素i的简单离子的操作和现象是_______ 。

(1)元素h的原子结构示意图为
(2)元素e的单质着火时,应该用
(3)元素g的氢氧化物化学式为
(4)写出元素f与元素i形成的化合物的电子式
(5)元素b、e、f的最高价氧化物对应的水化物碱性由强到弱的顺序是
(6)实验室检验元素i的简单离子的操作和现象是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】有四种短周期元素,它们的结构、性质等信息如表所述:
(1)基态A原子的核外电子排布式为_______
(2)A、B、C离子半径由大到小的顺序为:_______ ( 填元素符号)
(3)基态C原子的核外电子排布图是_______ ,其原子核外有_______ 个未成对电子,能量最高的电子为_______ 轨道 上的电子,其轨道呈_______ 形。
(4)D所在周期第一电离能最大的元素名为_______ ,该周期电负性最大的元素符号为_______ 。
(5)用电子式表示AD化合物的形成过程_______ 。
(6)CD3分子中含有的σ 键类型为_______ σ键。 (填s-s;s-p: p-p)
| 元素 | 结构、性质等信息 |
| A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
| B | B与A周同期,其最高价氧化物的水化物呈两性 |
| C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
(1)基态A原子的核外电子排布式为
(2)A、B、C离子半径由大到小的顺序为:
(3)基态C原子的核外电子排布图是
(4)D所在周期第一电离能最大的元素名为
(5)用电子式表示AD化合物的形成过程
(6)CD3分子中含有的σ 键类型为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】如表是元素周期表的一部分,请用规范的化学用语回答有关问题:
(1)元素⑨在周期表中所处位置______ 。
(2)表中化学性质最不活泼的元素,其原子结构示意图为______ 。
(3)④⑦⑨元素形成的化合物中含有的化学键类型为______ 。
(4)④、⑧、⑨三种元素的常见离子的半径由小到大的顺序为______ 。
(5)①、⑥、⑦三种元素的最高价氧化物的水化物中碱性最强的是______ 。
(6)写出⑥、⑧元素的最高价氧化物的水化物发生反应的离子方程式_______ 。
(7)②、③、④的简单氢化物中最稳定的是______ 。
(8)用电子式表示⑥与⑨形成的化合物的形成过程______ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ③ | ④ | ⑤ | |||
| 三 | ⑥ | ⑦ | ⑧ | ⑨ |
(2)表中化学性质最不活泼的元素,其原子结构示意图为
(3)④⑦⑨元素形成的化合物中含有的化学键类型为
(4)④、⑧、⑨三种元素的常见离子的半径由小到大的顺序为
(5)①、⑥、⑦三种元素的最高价氧化物的水化物中碱性最强的是
(6)写出⑥、⑧元素的最高价氧化物的水化物发生反应的离子方程式
(7)②、③、④的简单氢化物中最稳定的是
(8)用电子式表示⑥与⑨形成的化合物的形成过程
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】现有A、B、C、D、E、F、G七种短周期主族元素,其原子序数依次增大。已知A、D位于同一主族,D是短周期中原子半径最大的元素。B、E最外层电子数是最内层电子数的2倍。C、F的最外层电子数相等,且C、F的原子序数之和为A、D原子序数之和的两倍。
(1)A、C、D、F形成的简单离子半径由大到小的顺序是___________ (用元素符号填写);
(2)B、E、F、G的最高价氧化物对应的水化物酸性最强的是___________ (用化学式填写);
(3)由C、D两元素能形成一种原子个数比为1:1的化合物,该化合物所含的化学键类型有___________ ;
(4)下列事实能说明G元素的非金属性比F元素的非金属性强的是___________ (填字母序号)。
a.G单质与Na2S溶液反应溶液变浑浊
b.F氢化物的酸性比G的氢化物酸性弱
c.G和F两元素的简单氢化物受热分解,前者的分解温度高
(1)A、C、D、F形成的简单离子半径由大到小的顺序是
(2)B、E、F、G的最高价氧化物对应的水化物酸性最强的是
(3)由C、D两元素能形成一种原子个数比为1:1的化合物,该化合物所含的化学键类型有
(4)下列事实能说明G元素的非金属性比F元素的非金属性强的是
a.G单质与Na2S溶液反应溶液变浑浊
b.F氢化物的酸性比G的氢化物酸性弱
c.G和F两元素的简单氢化物受热分解,前者的分解温度高
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】X、Y、Z、W、R是短周期元素,原子序数依次增大。非金属X原子核外各层电子数之比为1:2,Y原子和Z原子的核外电子数之和为20,W和R是同周期相邻元素,Y的氧化物和R的氧化物均能形成酸雨。请回答下列问题:
(1)元素X的最高价氧化物的电子式为_______ ;元素Z的离子结构示意图为_______ 。
(2)用电子式表示元素R氢化物的形成过程:_______ ;
(3)单质铜和元素Y的最高价氧化物对应水化物的稀溶液发生反应的化学方程式为_______ 。
(4)元素W位于周期表的位置:_______ ,其非金属性比R弱,用原子结构的知识解释原因:_______ 。
(5)R的一种氧化物能使品红溶液褪色,工业上用Y的气态氢化物的水溶液作该氧化物的吸收剂,写出吸收剂与过量该氧化物反应的离子方程式:_______ 。
(1)元素X的最高价氧化物的电子式为
(2)用电子式表示元素R氢化物的形成过程:
(3)单质铜和元素Y的最高价氧化物对应水化物的稀溶液发生反应的化学方程式为
(4)元素W位于周期表的位置:
(5)R的一种氧化物能使品红溶液褪色,工业上用Y的气态氢化物的水溶液作该氧化物的吸收剂,写出吸收剂与过量该氧化物反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下图是短周期元素 在元素周期表中的位置。
在元素周期表中的位置。 在周期表中的位置是第
在周期表中的位置是第___________ 周期第___________ 族。
(2)b、c、e三种元素原子半径由大到小的顺序是___________ (填元素符号)。
(3)非金属性:e___________ f(填“ ”或“
”或“ ”),从原子结构角度解释其原因是
”),从原子结构角度解释其原因是___________ 。
(4)b、f两种元素形成的化合物有重要的用途,高温灼烧该化合物时,火焰呈___________ 色;用电子式表示a、f形成化合物的过程___________ 。
 在元素周期表中的位置。
在元素周期表中的位置。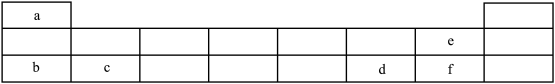
 在周期表中的位置是第
在周期表中的位置是第(2)b、c、e三种元素原子半径由大到小的顺序是
(3)非金属性:e
 ”或“
”或“ ”),从原子结构角度解释其原因是
”),从原子结构角度解释其原因是(4)b、f两种元素形成的化合物有重要的用途,高温灼烧该化合物时,火焰呈
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】现有部分短周期元素的性质或原子结构如表:
回答下列问题:
(1)X的离子结构示意图为__ 。
(2)Z的简单气态氢化物的VSEPR模型为___ ,分子中的中心原子的杂化轨道类型为___ ,分子的空间结构为__ 。
(3)1个Z的单质分子中,含有__ 个σ键和__ 个π键。
(4)Y的最高价氧化物对应的水化物与KOH反应的化学方程式为__ 。
(5)元素T与氯元素相比,非金属性较强的是__ (填元素符号),下列表述中能证明这事实的是__ (填标号)。
a.常温下氯气的颜色比T单质的颜色深
b.T的单质通入氯化钠水溶液中不能置换出氯气
c.氯与T形成的化合物中,氯元素呈正价
| 元素 | 元素性质或原子结构 |
| T | 2p轨道上有5个电子 |
| X | L层p能级电子数比s能级电子数多2个 |
| Y | 第三周期元素的简单离子中半径最小 |
| Z | L层有3个未成对电子 |
回答下列问题:
(1)X的离子结构示意图为
(2)Z的简单气态氢化物的VSEPR模型为
(3)1个Z的单质分子中,含有
(4)Y的最高价氧化物对应的水化物与KOH反应的化学方程式为
(5)元素T与氯元素相比,非金属性较强的是
a.常温下氯气的颜色比T单质的颜色深
b.T的单质通入氯化钠水溶液中不能置换出氯气
c.氯与T形成的化合物中,氯元素呈正价
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
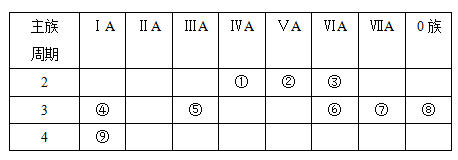
(1)在这些元素中,化学性质最不活泼的是______ (填元素符号,下同)。
(2)从①到③的元素中,非金属性最强的是_____ 。
(3)在最高价氧化物的水化物中,酸性最强的化合物的化学式是______ ,碱性最强的化合物的电子式是______ 。
(4)最高价氧化物是两性氧化物的元素是______ ;写出它的最高价氧化物与氢氧化钠反应的离子方程式______________________ 。
(5)用结构式表示元素①与③形成的一种可溶于水的化合物_____ ,该化合物的常见固体是______ 晶体。
(6)写出元素④的单质与水反应的化学方程式_________________ 。
(7)写出元素①的单质和元素⑥最高价氧化物对应水化物的浓溶液反应的化学方程式_______________________________ 。

(1)在这些元素中,化学性质最不活泼的是
(2)从①到③的元素中,非金属性最强的是
(3)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
(4)最高价氧化物是两性氧化物的元素是
(5)用结构式表示元素①与③形成的一种可溶于水的化合物
(6)写出元素④的单质与水反应的化学方程式
(7)写出元素①的单质和元素⑥最高价氧化物对应水化物的浓溶液反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】已知X、Y、Z、M、G、Q是六种短周期主族元素,原子序数依次增大。X、Z、Q的单质在常温下呈气态,Y的原子最外层电子数是其电子层数的2倍,X与M同主族,Z的气态氢化物能与其最高价氧化物的水化物反应,G是地壳中含量最高的金属元素。请回答下列问题:
(1)Q的元素符号为______ ,Y、Z、M、G四种元素原子半径由大到小的顺序是(写元素符号)_______ 。
(2)Y在元素周期表中的位置为_______________ ,Y与硫元素形成的二元化合物的电子式为_________________________ 。
(3)上述元素的最高价氧化物对应的水化物酸性最强的是(写化学式)_____________ 。
(4)单质Y和元素Z的最高价氧化物对应水化物的浓溶液发生反应的化学方程式为_________ 。
(5)Z和G组成的化合物GZ,被大量用于制造电子元件。工业上用G的氧化物、Y单质和Z单质在高温下制备GZ,其中G的氧化物和Y单质的物质的量之比为1∶3,则该反应的化学方程式为__________________________ 。
(1)Q的元素符号为
(2)Y在元素周期表中的位置为
(3)上述元素的最高价氧化物对应的水化物酸性最强的是(写化学式)
(4)单质Y和元素Z的最高价氧化物对应水化物的浓溶液发生反应的化学方程式为
(5)Z和G组成的化合物GZ,被大量用于制造电子元件。工业上用G的氧化物、Y单质和Z单质在高温下制备GZ,其中G的氧化物和Y单质的物质的量之比为1∶3,则该反应的化学方程式为
您最近一年使用:0次



