下列实验操作不正确的是
| 实验目的 | 实验操作 | |
| A | 验证化学反应中的能量变化 | 将NO2球浸泡在冰水,热水中观察颜色变化 |
| B | 证明非金属性:Cl>C>Si | 将纯碱与足量浓盐酸反应后产生的气体直接通入硅酸钠溶液中 |
| C | 探究相同条件下,溶液浓度对反应速率的影响 | 在两支试管中各加入4 mL 0.01 mol/L的KMnO4酸性溶液,再分别加入0.1 mol/L H2C2O4溶液2 mL、0.2 mol/L H2C2O4 溶液2 mL,分别记录溶液褪色所需时间 |
| D | 除去氢氧化铁中少量的氢氧化铜 | 将过量氨水加入混合物中并充分搅拌,然后过滤、洗涤、干燥 |
| A.A | B.B | C.C | D.D |
更新时间:2017-07-05 19:44:33
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列反应条件的控制中,不恰当的是( )
| A.为防止铁生锈,在其表面涂一层防锈油漆 |
| B.为防止火灾,在面粉厂、加油站等场所要严禁烟火 |
| C.为加快氯酸钾的分解速率,加入二氧化锰 |
| D.为加快过氧化氢的分解速率,把反应容器放到冷水中 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定条件下,反应H2(g)+Br2(g)=2HBr(g)的速率可用 =kcα(H2)cβ(Br2)cγ(HBr)表示,已知k为与温度有关的常数。该反应在不同浓度下的反应速率如表:
=kcα(H2)cβ(Br2)cγ(HBr)表示,已知k为与温度有关的常数。该反应在不同浓度下的反应速率如表:
下列说法错误的是
 =kcα(H2)cβ(Br2)cγ(HBr)表示,已知k为与温度有关的常数。该反应在不同浓度下的反应速率如表:
=kcα(H2)cβ(Br2)cγ(HBr)表示,已知k为与温度有关的常数。该反应在不同浓度下的反应速率如表:| c(H2)/(mol•L-1) | c(Br2)/(mol•L-1) | c(HBr)/(mol•L-1) | 反应速率 |
| 0.1 | 0.1 | 2 |  0 0 |
| 0.1 | 0.4 | 2 | 8 0 0 |
| 0.2 | 0.4 | 2 | 16 0 0 |
| 0.4 | 0.1 | 4 | 2 0 0 |
| A.α=1 | B.β= | C.γ=1 | D.温度升高时,k增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】某温度下,在一恒容密闭容器中进行如下两个反应并达到平衡:
①

②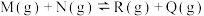

下列叙述错误的是
①


②
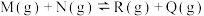

下列叙述错误的是
| A.加入适量Z,反应①和反应②的平衡均不移动 |
| B.通入稀有气体Ar,反应①的平衡正向移动 |
| C.降温时反应②的平衡逆向移动 |
| D.通入Y,则N的浓度增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列实验方案不能达到相应目的的是
| A | B | C | D | |
| 目的 | 比较 与 与 水解程度 水解程度 | 研究浓度对化学平衡的影响 | 证明 (aq)+H2O(l)⇌2 (aq)+H2O(l)⇌2 (aq)+2H+(aq)平衡的存在 (aq)+2H+(aq)平衡的存在 | 比较碳酸、醋酸和硼酸的酸性强弱 |
| 实验 方 案 | 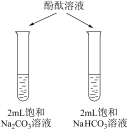 | 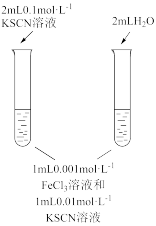 | 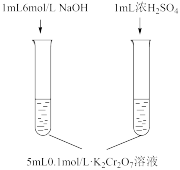 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】有A、B、C、D、E 5种元素,它们的核电荷数依次增大,且都小于20,其中C、E是金属元素;A和E属同一族,它们原子的最外层电子排布为ns1 ,B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半,下列说法不正确的是
A.D原子价层电子排布为3s23p4,轨道表示式为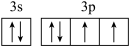 |
| B.E的最高价氧化物的水化物碱性比氢氧化钠强 |
| C.C的最高价氧化物的水化物是两性氢氧化物 |
| D.不存在由这五种元素组成的化合物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列结论不正确的是( )
①氢化物的稳定性:HF>HCl>SiH4 ②离子半径: Al3+>S2->Cl- ③离子的还原性:S2->Cl->Br- ④酸性:H2SO4>H3PO4>HClO ⑤沸点: H2S>H2O
①氢化物的稳定性:HF>HCl>SiH4 ②离子半径: Al3+>S2->Cl- ③离子的还原性:S2->Cl->Br- ④酸性:H2SO4>H3PO4>HClO ⑤沸点: H2S>H2O
| A.②③⑤ | B.①②③ | C.②④⑤ | D.①③⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】如表实验中,对应的现象以及结论都正确且两者具有因果关系的是
| 选项 | 实验 | 现象 | 结论 |
| A | 向装有石灰石的简易启普发生器中加入浓醋酸,将产生的气体通入苯酚钠溶液中 | 苯酚钠溶液产生浑浊 | 酸性:醋酸>碳酸>苯酚 |
| B | 将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡、静置 | 下层溶液显紫红色 | 氧化性:Fe3+>I2 |
| C | 向10 mL 0.2 mol·L-1NaOH溶液中滴入2滴0.1 mol·L-1MgCl2溶液,产生白色沉淀后,再滴加2滴0.1 mol·L-1FeCl3溶液 | 白色沉淀转化为红褐色沉淀 | 相同温度下的KspMg(OH)2>KspFe(OH)3 |
| D | 室温下,用pH试纸分别测定浓度为0.1 mol·L-1NaClO溶液和0.1 mol·L-1CH3COONa溶液的pH | CH3COONa溶液的pH试纸颜色深 | 酸性:HClO>CH3COOH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列对相关实验操作、现象的解释或结论都正确的是
选项 | 实验操作 | 现象 | 解释或结论 |
A | 向铁粉(过量)中加入稀硝酸,充分反应后,滴入KSCN溶液 | 溶液呈红色 | 稀硝酸将Fe氧化为Fe3+ |
B | 常温下,向黄色AgI沉淀中滴入足量浓KCl溶液 | 无明显现象 | AgI比AgCl更难溶 |
C | 将铝箔插入稀硝酸中 | 无现象 | 铝箔表面被HNO3氧化,形成致密的氧化膜 |
D | 将蘸有浓氨水的玻璃棒移近某试剂瓶口(瓶盖打开) | 瓶口出现白烟 | 试剂瓶中存放的是浓盐酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次


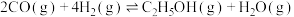 ,该反应的速率方程为
,该反应的速率方程为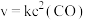 ,其中k为速率常数,下列说法中错误的是
,其中k为速率常数,下列说法中错误的是 的浓度越大
的浓度越大 可提高反应速率
可提高反应速率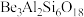 )被称为宝石之王,与其相似的天然绿色宝石有萤石[主要成分
)被称为宝石之王,与其相似的天然绿色宝石有萤石[主要成分 ]、磷灰石[主要成分
]、磷灰石[主要成分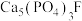 ]。下列说法正确的是
]。下列说法正确的是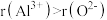
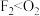


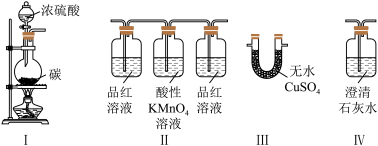
 溶液的作用是除去
溶液的作用是除去


