金属钙线是炼制优质钢材的脱氧脱磷剂,某钙线的主要成分为金属M和Ca,并含有3.5%(质量分数)CaO.
(1)Ca与最活跃的非金属元素A形成化合物D,D的电子式为___________________ ,D的沸点比A与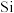 形成的化合物E的沸点
形成的化合物E的沸点_________ .(填“高”或“低”)
(2)配平用钙线氧脱鳞的化学方程式:__ P+ __FeO+__CaO __Ca3(PO4)2+__Fe
__Ca3(PO4)2+__Fe
(3)将钙线试样溶于稀盐酸后,加入过量 溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色
溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色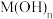 .则金属M为
.则金属M为________ (填元素符号);检测溶液中含有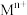 的方法是
的方法是_______________________________________________ .
(4)取1.6g钙线试样,与水充分反映,生成224mL (标准状况),在此溶液中通入适量的
(标准状况),在此溶液中通入适量的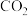 ,最多能得到
,最多能得到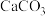
___________________ g.
(1)Ca与最活跃的非金属元素A形成化合物D,D的电子式为
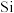 形成的化合物E的沸点
形成的化合物E的沸点(2)配平用钙线氧脱鳞的化学方程式:
 __Ca3(PO4)2+__Fe
__Ca3(PO4)2+__Fe(3)将钙线试样溶于稀盐酸后,加入过量
 溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色
溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色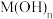 .则金属M为
.则金属M为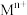 的方法是
的方法是(4)取1.6g钙线试样,与水充分反映,生成224mL
 (标准状况),在此溶液中通入适量的
(标准状况),在此溶液中通入适量的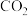 ,最多能得到
,最多能得到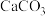
更新时间:2017-09-15 20:35:43
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】已知 与碱溶液发生反应时,依次发生如下离子反应:
与碱溶液发生反应时,依次发生如下离子反应:
与氢氧化钠:

与氢氧化钙:

(1)向含0.01mol氢氧化钙的石灰水中通入 ,得到0.4g白色沉淀,则
,得到0.4g白色沉淀,则 的体积(折合标况)为
的体积(折合标况)为___________ L或___________ L。
(2)现有NaOH和 混合溶液100mL,已知该溶液中
混合溶液100mL,已知该溶液中 mol/L,向溶液中缓缓通入
mol/L,向溶液中缓缓通入 气体(溶液体积变化忽略不计);当通入
气体(溶液体积变化忽略不计);当通入 气体体积为0.56L(标准状况)时生成的沉淀最多,则原浴液中氢氧化钠和氢氧化钙的物质的量浓度各为多少
气体体积为0.56L(标准状况)时生成的沉淀最多,则原浴液中氢氧化钠和氢氧化钙的物质的量浓度各为多少_______ ?
 与碱溶液发生反应时,依次发生如下离子反应:
与碱溶液发生反应时,依次发生如下离子反应:与氢氧化钠:


与氢氧化钙:


(1)向含0.01mol氢氧化钙的石灰水中通入
 ,得到0.4g白色沉淀,则
,得到0.4g白色沉淀,则 的体积(折合标况)为
的体积(折合标况)为(2)现有NaOH和
 混合溶液100mL,已知该溶液中
混合溶液100mL,已知该溶液中 mol/L,向溶液中缓缓通入
mol/L,向溶液中缓缓通入 气体(溶液体积变化忽略不计);当通入
气体(溶液体积变化忽略不计);当通入 气体体积为0.56L(标准状况)时生成的沉淀最多,则原浴液中氢氧化钠和氢氧化钙的物质的量浓度各为多少
气体体积为0.56L(标准状况)时生成的沉淀最多,则原浴液中氢氧化钠和氢氧化钙的物质的量浓度各为多少
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】已知铝是一种能够和强碱溶液反应生成氢气的一种特殊金属,其反应的化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,现向400mLNaOH溶液中投入10.8gAl,二者恰好完全反应,计算:
(1)Al的物质的量为______ mol。
(2)参加反应的NaOH的物质的量为______ mol;溶液的物质的量浓度_______ mol•L-1。
(3)生成的H2在标准状况下的体积为______ L;含有的电子数为______ 。
(1)Al的物质的量为
(2)参加反应的NaOH的物质的量为
(3)生成的H2在标准状况下的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】研究物质性质及物质转化具有重要的价值,根据所学知识回答下列问题:
(1)我国四大发明之一的火药是由硫磺粉、硝酸钾、木炭粉按一定比例混合而成的,爆炸时的反应为 ,在该反应的生成物中,属于非电解质的物质是
,在该反应的生成物中,属于非电解质的物质是___________ (填化学式,下同),属于电解质的物质是___________ ,还原产物是___________ ;当3.2gS参与反应时,生成的气体质量为___________ g。
(2) 是高效、绿色的水处理剂,其原理如图所示。
是高效、绿色的水处理剂,其原理如图所示。
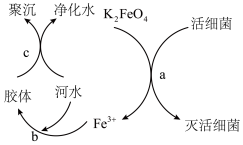
①从物质的类别来看,高铁酸钾( )属于
)属于___________ (“酸”“碱”“盐”或“氧化物”)。
②从元素的化合价角度来看, 中铁的化合价为
中铁的化合价为___________ 价,则过程a中 体现了
体现了___________ (填“氧化”或“还原”)性,活细菌发生了___________ (填“氧化”或“还原”)反应,该过程中消耗2个 时,转移的电子数目为
时,转移的电子数目为___________ 。
(3)纯碱和小苏打是日常家庭厨房中的常见用品,从物质的类别来看,均属于盐类。若取适量小苏打加水溶解,配制成溶液,再向其中加入少量澄清石灰水,发生反应的离子方程式是___________ 。
(1)我国四大发明之一的火药是由硫磺粉、硝酸钾、木炭粉按一定比例混合而成的,爆炸时的反应为
 ,在该反应的生成物中,属于非电解质的物质是
,在该反应的生成物中,属于非电解质的物质是(2)
 是高效、绿色的水处理剂,其原理如图所示。
是高效、绿色的水处理剂,其原理如图所示。
①从物质的类别来看,高铁酸钾(
 )属于
)属于②从元素的化合价角度来看,
 中铁的化合价为
中铁的化合价为 体现了
体现了 时,转移的电子数目为
时,转移的电子数目为(3)纯碱和小苏打是日常家庭厨房中的常见用品,从物质的类别来看,均属于盐类。若取适量小苏打加水溶解,配制成溶液,再向其中加入少量澄清石灰水,发生反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)现有以下物质:①NaCl晶体 ②液态SO3 ③液态的醋酸 ④汞 ⑤BaSO4固体 ⑥蔗糖(C12H22O11) ⑦酒精(C2H5OH) ⑧熔化K2SO4 请回答下列问题(用序号):
①以上物质中属于电解质的是____________ ;
②以上物质中属于非电解质的是___________ ;
(2)碘元素的一种核素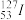 I可用于治疗肿瘤。该核素的质子数为
I可用于治疗肿瘤。该核素的质子数为_________ ,中子数为___________ ,质量数为______________ ,核外电子数为______________ 。
(3)在一定条件下,21.6gA单质与1.20molCl2完全反应,生成0.800molAClx,则X=____________ ,A的摩尔质量为_______________ 。
(4)有反应如下:Al2O3+N2+3C=2AlN+3CO
①标出该反应中电子转移的方向和数目______________ 。
②在该反应中,氧化剂是___________ ,还原剂是_________________ 。
①以上物质中属于电解质的是
②以上物质中属于非电解质的是
(2)碘元素的一种核素
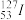 I可用于治疗肿瘤。该核素的质子数为
I可用于治疗肿瘤。该核素的质子数为(3)在一定条件下,21.6gA单质与1.20molCl2完全反应,生成0.800molAClx,则X=
(4)有反应如下:Al2O3+N2+3C=2AlN+3CO
①标出该反应中电子转移的方向和数目
②在该反应中,氧化剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】自舍勒发现氯气可以作为消毒剂以来,人们陆续发现和使用了形形色色的消毒剂。
(1)舍勒发现氯气的方法至今还是实验室制取氯气的主要方法之一。请写出实验室用 和浓盐酸制氯气的化学反应方程式,并用双线桥表示电子的转移
和浓盐酸制氯气的化学反应方程式,并用双线桥表示电子的转移_________ 。反应中盐酸表现出的性质有_________ 。
(2)根据世界环保联盟的要求,二氧化氯( )消毒剂将逐渐取代
)消毒剂将逐渐取代 成为水的消毒剂。工业上常用
成为水的消毒剂。工业上常用 和
和 溶液混合并加入稀
溶液混合并加入稀 酸化后制得
酸化后制得 ,反应的离子方程式为:
,反应的离子方程式为:_________ 。
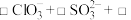 _________
_________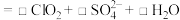
(3)高铁酸钾 是新型高效、多功能、绿色消毒剂。
是新型高效、多功能、绿色消毒剂。
①湿法制备高铁酸钾的反应体系中有六种微粒: 、
、 、
、 、
、 、
、 、
、 ,写出湿法制备高铁酸钾的离子方程式
,写出湿法制备高铁酸钾的离子方程式_________ 。
②如下图所示,用 氧化
氧化 也可以制备高铁酸钾,反应原理为:
也可以制备高铁酸钾,反应原理为: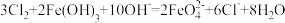 。
。

反应后取出三口瓶中的溶液于试管中,加入稀 后产生黄绿色气体
后产生黄绿色气体 ,同时检测到溶液中存在
,同时检测到溶液中存在 。制备高铁酸钾的实验中,氧化性:
。制备高铁酸钾的实验中,氧化性:
_________  (填写>,<或=)。试管中发生反应再次产生
(填写>,<或=)。试管中发生反应再次产生 的实验中,氧化性:
的实验中,氧化性:
_________  (填写>,<或=)。试说明影响
(填写>,<或=)。试说明影响 和
和 氧化性强弱的因素
氧化性强弱的因素_________ 。
(1)舍勒发现氯气的方法至今还是实验室制取氯气的主要方法之一。请写出实验室用
 和浓盐酸制氯气的化学反应方程式,并用双线桥表示电子的转移
和浓盐酸制氯气的化学反应方程式,并用双线桥表示电子的转移(2)根据世界环保联盟的要求,二氧化氯(
 )消毒剂将逐渐取代
)消毒剂将逐渐取代 成为水的消毒剂。工业上常用
成为水的消毒剂。工业上常用 和
和 溶液混合并加入稀
溶液混合并加入稀 酸化后制得
酸化后制得 ,反应的离子方程式为:
,反应的离子方程式为: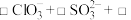 _________
_________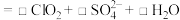
(3)高铁酸钾
 是新型高效、多功能、绿色消毒剂。
是新型高效、多功能、绿色消毒剂。①湿法制备高铁酸钾的反应体系中有六种微粒:
 、
、 、
、 、
、 、
、 、
、 ,写出湿法制备高铁酸钾的离子方程式
,写出湿法制备高铁酸钾的离子方程式②如下图所示,用
 氧化
氧化 也可以制备高铁酸钾,反应原理为:
也可以制备高铁酸钾,反应原理为: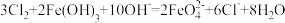 。
。
反应后取出三口瓶中的溶液于试管中,加入稀
 后产生黄绿色气体
后产生黄绿色气体 ,同时检测到溶液中存在
,同时检测到溶液中存在 。制备高铁酸钾的实验中,氧化性:
。制备高铁酸钾的实验中,氧化性:
 (填写>,<或=)。试管中发生反应再次产生
(填写>,<或=)。试管中发生反应再次产生 的实验中,氧化性:
的实验中,氧化性:
 (填写>,<或=)。试说明影响
(填写>,<或=)。试说明影响 和
和 氧化性强弱的因素
氧化性强弱的因素
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】钒具有众多优良的性能,用途十分广泛,有金属“维生素”之称。完成下列填空:
(1)将废钒催化剂(主要成分 V2O5)与稀硫酸、亚硫酸钾溶液混合,充分反应,所得溶液显酸性,溶液中含 VO2+、K+、SO42-等离子。写出该反应的化学方程式:____________ 。
(2)向上述所得溶液中加入 KClO3 溶液,充分反应后,溶液中新增加了 VO2+、Cl-。写出并配平该反应的离子方程式,并标出电子转移的数目和方向_____ 。
(3)已知V2O5 能和盐酸反应生成氯气和VO2+,请再写一个离子方程式:________ ,说明还原性:SO32->Cl->VO2+。
(1)将废钒催化剂(主要成分 V2O5)与稀硫酸、亚硫酸钾溶液混合,充分反应,所得溶液显酸性,溶液中含 VO2+、K+、SO42-等离子。写出该反应的化学方程式:
(2)向上述所得溶液中加入 KClO3 溶液,充分反应后,溶液中新增加了 VO2+、Cl-。写出并配平该反应的离子方程式,并标出电子转移的数目和方向
(3)已知V2O5 能和盐酸反应生成氯气和VO2+,请再写一个离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】完成下列填空
(1)某Fe2(SO4)3样品含有少量FeSO4杂质,将其配成溶液。
①若要检验溶液中的Fe3+,可加入___________ 试剂(填化学式),观察溶液呈血红色。
②若要检验溶液中的Fe2+,下列方法可行的是:___________ 。
A.取少量溶液于试管中,滴入几滴酸性高锰酸钾溶液,若紫红色褪去,则含有Fe2+
B.取少量溶液于试管中,加入新制氯水,再滴入硫氰化钾,若呈血红色,则含有Fe2+
C.取少量溶液于试管中,滴入NaOH溶液,看到白色沉淀迅速变为灰绿再变为红褐色,则含有Fe2+
(2)高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,某学习小组设计如图方案制备高铁酸钾:
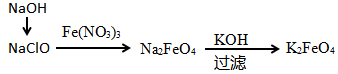
①高铁酸钾中铁元素的化合价为___________ ,据此推测它具有的化学性质是___________ 。
②其中第一步操作是:在NaClO溶液中加入烧碱固体形成强碱性环境,将研磨过的硝酸铁少量多次地加入上述溶液中,温度保持0℃反应1h,则采用的合适控温方式是___________ 。发生的离子反应为:___________ 。
③高铁酸钾和水发生反应,生成一种胶体能吸附杂质净水,同时还产生气体,写出反应的离子方程式:___________ 。
(1)某Fe2(SO4)3样品含有少量FeSO4杂质,将其配成溶液。
①若要检验溶液中的Fe3+,可加入
②若要检验溶液中的Fe2+,下列方法可行的是:
A.取少量溶液于试管中,滴入几滴酸性高锰酸钾溶液,若紫红色褪去,则含有Fe2+
B.取少量溶液于试管中,加入新制氯水,再滴入硫氰化钾,若呈血红色,则含有Fe2+
C.取少量溶液于试管中,滴入NaOH溶液,看到白色沉淀迅速变为灰绿再变为红褐色,则含有Fe2+
(2)高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,某学习小组设计如图方案制备高铁酸钾:
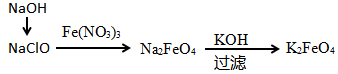
①高铁酸钾中铁元素的化合价为
②其中第一步操作是:在NaClO溶液中加入烧碱固体形成强碱性环境,将研磨过的硝酸铁少量多次地加入上述溶液中,温度保持0℃反应1h,则采用的合适控温方式是
③高铁酸钾和水发生反应,生成一种胶体能吸附杂质净水,同时还产生气体,写出反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】明矾[ KAl(SO4)2·12H2O ]在造纸、净水等方面应用广泛。以处理过的废旧易拉罐碎屑为原料(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如下图所示。

回答下列问题:
(1)原料溶解过程中反应的离子方程式是_________________________ 。
(2)Al(OH)3 与稀硫酸反应的离子方程式是__________________________ 。
(3)溶液A中通入过量CO2,反应的离子方程式是_________________ 。
(4)为证明固体B中含有铁,某同学做如下实验:取少量固体B,加入稀硫酸使其溶解,观察到有无色气体生成。向溶液中加入___________ ,溶液立即变红,证明固体B中含有铁。

回答下列问题:
(1)原料溶解过程中反应的离子方程式是
(2)Al(OH)3 与稀硫酸反应的离子方程式是
(3)溶液A中通入过量CO2,反应的离子方程式是
(4)为证明固体B中含有铁,某同学做如下实验:取少量固体B,加入稀硫酸使其溶解,观察到有无色气体生成。向溶液中加入
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol/L的溶液.在FeCl2溶液中需加入少量铁屑,其目的是________ 。
(2)甲组同学取2mL FeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为_______ 。
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mLFeCl2溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和l滴KSCN溶液,溶液变红,煤油的作用是______ 。
(4)丙组同学取10 mL0.1mol/LKI溶液,加入6mL0.1mol/LFeCl3溶液混合。分别取2mL此溶液于3 支试管中进行如下实验:
①第一支试管中加入1mLCCl4充分振荡、静置,CCl4层呈紫色;
②第二支试管中加入1滴K3[Fe(CN)6] 溶液,生成蓝色沉淀:
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是_____ (填离子符号);实验①和③说明:在I- 过量的情况下,溶液中仍含有______ (填离子符号),由此可以证明该氧化还原反应为______ 。
(5)丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为________ ;
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol/L的溶液.在FeCl2溶液中需加入少量铁屑,其目的是
(2)甲组同学取2mL FeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mLFeCl2溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和l滴KSCN溶液,溶液变红,煤油的作用是
(4)丙组同学取10 mL0.1mol/LKI溶液,加入6mL0.1mol/LFeCl3溶液混合。分别取2mL此溶液于3 支试管中进行如下实验:
①第一支试管中加入1mLCCl4充分振荡、静置,CCl4层呈紫色;
②第二支试管中加入1滴K3[Fe(CN)6] 溶液,生成蓝色沉淀:
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是
(5)丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)下列变化:①I2升华;②烧碱熔化;③NaCl溶于水;④HCl溶于水;⑤O2溶于水;⑥NH4HCO3受热分解。其中仅发生共价键破坏的是_____ (填序号,下同);仅发生离子键破坏的是_____ 。
(2)在下列物质中:①HCl、②N2、③NH3、④Na2O2、⑤H2O2、⑥NH4Cl、⑦NaOH、⑧Ar、⑨CO2、⑩C2H4(用物质前序号填空),其中只存在非极性键的分子是_____ ;既存在离子键又存在极性键的是_____ 。
(3)写出下列物质的电子式。
①Na2O2_____ 。
②HClO_____ 。
③NH4Cl_____ 。
(1)下列变化:①I2升华;②烧碱熔化;③NaCl溶于水;④HCl溶于水;⑤O2溶于水;⑥NH4HCO3受热分解。其中仅发生共价键破坏的是
(2)在下列物质中:①HCl、②N2、③NH3、④Na2O2、⑤H2O2、⑥NH4Cl、⑦NaOH、⑧Ar、⑨CO2、⑩C2H4(用物质前序号填空),其中只存在非极性键的分子是
(3)写出下列物质的电子式。
①Na2O2
②HClO
③NH4Cl
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下面是元素周期表的草图,表中所列字母代号分别代表某一种元素,请回答:
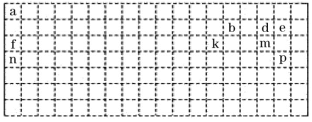
(1)表中的实线表示元素周期表的左右边界,请用实线补全元素周期表的上下边界。_______
(2)表中最活泼的金属与最活泼的非金属形成的物质是_______ (填化学式)。
(3)由a、d两种元素可形成两种化合物,写出其中一种化合物分解生成另一种化合物的化学方程式:____ ,这两种化合物中所含的化学键有____ (填字母)。
A.极性共价键 B.非极性共价键 C.离子键
(4)e、f、k、m对应的单原子离子的半径由大到小的顺序为___ (填离子符号)。
(5)e、p对应的离子还原性由强到弱顺序为_____ (填离子符号)。
(6)d、e、m的气态氢化物中,最不稳定的是_______ (填化学式)。
(7)用电子式表示n与m形成的原子个数比2∶1的化合物的形成过程:________ 。

(1)表中的实线表示元素周期表的左右边界,请用实线补全元素周期表的上下边界。
(2)表中最活泼的金属与最活泼的非金属形成的物质是
(3)由a、d两种元素可形成两种化合物,写出其中一种化合物分解生成另一种化合物的化学方程式:
A.极性共价键 B.非极性共价键 C.离子键
(4)e、f、k、m对应的单原子离子的半径由大到小的顺序为
(5)e、p对应的离子还原性由强到弱顺序为
(6)d、e、m的气态氢化物中,最不稳定的是
(7)用电子式表示n与m形成的原子个数比2∶1的化合物的形成过程:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】按要求回答下列问题:
(1)在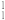 H、
H、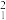 H、
H、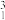 H、
H、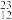 Mg、
Mg、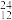 Mg和
Mg和 Cu中共有
Cu中共有______ 种元素,______ 种原子
(2)下列各组微粒:①16O2和18O2 ②H2和D2 ③1735Cl和1737Cl ④1H218O和2H216O属于同位素的是___________________
(3)下列物质中:H2O2、KCl、Na2SO4、Na2O2、HCl、O2; 其中只含离子键的是________ ,只含极性键的是______ ,既含离子键又含极性键的是_____ ,既含离子键又含非极性键的是_______
(4)写出下列物质的电子式:Na2O2 :______________ H2O2 :________________
(5)用电子式表示下列化合物的形成过程
H2S:__________________________________
KCl:_________________
(1)在
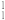 H、
H、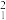 H、
H、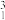 H、
H、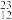 Mg、
Mg、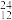 Mg和
Mg和 Cu中共有
Cu中共有(2)下列各组微粒:①16O2和18O2 ②H2和D2 ③1735Cl和1737Cl ④1H218O和2H216O属于同位素的是
(3)下列物质中:H2O2、KCl、Na2SO4、Na2O2、HCl、O2; 其中只含离子键的是
(4)写出下列物质的电子式:Na2O2 :
(5)用电子式表示下列化合物的形成过程
H2S:
KCl:
您最近一年使用:0次



