向某密闭容器中加入0.6 mol A、0.2 mol C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如图甲所示(其中t0~t1阶段c(B)未画出)。t2时刻后改变条件反应体系中反应速率随时间变化的情况如图乙所示,且四个阶段都只改变一种条件并且改变的条件均不相同。下列说法正确的是
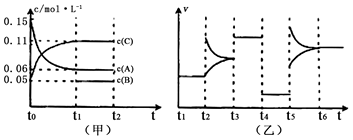

A.反应的方程式为3A(g)+B(g) 2C(g) 2C(g) |
| B.t3~t4,t4~t5,t5~t6各阶段改变的条件依次为:加催化剂,降低反应温度,增大压强 |
| C.B的起始物质的量为0.08 mol |
| D.t0~t1阶段A的转化率为40% |
更新时间:2017-10-19 08:27:59
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】一定条件下,0.2 mol X(g)与0.2 mol Y(g)在容积固定的密闭容器中发生反应:X(g)+2Y(g) Z(g) △H= -akJ· mol-1,下列说法正确的是
Z(g) △H= -akJ· mol-1,下列说法正确的是
 Z(g) △H= -akJ· mol-1,下列说法正确的是
Z(g) △H= -akJ· mol-1,下列说法正确的是| A.反应一段时间后,X与Y的物质的量之比仍为1:1 |
| B.达到平衡时,反应放出0. la kJ的热量 |
| C.达到平衡后,若向平衡体系中充入稀有气体,Z的正反应速率不变 |
| D.X的体积分数保持不变,说明反应已达到平衡 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】恒温恒容条件下,向密闭容器中加入一定量X,发生反应的方程式为①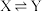 ;②
;②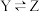 。反应的速率
。反应的速率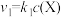 ,反应②的速率
,反应②的速率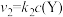 ,式中
,式中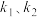 为速率常数。图甲为该体系中X、Y、Z浓度随时间变化的曲线,图乙为反应①和②的
为速率常数。图甲为该体系中X、Y、Z浓度随时间变化的曲线,图乙为反应①和②的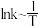 曲线。下列说法错误的是
曲线。下列说法错误的是
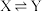 ;②
;②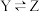 。反应的速率
。反应的速率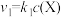 ,反应②的速率
,反应②的速率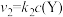 ,式中
,式中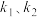 为速率常数。图甲为该体系中X、Y、Z浓度随时间变化的曲线,图乙为反应①和②的
为速率常数。图甲为该体系中X、Y、Z浓度随时间变化的曲线,图乙为反应①和②的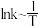 曲线。下列说法错误的是
曲线。下列说法错误的是
A.温度低于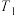 时,总反应速率由反应②决定 时,总反应速率由反应②决定 |
B.随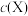 的减小,反应②的速率先增大后减小 的减小,反应②的速率先增大后减小 |
C.体系存在的速率关系: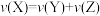 |
| D.欲提高Y产率,需提高反应温度且控制反应时间 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】已知合成氨反应: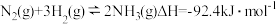 ,反应速率方程为
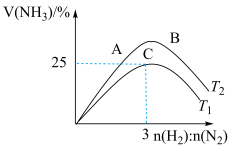
,反应速率方程为 (k为常数,随温度的升高而增大)。下图表示在恒压密闭容器中,不同温度下,达到平衡时
(k为常数,随温度的升高而增大)。下图表示在恒压密闭容器中,不同温度下,达到平衡时 的体积百分数与投料比
的体积百分数与投料比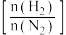 的关系。有关说法错误的是
的关系。有关说法错误的是
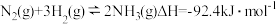 ,反应速率方程为
,反应速率方程为 (k为常数,随温度的升高而增大)。下图表示在恒压密闭容器中,不同温度下,达到平衡时
(k为常数,随温度的升高而增大)。下图表示在恒压密闭容器中,不同温度下,达到平衡时 的体积百分数与投料比
的体积百分数与投料比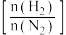 的关系。有关说法错误的是
的关系。有关说法错误的是
| A.该反应低温可自发 |
B.其他条件不变,减小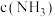 可使合成氨速率加快 可使合成氨速率加快 |
C.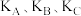 的大小关系为 的大小关系为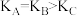 |
D.C点时 的平衡转化率为 的平衡转化率为 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】在 个容积均为
个容积均为 的恒容密闭容器中发生反应:
的恒容密闭容器中发生反应: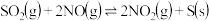 。改变容器Ⅰ的反应温度,平衡时
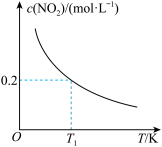
。改变容器Ⅰ的反应温度,平衡时 与温度的关系如图所示。下列说法正确的是
与温度的关系如图所示。下列说法正确的是
 个容积均为
个容积均为 的恒容密闭容器中发生反应:
的恒容密闭容器中发生反应: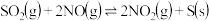 。改变容器Ⅰ的反应温度,平衡时
。改变容器Ⅰ的反应温度,平衡时 与温度的关系如图所示。下列说法正确的是
与温度的关系如图所示。下列说法正确的是
| 容器编号 | 温度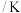 | 起始物质的量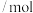 | |||
 |  |  |  | ||
| Ⅰ | 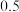 | 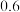 |  |  | |
| Ⅱ |  | 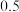 |  | 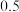 |  |
| Ⅲ |  | 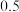 |  |  |  |
A.该反应的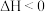 |
B. 时,该反应的平衡常数为 时,该反应的平衡常数为 |
C.容器Ⅰ与容器Ⅱ均在 时达到平衡,总压强之比小于 时达到平衡,总压强之比小于 |
D.若 ,达到平衡时,容器Ⅲ中 ,达到平衡时,容器Ⅲ中 的体积分数大于 的体积分数大于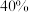 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】氢能是一种绿色能源。以乙醇和水催化重整可获得到 。有关反应如下:
。有关反应如下:
反应①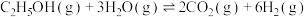
 ,平衡常数
,平衡常数 ;
;
反应②
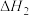 ,平衡常数
,平衡常数 ;
;
反应③
 ,平衡常数
,平衡常数 。
。
已知:平衡常数与 关系为
关系为 (R为常能数,K为平衡常数,T为温度)。
(R为常能数,K为平衡常数,T为温度)。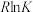 与T关系如图所示。下列推断正确的是
与T关系如图所示。下列推断正确的是

 。有关反应如下:
。有关反应如下:反应①
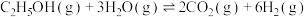
 ,平衡常数
,平衡常数 ;
;反应②

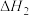 ,平衡常数
,平衡常数 ;
;反应③

 ,平衡常数
,平衡常数 。
。已知:平衡常数与
 关系为
关系为 (R为常能数,K为平衡常数,T为温度)。
(R为常能数,K为平衡常数,T为温度)。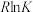 与T关系如图所示。下列推断正确的是
与T关系如图所示。下列推断正确的是
A. , , | B.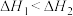 |
C.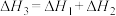 | D.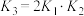 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】二氧化碳的化工利用是降低大气中二氧化碳浓度的有效途径,二氧化碳加氢制甲烷是该领域的最佳选择。反应体系中,主要发生反应的热化学方程式如下:
反应Ⅰ:CO2(g)+4H2(g) CH4(g)+2H2O(g)△H=-164.7kJ•mol-1
CH4(g)+2H2O(g)△H=-164.7kJ•mol-1
反应Ⅱ:CO2(g)+H2(g) CO(g)+H2O(g)△H=+41.2kJ•mol-1
CO(g)+H2O(g)△H=+41.2kJ•mol-1
反应Ⅲ:2CO(g) +2H2(g) CO2(g)+CH4(g)△H=-247.1kJ•mol-1
CO2(g)+CH4(g)△H=-247.1kJ•mol-1
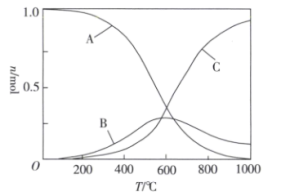
向恒压密闭容器中通入1molCO2和4molH2,不同温度下,使反应均进行tmin,测得CH4、CO、CO2的物质的量随温度的变化如图所示。下列说法中不正确的是
反应Ⅰ:CO2(g)+4H2(g)
 CH4(g)+2H2O(g)△H=-164.7kJ•mol-1
CH4(g)+2H2O(g)△H=-164.7kJ•mol-1反应Ⅱ:CO2(g)+H2(g)
 CO(g)+H2O(g)△H=+41.2kJ•mol-1
CO(g)+H2O(g)△H=+41.2kJ•mol-1反应Ⅲ:2CO(g) +2H2(g)
 CO2(g)+CH4(g)△H=-247.1kJ•mol-1
CO2(g)+CH4(g)△H=-247.1kJ•mol-1向恒压密闭容器中通入1molCO2和4molH2,不同温度下,使反应均进行tmin,测得CH4、CO、CO2的物质的量随温度的变化如图所示。下列说法中不正确的是

A.反应Ⅰ的平衡常数可表示为K=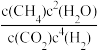 |
| B.图中曲线B表示CH4的物质的量随温度的变化 |
| C.为提高CO2转化为CH4的转化率,需要研发在低温区高效的催化剂 |
D.CH4(g)+H2O(g) CO(g)+3H2(g)在任何温度下均能自发 CO(g)+3H2(g)在任何温度下均能自发 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下[已知N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ·mol-1]。下列说法正确的是
2NH3(g) ΔH=-92.4kJ·mol-1]。下列说法正确的是
 2NH3(g) ΔH=-92.4kJ·mol-1]。下列说法正确的是
2NH3(g) ΔH=-92.4kJ·mol-1]。下列说法正确的是| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1molN2、3molH2 | 2molNH3 | 4molNH3 |
| NH3的浓度(mol·L-1) | c1 | c2 | c3 |
| 反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | α1 | α2 | α3 |
| A.2c1>c3 | B.a=b | C.2p2<p3 | D.α1+α3<1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】工业上以1,4-丁二醇(BD)为原料催化脱氢制备γ-丁内酯(BL),其副反应产物为四氢呋喃( ,THF)、正丁醇(BuOH)以及其他四碳有机物。其他条件相同时,不同温度下,向1L容器中通入4×10-2molBD反应2h,测得BL、THF、BuOH在四碳有机产物中的物质的量分数如表:
,THF)、正丁醇(BuOH)以及其他四碳有机物。其他条件相同时,不同温度下,向1L容器中通入4×10-2molBD反应2h,测得BL、THF、BuOH在四碳有机产物中的物质的量分数如表:
| 温度/℃ | 220 | 240 | 250 | 255 |
| BL/% | 60.2 | 84.6 | 92.6 | 95.2 |
| THF/% | 1.2 | 1.8 | 1.9 | 2.1 |
| BuOH/% | 0.2 | 0.3 | 0.4 | 0.6 |
已知:HO(CH2)4OH(g,BD)
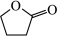 (g,BL)+2H2(g) △H>0
(g,BL)+2H2(g) △H>0
| A.255℃,2h时n(BL)=1.5×10-2mol,则0~2h内v(H2)主反应=1.5×10-2mol•L-1•h-1 |
| B.250℃,2h时n(BD)+n(BL)+n(THF)+n(BuOH)=4×10-2mol |
| C.220℃,2h时n(BL)=9.03×10-3mol,则BD的总转化率为37.5% |
| D.由表中数据可知:220~255℃,BL的选择性随着温度的升高而提高 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】在密闭容器中,对于可逆反应:A(?)+3B(?) 2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是
2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是

 2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是
2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是
| A.若正反应方向△H<0,则T1>T2 | B.压强增大时,混合气体的平均相对分子质量减小 |
| C.A一定为气体 | D.B一定为气体 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】对于可逆反应2A(g)+B(g)  2C(g) ΔH< 0,下列各项对示意图的解释与图象相符的是
2C(g) ΔH< 0,下列各项对示意图的解释与图象相符的是
 2C(g) ΔH< 0,下列各项对示意图的解释与图象相符的是
2C(g) ΔH< 0,下列各项对示意图的解释与图象相符的是A.①压强对反应的影响( P2>P1)  |
B.②温度对反应的影响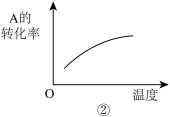 |
C.③平衡体系增加A对反应的影响 |
D.④催化剂对反应的影响 |
您最近一年使用:0次


 进行反应,达平衡时各组分的物质的量分数随温度变化曲线如图所示。下列说法错误的是
进行反应,达平衡时各组分的物质的量分数随温度变化曲线如图所示。下列说法错误的是
 的物质的量分数随温度的变化
的物质的量分数随温度的变化 的平衡转化率为60%
的平衡转化率为60%