反应3Fe(s)+4H2O(g)=Fe3O4(s)+4H2(g)在一可变容积的容器中进行,下列条件的改变对其反应速率几乎没有影响的是
| A.增加Fe 的用量 |
| B.将容器的体积缩小一半 |
| C.保持体积不变,充入H2O(g)使体系压强增大 |
| D.保持压强不变,充入N2使容器体积增大 |
更新时间:2017-11-10 19:44:43
|
【知识点】 压强对化学反应速率的影响解读
相似题推荐
单选题
|
适中
(0.65)
【推荐1】已知常温下氨气能与 CaCl2 固体结合生成 CaCl2·8NH3。下列说法不正确的是
A.CaCl2·6NH3(s)+ 2NH3(g)  CaCl2·8NH3(s) ΔH < 0 CaCl2·8NH3(s) ΔH < 0 |
| B.实验室可用氯化铵固体和熟石灰共热来制备氨气,说明相对高温不利于 CaCl2 与氨气的化合 |
| C.常温下,在密闭容器中缩体加压能增加体系中活化分子百分数,有利于氨气的吸收 |
| D.CaCl2·6NH3(s) CaCl2·c4NH3(s)+ 2NH3(g),He 气流可促进反应进行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】对可逆反应N2 (g)+3H2(g)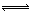 2 NH3(g),△H=-92.4 kJ·mol-1下列叙述正确的是
2 NH3(g),△H=-92.4 kJ·mol-1下列叙述正确的是
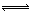 2 NH3(g),△H=-92.4 kJ·mol-1下列叙述正确的是
2 NH3(g),△H=-92.4 kJ·mol-1下列叙述正确的是| A.达到化学平衡时,若增加容器体积,则正反应速率减小 ,逆反应速率增大 |
| B.若单位时间内生成x mol N2的同时,消耗2x molNH3,则反应达到平衡状态 |
| C.达到化学平衡时,2v正(H2)=3v逆(NH3) |
| D.加入催化剂,正反应速率增大,逆反应速率不变 |
您最近一年使用:0次


 2BaO(S)+O2(g),O2的平衡浓度与容器容积的关系
2BaO(S)+O2(g),O2的平衡浓度与容器容积的关系

