甲醇(CH3OH)是一种新型清洁能源。回答问题:
(1)101KPa、25℃时,燃烧32g液态甲醇生成液态水和二氧化碳放热726.5kJ,则甲醇燃烧的热化学方程式为_____________
已知:2CH3OH(g)=CH3OCH3(g)+H2O(g) △H=-24.5kJ·mol-1
CO(g)+2H2(g) CH3OH(g) △H=akJ·mol-1
CH3OH(g) △H=akJ·mol-1
则2CO(g)+4H2(g)= CH3OCH3(g)+H2O(g) △H=__________
(2)工业上可用CO和H2制取甲醇,其热化学反应方程式为:CO(g)+2H2(g) CH3OH(g) △H=akJ·mol-1,CO在不同温度下的平衡转化率与压强的关系如下图所示
CH3OH(g) △H=akJ·mol-1,CO在不同温度下的平衡转化率与压强的关系如下图所示

①△H______ 0(填“﹥”或“<”).判断依据是___________________
②为提高CO转化率,可采取的措施是_____________________________ (至少答出两条)
③实际生产中,反应的条件控制在250℃,1.3×104kPa左右,选择此压强的理由是______________________ 。
(1)101KPa、25℃时,燃烧32g液态甲醇生成液态水和二氧化碳放热726.5kJ,则甲醇燃烧的热化学方程式为
已知:2CH3OH(g)=CH3OCH3(g)+H2O(g) △H=-24.5kJ·mol-1
CO(g)+2H2(g)
 CH3OH(g) △H=akJ·mol-1
CH3OH(g) △H=akJ·mol-1则2CO(g)+4H2(g)= CH3OCH3(g)+H2O(g) △H=
(2)工业上可用CO和H2制取甲醇,其热化学反应方程式为:CO(g)+2H2(g)
 CH3OH(g) △H=akJ·mol-1,CO在不同温度下的平衡转化率与压强的关系如下图所示
CH3OH(g) △H=akJ·mol-1,CO在不同温度下的平衡转化率与压强的关系如下图所示
①△H
②为提高CO转化率,可采取的措施是
③实际生产中,反应的条件控制在250℃,1.3×104kPa左右,选择此压强的理由是
更新时间:2017-11-28 20:15:33
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5 μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等。因此,对PM2.5 、SO2、NOx等进行研究具有重要意义。请回答下列问题:
(1)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据判断PM2.5试样的pH=_____________ 。
(2)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料。
已知:H2(g)+ O2(g) = H2O(g) ΔH=-241.8 kJ·mol-1
O2(g) = H2O(g) ΔH=-241.8 kJ·mol-1
C(s)+ O2(g) = CO(g) ΔH=-110.5 kJ·mol-1
O2(g) = CO(g) ΔH=-110.5 kJ·mol-1
写出焦炭与水蒸气反应的热化学方程式:______________________________________ 。
②洗涤含SO2的烟气。以下物质可作洗涤剂的是________ 。(填字母)
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(3)汽车尾气中NOx和CO的生成及转化
①已知汽缸中生成NO的反应为:N2(g)+O2(g) ⇌2NO(g) ΔH>0。汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是___________________ 。
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g) = 2C(s)+O2(g)。已知该反应的ΔH>0,简述该设想能否实现的依据:____________________ 。
(1)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ | NH | SO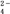 | NO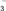 | Cl- |
| 浓度(mol·L-1) | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
根据表中数据判断PM2.5试样的pH=
(2)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料。
已知:H2(g)+
 O2(g) = H2O(g) ΔH=-241.8 kJ·mol-1
O2(g) = H2O(g) ΔH=-241.8 kJ·mol-1C(s)+
 O2(g) = CO(g) ΔH=-110.5 kJ·mol-1
O2(g) = CO(g) ΔH=-110.5 kJ·mol-1写出焦炭与水蒸气反应的热化学方程式:
②洗涤含SO2的烟气。以下物质可作洗涤剂的是
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(3)汽车尾气中NOx和CO的生成及转化
①已知汽缸中生成NO的反应为:N2(g)+O2(g) ⇌2NO(g) ΔH>0。汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g) = 2C(s)+O2(g)。已知该反应的ΔH>0,简述该设想能否实现的依据:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】汽车尾气主要含有CO2、CO、SO2、NO及汽油、柴油等物质,这种尾气越来越成为城市空气污染的主要来源,必须予以治理。治理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂)。它的特点是使CO与NO反应,生成可参与大气生态环境循环的无毒气体,并促使汽油、柴油等物质充分燃烧及SO2的转化。
(1)汽车尾气中NO的来源是_________ 。
A.汽油、柴油中含氮,是其燃烧产物
B.是空气中的N2与汽油、柴油的反应产物
C.是空气中的N2与O2在汽车气缸内的高温环境下的反应产物
D.是汽车高温尾气导致了空气中N2与O2的化合反应
(2)写出CO与NO反应的化学方程式:_____________________________ 。
(3)“催化转化器”的缺点是在一定程度上提高了空气的酸度,其原因是______________
(4)控制或者减少城市汽车尾气污染的方法可以有___________ 。(多选)
A.开发氢能源 B.使用电动车 C.限制车辆行驶 D.使用乙醇汽油
(1)汽车尾气中NO的来源是
A.汽油、柴油中含氮,是其燃烧产物
B.是空气中的N2与汽油、柴油的反应产物
C.是空气中的N2与O2在汽车气缸内的高温环境下的反应产物
D.是汽车高温尾气导致了空气中N2与O2的化合反应
(2)写出CO与NO反应的化学方程式:
(3)“催化转化器”的缺点是在一定程度上提高了空气的酸度,其原因是
(4)控制或者减少城市汽车尾气污染的方法可以有
A.开发氢能源 B.使用电动车 C.限制车辆行驶 D.使用乙醇汽油
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】请根据要求填空:
(1)化学反应过程中,不仅有物质的变化,还伴随有能量的变化。根据下图写出反应的热化学方程式:_________________________________ 。

(2)化学反应速率和化学平衡是化学反应原理的重要组成部分。
将4.0mol PCl3和2.0 mol Cl2充入10 L恒容密闭容器中,在一定条件下发生反应PCl3(g)+Cl2(g) PCl5(g),经2 min达到平衡时,PCl5为0.40 mol。
PCl5(g),经2 min达到平衡时,PCl5为0.40 mol。
①在0~2 min 内,用Cl2 表示的反应速率为:v(Cl2)=_____ mol·L-l·min-1;
②达到平衡时,PCl3的转化率为___________________ 。
③如果再通入1.0 mol Cl2,相同温度下重新达到平衡时,PCl5的物质的量________________ 。(填标号)
A.增大 B.减小 C.不变
(1)化学反应过程中,不仅有物质的变化,还伴随有能量的变化。根据下图写出反应的热化学方程式:

(2)化学反应速率和化学平衡是化学反应原理的重要组成部分。
将4.0mol PCl3和2.0 mol Cl2充入10 L恒容密闭容器中,在一定条件下发生反应PCl3(g)+Cl2(g)
 PCl5(g),经2 min达到平衡时,PCl5为0.40 mol。
PCl5(g),经2 min达到平衡时,PCl5为0.40 mol。①在0~2 min 内,用Cl2 表示的反应速率为:v(Cl2)=
②达到平衡时,PCl3的转化率为
③如果再通入1.0 mol Cl2,相同温度下重新达到平衡时,PCl5的物质的量
A.增大 B.减小 C.不变
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在密闭容器中的可逆反应CO(g)+NO2(g) ⇌CO2(g)+NO(g)(正反应为放热反应)达到平衡后:
(1)扩大容器体积,平衡_______ (向左、向右、不)移动,反应混合物的颜色_______ (变深、变浅、不变)。
(2)容器容积不变,升高温度,平衡_______ (向左、向右、不)移动,体系的压强_______ (增大、减小、不变)。
(3)加入催化剂,NO的物质的量_______ (增大、减小、不变),原因是_______ 。
(1)扩大容器体积,平衡
(2)容器容积不变,升高温度,平衡
(3)加入催化剂,NO的物质的量
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知尿酸是一种有机酸(以HUr表示),能溶于水。关节炎的原因归结于在关节滑液中形成了尿酸钠晶体(NaUr)。发生的反应如下:
HUr Ur-+H+ ①
Ur-+H+ ①
Ur-(aq)+Na+(aq) NaUr(s) ②
NaUr(s) ②
(1)关节炎大都是阴冷天气时发作,这说明反应②是_______ (填“放热”或“吸热”)反应。简述你得出该结论的理由:_______ 。
(2)当温度升高时,反应②的化学平衡常数_______ (填“增大”、“减小”或“不变”)。
(3)写出反应②的平衡常数表达式K=_______ 。
HUr
 Ur-+H+ ①
Ur-+H+ ①Ur-(aq)+Na+(aq)
 NaUr(s) ②
NaUr(s) ②(1)关节炎大都是阴冷天气时发作,这说明反应②是
(2)当温度升高时,反应②的化学平衡常数
(3)写出反应②的平衡常数表达式K=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】丁烯(C4H8)是重要的化工原料,可由丁烷(C4H10)催化脱氢制备,反应如下:CH3CH2CH2CH3(g) CH2=CHCH2CH3(g)+H2(g)ΔH
CH2=CHCH2CH3(g)+H2(g)ΔH
已知:
i.该工艺过程的副产物有炭(C),生成的积炭会附着在催化剂表面,影响催化效果。
ii.温度过高会引发正丁烷裂解生成低碳烃类的副反应。
iii.H2(g)+ O2(g)=H2O(l) ΔH1
O2(g)=H2O(l) ΔH1
CH3CH2CH2CH3(g)+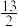 O2(g)=4CO2(g)+5H2O(l) ΔH2
O2(g)=4CO2(g)+5H2O(l) ΔH2
CH2=CHCH2CH3(g)+6O2(g)=4CO2(g)+4H2O(l) ΔH3
(1)用ΔH1、ΔH2、ΔH3表示丁烷催化脱氢反应的反应热ΔH=___ 。
(2)寻找高效的催化剂是脱氢反应重要的研究课题之一。
①催化剂使用一段时间后活性会下降,通入适量氢气可使其改善,氢气的作用是___ 。
②其他条件相同时,以SiO2为载体与不同质量百分比的CrOx组合,催化效果相关数据如表。
下列说法正确的是____ (填序号)。
a.脱氢反应中SiO2不起催化作用
b.CrOx的含量越高,反应的催化效果越好
c.CrOx的含量对丁烷脱氢反应的焓变无影响
(3)其他条件相同,30min时测得正丁烷转化率、正丁烯收率随温度的变化如图1。
[收率= ×100%]
×100%]
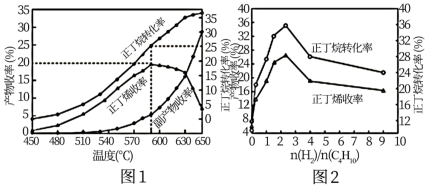
①实际生产温度选择590℃,由图1说明其理由是___ 。
②590℃时,向体积为1L的密闭容器中充入3mol正丁烷气体,据图1计算0~30min内生成正丁烯的平均反应速率为__ mol/(L·min)。
(4)其他条件相同,30min时正丁烷转化率、正丁烯收率随进料气中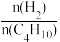 的变化如图2。图2中,
的变化如图2。图2中,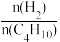 >2.5后,正丁烷转化率和正丁烯收率呈减小趋势,原因是
>2.5后,正丁烷转化率和正丁烯收率呈减小趋势,原因是___ 。
 CH2=CHCH2CH3(g)+H2(g)ΔH
CH2=CHCH2CH3(g)+H2(g)ΔH已知:
i.该工艺过程的副产物有炭(C),生成的积炭会附着在催化剂表面,影响催化效果。
ii.温度过高会引发正丁烷裂解生成低碳烃类的副反应。
iii.H2(g)+
 O2(g)=H2O(l) ΔH1
O2(g)=H2O(l) ΔH1CH3CH2CH2CH3(g)+
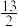 O2(g)=4CO2(g)+5H2O(l) ΔH2
O2(g)=4CO2(g)+5H2O(l) ΔH2CH2=CHCH2CH3(g)+6O2(g)=4CO2(g)+4H2O(l) ΔH3
(1)用ΔH1、ΔH2、ΔH3表示丁烷催化脱氢反应的反应热ΔH=
(2)寻找高效的催化剂是脱氢反应重要的研究课题之一。
①催化剂使用一段时间后活性会下降,通入适量氢气可使其改善,氢气的作用是
②其他条件相同时,以SiO2为载体与不同质量百分比的CrOx组合,催化效果相关数据如表。
| 实验组 | 催化剂组成 | 正丁烷转化率/% | 正丁烯收率/% |
| 1 | 无催化剂 | 5 | 0.35 |
| 2 | SiO2 | 5 | 0.35 |
| 3 | SiO2+9%CrOx | 25.5 | 18.3 |
| 4 | SiO2+15%CrOx | 27.5 | 20.65 |
| 5 | SiO2+21%CrOx | 24 | 17.87 |
a.脱氢反应中SiO2不起催化作用
b.CrOx的含量越高,反应的催化效果越好
c.CrOx的含量对丁烷脱氢反应的焓变无影响
(3)其他条件相同,30min时测得正丁烷转化率、正丁烯收率随温度的变化如图1。
[收率=
 ×100%]
×100%]
①实际生产温度选择590℃,由图1说明其理由是
②590℃时,向体积为1L的密闭容器中充入3mol正丁烷气体,据图1计算0~30min内生成正丁烯的平均反应速率为
(4)其他条件相同,30min时正丁烷转化率、正丁烯收率随进料气中
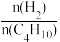 的变化如图2。图2中,
的变化如图2。图2中,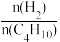 >2.5后,正丁烷转化率和正丁烯收率呈减小趋势,原因是
>2.5后,正丁烷转化率和正丁烯收率呈减小趋势,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某冶炼厂利用含ZnO的烟灰脱除工业废气中的SO2,最终得到锌盐。该厂所用烟灰的主要成分如下表所示:
在一定条件下,将含SO2的工业废气通入烟灰浆液(烟灰和水的混合物)进行脱硫,过程中测得pH和上清液中溶解的SO2物质的量浓度[c(SO2)]随时间的变化如图所示:

(1)纯ZnO浆液的pH为6.8,但上述烟灰浆液的初始pH为7.2。在开始脱硫后3 min内(a~b段),pH迅速降至6.8,引起pH迅速变化的原因是_____ (结合化学用语解释)。
(2)生产中脱除SO2效果最佳的时间范围是_____ (填字母序号)。
A.20~30 min B.30~40 min C.50~60 min D.70~80 min
(3)在脱硫过程中涉及到的主要反应原理:
Ⅰ.ZnO + SO2 === ZnSO3↓
Ⅱ.ZnSO3 + SO2 + H2O === Zn(HSO3)2
①在30~40 min时,主要发生反应II,生成可溶性的Zn(HSO3)2。上清液中c(SO2)上升的原因可能是______ 。
②在30~80 min时,pH降低的原因可能是______ (写出2点)。
③将脱硫后的混合物利用空气氧化技术处理,该过程中发生反应:2ZnSO3 + O2 === 2ZnSO4和______ 。
| 主要成分 | ZnO | CaO | Fe2O3 | SiO2 | 其它 |
| 质量分数/% | 81 | 0.098 | 1.14 | 0.5 | ———— |
在一定条件下,将含SO2的工业废气通入烟灰浆液(烟灰和水的混合物)进行脱硫,过程中测得pH和上清液中溶解的SO2物质的量浓度[c(SO2)]随时间的变化如图所示:

(1)纯ZnO浆液的pH为6.8,但上述烟灰浆液的初始pH为7.2。在开始脱硫后3 min内(a~b段),pH迅速降至6.8,引起pH迅速变化的原因是
(2)生产中脱除SO2效果最佳的时间范围是
A.20~30 min B.30~40 min C.50~60 min D.70~80 min
(3)在脱硫过程中涉及到的主要反应原理:
Ⅰ.ZnO + SO2 === ZnSO3↓
Ⅱ.ZnSO3 + SO2 + H2O === Zn(HSO3)2
①在30~40 min时,主要发生反应II,生成可溶性的Zn(HSO3)2。上清液中c(SO2)上升的原因可能是
②在30~80 min时,pH降低的原因可能是
③将脱硫后的混合物利用空气氧化技术处理,该过程中发生反应:2ZnSO3 + O2 === 2ZnSO4和
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】工业制造硫酸的主要反应为:
SO2(g)+ O2(g)=SO3(g) △H=-99kJ•mol-1 ①
O2(g)=SO3(g) △H=-99kJ•mol-1 ①
SO3(g)+H2O(l)=H2SO4(aq) ②
反应①的平衡常数K随温度升高而减小,所用催化剂的主要成分为V2O5(6%~12%)、K2SO4(17%~20%)、SiO2(50%~70%),能使催化剂中毒的物质有砷、硒、氟等。请根据以上信息讨论二氧化硫氧化反应的工艺条件(温度、压强、原料气配比等)对工业生产硫酸的影响____ 。
SO2(g)+
 O2(g)=SO3(g) △H=-99kJ•mol-1 ①
O2(g)=SO3(g) △H=-99kJ•mol-1 ①SO3(g)+H2O(l)=H2SO4(aq) ②
反应①的平衡常数K随温度升高而减小,所用催化剂的主要成分为V2O5(6%~12%)、K2SO4(17%~20%)、SiO2(50%~70%),能使催化剂中毒的物质有砷、硒、氟等。请根据以上信息讨论二氧化硫氧化反应的工艺条件(温度、压强、原料气配比等)对工业生产硫酸的影响
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】研究含氮物质之间的转化,对防治污染具有重大意义。回答下列问题:
(1)已知:①
②
一定条件下,向体积为 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和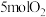 发生上述反应。经过t秒达到平衡状态,测得平衡时容器中
发生上述反应。经过t秒达到平衡状态,测得平衡时容器中 为
为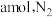 为
为 ,则
,则
________ (用含字母的代数式表示)。理论上参与反应①和②的 之比为
之比为______ 时,生成的 在混合气体中的含量最高。
在混合气体中的含量最高。
(2)在一定温度下,向容积不同的恒容密闭容器中分别通入 和
和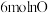 ,发生反应
,发生反应 。反应相同时间,某时刻测得各容器中
。反应相同时间,某时刻测得各容器中 的转化率与容器体积的关系如图所示。
的转化率与容器体积的关系如图所示。
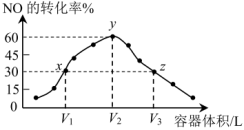
①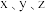 三点对应速率常数
三点对应速率常数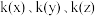 ,三者间的大小关系为
,三者间的大小关系为__ ,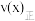
__ 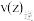 。
。
②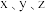 三点中已达到平衡状态的点为
三点中已达到平衡状态的点为___ ,z点比y点转化率低的原因是____ 。
(3)在一恒容密闭容器中充入 和
和 发生反应
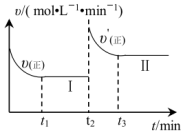
发生反应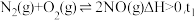 时达到平衡状态I,在
时达到平衡状态I,在 时改变某一条件,
时改变某一条件, 时重新达到平衡状态II,正反应速率随时间的变化如图所示。
时重新达到平衡状态II,正反应速率随时间的变化如图所示。 时改变的条件可能为
时改变的条件可能为_____ (答2条)。
(1)已知:①

②

一定条件下,向体积为
 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和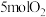 发生上述反应。经过t秒达到平衡状态,测得平衡时容器中
发生上述反应。经过t秒达到平衡状态,测得平衡时容器中 为
为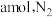 为
为 ,则
,则
 之比为
之比为 在混合气体中的含量最高。
在混合气体中的含量最高。(2)在一定温度下,向容积不同的恒容密闭容器中分别通入
 和
和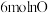 ,发生反应
,发生反应 。反应相同时间,某时刻测得各容器中
。反应相同时间,某时刻测得各容器中 的转化率与容器体积的关系如图所示。
的转化率与容器体积的关系如图所示。
①
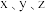 三点对应速率常数
三点对应速率常数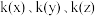 ,三者间的大小关系为
,三者间的大小关系为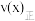
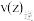 。
。②
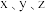 三点中已达到平衡状态的点为
三点中已达到平衡状态的点为(3)在一恒容密闭容器中充入
 和
和 发生反应
发生反应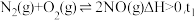 时达到平衡状态I,在
时达到平衡状态I,在 时改变某一条件,
时改变某一条件, 时重新达到平衡状态II,正反应速率随时间的变化如图所示。
时重新达到平衡状态II,正反应速率随时间的变化如图所示。 时改变的条件可能为
时改变的条件可能为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】天然气的综合利用是实现社会可持续发展的需要。
(1)由甲烷催化制取氢气的原理如下:CH4(g)+H2O(g) CO(g)+3H2(g) ΔH=+260kJ·mol-1
CO(g)+3H2(g) ΔH=+260kJ·mol-1
①对于该反应,一定能提高平衡体系中H2的百分含量,又能加快反应速率的措施是___________ 。
②空速代表单位时间内通过催化剂的原料量。在一定温度下,不同催化剂作用下,甲烷的转化率与空速的关系如图,随空速增大甲烷转化率减小的可能原因是___________ 。

(2)甲烷通过电解法制备有机物的原理如图:

①M为电源的___________ 极
②写出CH4生成C2H4的电极反应式___________ 。
③若生成C2H4和C2H6各1mol,则理论上需要CO2的物质的量为___________ 。
(1)由甲烷催化制取氢气的原理如下:CH4(g)+H2O(g)
 CO(g)+3H2(g) ΔH=+260kJ·mol-1
CO(g)+3H2(g) ΔH=+260kJ·mol-1①对于该反应,一定能提高平衡体系中H2的百分含量,又能加快反应速率的措施是
②空速代表单位时间内通过催化剂的原料量。在一定温度下,不同催化剂作用下,甲烷的转化率与空速的关系如图,随空速增大甲烷转化率减小的可能原因是

(2)甲烷通过电解法制备有机物的原理如图:

①M为电源的
②写出CH4生成C2H4的电极反应式
③若生成C2H4和C2H6各1mol,则理论上需要CO2的物质的量为
您最近一年使用:0次

 液态化合物
液态化合物 与液态
与液态 恰好完全反应生成两种对环境友好的气体,此时放出
恰好完全反应生成两种对环境友好的气体,此时放出 的热量,请写出该反应的热化学方程式:
的热量,请写出该反应的热化学方程式: (视
(视 为已知数),请写出稀硫酸与稀
为已知数),请写出稀硫酸与稀 溶液反应的热化学方程式:
溶液反应的热化学方程式: ,把
,把 和
和 ,充入密闭容器中充分反应,测得放出的热量始终小于
,充入密闭容器中充分反应,测得放出的热量始终小于 。请简述其原因:
。请简述其原因: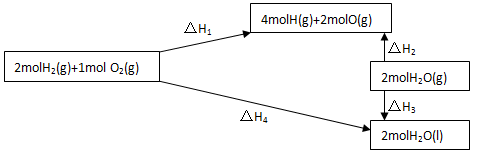

 、
、 、
、 表示)。
表示)。
 的排放,某研究小组在实验室以耐高温试剂
的排放,某研究小组在实验室以耐高温试剂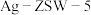 催化,测得
催化,测得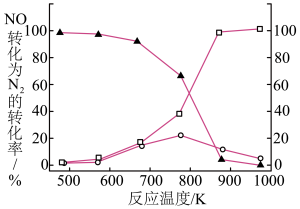
 时
时 条件下,
条件下, ,发现
,发现

