对于A+2B(g) nC(g)。在一定条件下达到平衡后,改变下列条件,请回答:
nC(g)。在一定条件下达到平衡后,改变下列条件,请回答:
(1)当n=3时,增压,平衡不移动,则A为______ 态。
(2)若A为固态,增大压强,C的组分含量增加,则n_________ ,反应的平衡常数__________ (填增大、减小或不变)。
(3)升温,平衡向右移动,达到新平衡前,υ正______ υ逆(填>、< 或 =),则该反应的逆反应为_______ 热反应,反应的平衡常数__________ (填增大、减小或不变)。
 nC(g)。在一定条件下达到平衡后,改变下列条件,请回答:
nC(g)。在一定条件下达到平衡后,改变下列条件,请回答:(1)当n=3时,增压,平衡不移动,则A为
(2)若A为固态,增大压强,C的组分含量增加,则n
(3)升温,平衡向右移动,达到新平衡前,υ正
更新时间:2017-12-11 09:10:44
|
【知识点】 化学平衡的移动及其影响因素
相似题推荐
填空题
|
适中
(0.65)
【推荐1】丙烯和氨分别是重要的有机和无机化工原料。丙烯主要用于生产聚丙烯、丙烯腈、环氧丙烷等。“丁烯裂解法”是一种重要的丙烯生产法,生产过程中会有生成乙烯的副反应发生。反应如下:
主反应: ;
;
副反应: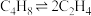 。
。
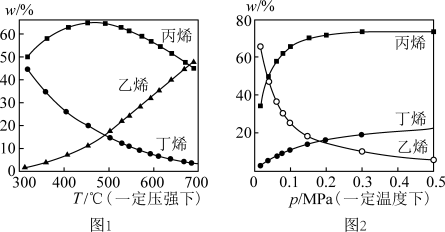
测得上述两反应的平衡体系中,各组分的质量分数(w%)随温度(T)和压强(p)变化的趋势分别如图1和图2所示:
(1)在10L恒容密闭容器中,投入1mol丁烯,在一定温度下进行反应,5分钟后测得体系压强变为开始时的1.2倍,乙烯0.1mol,则以丙烯表示的主反应的速率为___________ 。
(2)主反应的平衡常数表达式
___________ ,如果反应的平衡常数K值变大,该反应___________ (选填编号)。
a.一定向正反应方向移动 b.平衡移动时,正反应速率先减小后增大
c.一定向逆反应方向移动 d.平衡移动时,逆反应速率先增大后减小
(3)平衡体系中的丙烯和乙烯的质量比 是工业生产丙烯时选择反应条件的重要指标之一,从产物的纯度考虑,该数值越高越好,从图1和图2中表现的趋势来看,下列反应条件最适宜的是___________(填字母)。
是工业生产丙烯时选择反应条件的重要指标之一,从产物的纯度考虑,该数值越高越好,从图1和图2中表现的趋势来看,下列反应条件最适宜的是___________(填字母)。
(4)有研究者结合图1数据并综合考虑各种因素,认为450℃的反应温度比300℃或700℃更合适,从反应原理角度分析其理由可能是___________ 。
(5)图2中,随压强增大,平衡体系中丙烯的质量分数呈上升趋势,从平衡角度解释其原因是___________ 。
主反应:
 ;
; 副反应:
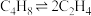 。
。测得上述两反应的平衡体系中,各组分的质量分数(w%)随温度(T)和压强(p)变化的趋势分别如图1和图2所示:

(1)在10L恒容密闭容器中,投入1mol丁烯,在一定温度下进行反应,5分钟后测得体系压强变为开始时的1.2倍,乙烯0.1mol,则以丙烯表示的主反应的速率为
(2)主反应的平衡常数表达式

a.一定向正反应方向移动 b.平衡移动时,正反应速率先减小后增大
c.一定向逆反应方向移动 d.平衡移动时,逆反应速率先增大后减小
(3)平衡体系中的丙烯和乙烯的质量比
 是工业生产丙烯时选择反应条件的重要指标之一,从产物的纯度考虑,该数值越高越好,从图1和图2中表现的趋势来看,下列反应条件最适宜的是___________(填字母)。
是工业生产丙烯时选择反应条件的重要指标之一,从产物的纯度考虑,该数值越高越好,从图1和图2中表现的趋势来看,下列反应条件最适宜的是___________(填字母)。A.300℃  | B.700℃  |
C.300℃ 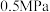 | D.700℃ 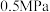 |
(5)图2中,随压强增大,平衡体系中丙烯的质量分数呈上升趋势,从平衡角度解释其原因是
您最近半年使用:0次
【推荐2】在2L密闭容器中,起始投入4molN2和6molH2在一定条件下生成NH3,平衡时仅改变温度测得的数据如表所示(已知:T1<T2)
(1)则K1__ K2,(填“>”、“<”或“=”)原因:___ 。
(2)在T2下,经过10s达到化学平衡状态,则平衡时H2的转化率为__ 。若再同时增加各物质的量为1 mol,该反应的平衡v正__ v逆,(>或=或<)平衡常数将___ (填“增大”、“减小”或“不变”)
(3)下列能说明该反应已达到平衡状态的是__ 。
A.3v正(H2)=2v逆(NH3) B.容器内气体压强不变
C.混合气体的平均相对分子质量不再改变的状态 D.c(H2)=c(NH3)
| 温度/K | 平衡时NH3的物质的量/mol |
| T1 | 3.6 |
| T2 | 2 |
(1)则K1
(2)在T2下,经过10s达到化学平衡状态,则平衡时H2的转化率为
(3)下列能说明该反应已达到平衡状态的是
A.3v正(H2)=2v逆(NH3) B.容器内气体压强不变
C.混合气体的平均相对分子质量不再改变的状态 D.c(H2)=c(NH3)
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】Ⅰ 某温度下,密闭容器中充入1 mol N2和3 mol H2,使之反应合成NH3,平衡后,测得NH3的体积分数为w,如果温度不变,只改变起始加入量,使之反应平衡后NH3的体积分数仍为w,N2、H2、NH3的物质的量分别用x、y、z表示。
(1)恒温恒容条件下:若x=0.75 mol, 则y=________ ,z=________ ;
(2)恒温恒压条件下,x、y、z(均不小于0)满足的一般条件是_____________ ;
Ⅱ 一定条件下,可逆反应X(g)+Y(g) 2Z(g)达到平衡时,各物质的平衡浓度为c(X)=0.5mol/L;c(Y) =0.1 mol /L;c (Z)=1.6 mol /L若用a、b、c分别表示X、Y、Z的初始浓度(mol/L)则a、b应满足的关系是
2Z(g)达到平衡时,各物质的平衡浓度为c(X)=0.5mol/L;c(Y) =0.1 mol /L;c (Z)=1.6 mol /L若用a、b、c分别表示X、Y、Z的初始浓度(mol/L)则a、b应满足的关系是____________ , a的取值范围为_______________ ;
Ⅲ 在10℃和4×105Pa的条件下,当反应aA(g) dD(g)+eE(g),建立平衡后,维持温度不变而压强改变,测得D的浓度变化如下:
dD(g)+eE(g),建立平衡后,维持温度不变而压强改变,测得D的浓度变化如下:
(1)压强从4×105Pa增加到6×105Pa时,平衡向________ (填“正”或“逆”)方向移动,理由是____________ ;
(2)压强从10×105Pa增加到20×105Pa时,平衡向_______ (填“正”或“逆”)方向移动。
(1)恒温恒容条件下:若x=0.75 mol, 则y=
(2)恒温恒压条件下,x、y、z(均不小于0)满足的一般条件是
Ⅱ 一定条件下,可逆反应X(g)+Y(g)
 2Z(g)达到平衡时,各物质的平衡浓度为c(X)=0.5mol/L;c(Y) =0.1 mol /L;c (Z)=1.6 mol /L若用a、b、c分别表示X、Y、Z的初始浓度(mol/L)则a、b应满足的关系是
2Z(g)达到平衡时,各物质的平衡浓度为c(X)=0.5mol/L;c(Y) =0.1 mol /L;c (Z)=1.6 mol /L若用a、b、c分别表示X、Y、Z的初始浓度(mol/L)则a、b应满足的关系是Ⅲ 在10℃和4×105Pa的条件下,当反应aA(g)
 dD(g)+eE(g),建立平衡后,维持温度不变而压强改变,测得D的浓度变化如下:
dD(g)+eE(g),建立平衡后,维持温度不变而压强改变,测得D的浓度变化如下:| 压强(Pa) | 4×105 | 6×105 | 10×105 | 20×105 |
| D的浓度(mol/L) | 0.085 | 0.126 | 0.200 | 0.440 |
(1)压强从4×105Pa增加到6×105Pa时,平衡向
(2)压强从10×105Pa增加到20×105Pa时,平衡向
您最近半年使用:0次



