在体积为2L的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g)。其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g)。其化学平衡常数K和温度t的关系如下表:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=________________ 。
(2)该反应为____________ 反应(选填吸热、放热),原因是_____________________ 。
(3)能判断该反应是否达到化学平衡状态的依据是________________ (多选扣分)。
a.容器中压强不变 b.混合气体中 c(CO)不变
c.υ正(H2)=υ逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为_______________ ℃。该温度下,若向容器中分别加入2mol H2和2molCO2,10s后达到平衡,则这段时间内υ(H2)=_______________ , CO2的转化率为_____________ 。
 CO(g)+H2O(g)。其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g)。其化学平衡常数K和温度t的关系如下表:| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=
(2)该反应为
(3)能判断该反应是否达到化学平衡状态的依据是
a.容器中压强不变 b.混合气体中 c(CO)不变
c.υ正(H2)=υ逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为
更新时间:2017-12-15 17:43:09
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】甲醇(CH3OH)广泛用作燃料电池的燃料,工业上可由CO和H2来合成,化学方程式为CO(g)+2H2(g) CH3OH(g)。
CH3OH(g)。
(1)下图是在不同温度下CO的转化率随时间变化的曲线。
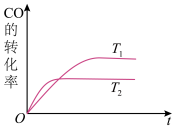
①T1_______ T2(填“>”、“<”或“=”)。该反应的ΔH_______ 0(填“>”、“<”或“=”)。
②若容器容积不变,下列措施能增加CO平衡转化率的是_______ (填字母)。
a.降低温度 b.使用合适的催化剂
c.将CH3OH(g)从体系中分离 d.充入He,使体系总压强增大
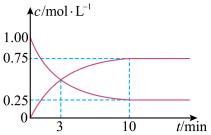
(2)下图是表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化情况。从反应开始到平衡,用CO浓度变化表示平均反应速率υ(CO)=_______ ;H2的平衡转化率为_______ 。
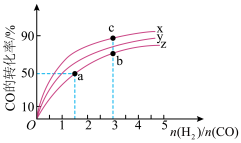
(3)一定温度下恒容容器中,分别研究在PX,PY,PZ三种压强下合成甲醇的规律。如图是上述三种压强下H2和CO的起始组成比[ ]与CO平衡转化率的关系,则PX,PY,PZ的大小关系是
]与CO平衡转化率的关系,则PX,PY,PZ的大小关系是_______ ,此时该反应的化学平衡常数KX,KY,KZ的大小关系为_______ 。
 CH3OH(g)。
CH3OH(g)。(1)下图是在不同温度下CO的转化率随时间变化的曲线。

①T1
②若容器容积不变,下列措施能增加CO平衡转化率的是
a.降低温度 b.使用合适的催化剂
c.将CH3OH(g)从体系中分离 d.充入He,使体系总压强增大
(2)下图是表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化情况。从反应开始到平衡,用CO浓度变化表示平均反应速率υ(CO)=

(3)一定温度下恒容容器中,分别研究在PX,PY,PZ三种压强下合成甲醇的规律。如图是上述三种压强下H2和CO的起始组成比[
 ]与CO平衡转化率的关系,则PX,PY,PZ的大小关系是
]与CO平衡转化率的关系,则PX,PY,PZ的大小关系是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】下列反应在210 ℃达到平衡:
①PCl5(g) PCl3(g)+Cl2(g) ΔH=Q1 K=1
PCl3(g)+Cl2(g) ΔH=Q1 K=1
②CO(g)+Cl2(g) COCl2(g) ΔH=-Q2 K'=5×104
COCl2(g) ΔH=-Q2 K'=5×104
③COCl2(g) CO(g)+Cl2(g) ΔH=Q3 K″
CO(g)+Cl2(g) ΔH=Q3 K″
(1)根据反应①的平衡常数K表达式,下列等式必定成立的是___ 。
A.c(PCl5)=c(PCl3)=c(Cl2)=1
B.c(PCl5)=c(PCl3)·c(Cl2)=1
C.c(PCl5)=c(PCl3)·c(Cl2)
(2)反应②和反应③的平衡常数K'和K″存在的关系为_________ 。
(3)温度不变,降低Cl2的浓度,反应③的K″的值___ (填“增大”“减小”或“不变”)。
(4)要使反应①和反应②的K值相等,应采取的措施是___ 。
A.反应①、②同时升高温度
B.反应①、②同时降低温度
C.反应①降低温度,反应②维持210 ℃
①PCl5(g)
 PCl3(g)+Cl2(g) ΔH=Q1 K=1
PCl3(g)+Cl2(g) ΔH=Q1 K=1②CO(g)+Cl2(g)
 COCl2(g) ΔH=-Q2 K'=5×104
COCl2(g) ΔH=-Q2 K'=5×104③COCl2(g)
 CO(g)+Cl2(g) ΔH=Q3 K″
CO(g)+Cl2(g) ΔH=Q3 K″(1)根据反应①的平衡常数K表达式,下列等式必定成立的是
A.c(PCl5)=c(PCl3)=c(Cl2)=1
B.c(PCl5)=c(PCl3)·c(Cl2)=1
C.c(PCl5)=c(PCl3)·c(Cl2)
(2)反应②和反应③的平衡常数K'和K″存在的关系为
(3)温度不变,降低Cl2的浓度,反应③的K″的值
(4)要使反应①和反应②的K值相等,应采取的措施是
A.反应①、②同时升高温度
B.反应①、②同时降低温度
C.反应①降低温度,反应②维持210 ℃
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】CO用途广泛,工业应用时离不开平衡思想的指导。
I.在某一容积为5L的体积不变的密闭容器内,加入0.3mol的CO和0.3mol的H2O,在催化剂存在和800℃的条件下加热,发生如下反应:
 ,反应中
,反应中 的浓度随时间变化情况如下图:
的浓度随时间变化情况如下图:
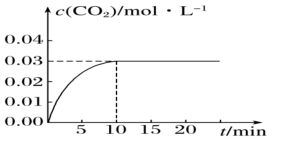
(1)根据图上数据,该温度(800℃)下的平衡常数
_______ 。
(2)在体积不变的条件下,改变下列条件能使平衡常数K增大的有_______ (填字母)。
A.升高温度 B.降低温度 C.增大压强 D.减小压强 E.加入催化剂 F.移出一氧化碳气体
(3)若保持温度和容器的体积不变,在(1)中上述平衡体系中,再充入0.3mol的水蒸气,重新达到平衡后, 的转化率
的转化率_______ (填“升高”“降低”或“不变”)。
(4)在催化剂存在和800℃的条件下,在某一时刻测得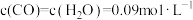 ;
; ,则此时正、逆反应速率的大小v正
,则此时正、逆反应速率的大小v正_______ (填“>”“<”或“=”)v逆
Ⅱ.在容积为1.00L的容器中,通入一定量的N2O4,发生反应 ,随温度升高,混合气体的颜色变深。回答下列问题:
,随温度升高,混合气体的颜色变深。回答下列问题:
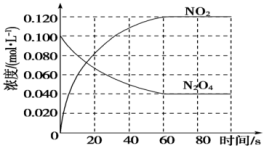
(5)反应的
_______ 0(填“大于”或“小于”);100℃时,体系中各物质浓度随时间变化如图所示。在0~60s时段,反应速率 为
为_______  ;反应的平衡常数
;反应的平衡常数 为
为_______ 。
I.在某一容积为5L的体积不变的密闭容器内,加入0.3mol的CO和0.3mol的H2O,在催化剂存在和800℃的条件下加热,发生如下反应:

 ,反应中
,反应中 的浓度随时间变化情况如下图:
的浓度随时间变化情况如下图:
(1)根据图上数据,该温度(800℃)下的平衡常数

(2)在体积不变的条件下,改变下列条件能使平衡常数K增大的有
A.升高温度 B.降低温度 C.增大压强 D.减小压强 E.加入催化剂 F.移出一氧化碳气体
(3)若保持温度和容器的体积不变,在(1)中上述平衡体系中,再充入0.3mol的水蒸气,重新达到平衡后,
 的转化率
的转化率(4)在催化剂存在和800℃的条件下,在某一时刻测得
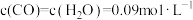 ;
; ,则此时正、逆反应速率的大小v正
,则此时正、逆反应速率的大小v正Ⅱ.在容积为1.00L的容器中,通入一定量的N2O4,发生反应
 ,随温度升高,混合气体的颜色变深。回答下列问题:
,随温度升高,混合气体的颜色变深。回答下列问题:
(5)反应的

 为
为 ;反应的平衡常数
;反应的平衡常数 为
为
您最近半年使用:0次
【推荐1】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) ⇌CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表:
回答下列问题:
(1)该反应的平衡常数表达式:_______ 。该反应为_______ 反应(填“吸热”、“放热”)。
(2)能使该反应的反应速率增大,且平衡向正反应方向移动的是_______ 。
a.及时分离出CO气体 b.适当升高温度
c.增大CO2的浓度 d.选择高效催化剂
(3) 能判断该反应是否达到化学平衡状态的依据是_______ (多选不得分)。
a.容器中压强不变 b.混合气体中 c(CO)不变
c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为_______ ℃。
(5)若在(4)所处的温度下,在1 L的密闭容器中,加入2 mol CO2和3 mol H2充分反应达平衡时,CO2的物质的量为_______ mol。
| T/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的平衡常数表达式:
(2)能使该反应的反应速率增大,且平衡向正反应方向移动的是
a.及时分离出CO气体 b.适当升高温度
c.增大CO2的浓度 d.选择高效催化剂
(3) 能判断该反应是否达到化学平衡状态的依据是
a.容器中压强不变 b.混合气体中 c(CO)不变
c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为
(5)若在(4)所处的温度下,在1 L的密闭容器中,加入2 mol CO2和3 mol H2充分反应达平衡时,CO2的物质的量为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在密闭容器中的可逆反应CO(g)+NO2(g)  CO2(g)+NO(g) △H<0达到平衡后:
CO2(g)+NO(g) △H<0达到平衡后:
(1)扩大容器体积,平衡__________________ 移动(填“正向”“逆向”或“不”,下同),C(NO2)将 ______________ (填“变大”“变小”或“不变”),反应混合物的颜色 _______________ (填“变深”或“变浅”)
(2)升高温度,正反应速率__________________ (填“变大”“变小”或“不变”,下同),平衡常数K ____________________
(3)加入催化剂,NO的物质的量____________________
 CO2(g)+NO(g) △H<0达到平衡后:
CO2(g)+NO(g) △H<0达到平衡后:(1)扩大容器体积,平衡
(2)升高温度,正反应速率
(3)加入催化剂,NO的物质的量
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】合成氨是人类科技发展史上的一项重大突破,已知:25℃时,合成氨反应的热化学为:N2(g)+3H2(g) ⇌2NH3(g) ΔH=-92.4kJ/mol,请回答下列问题:
(1)其他条件不变时,升高温度,化学反应速率_____ (填“增大”或“减小”);
(2)25℃时,取1mol N2和3mol H2置于2L的密闭容器中,在催化剂存在下进行反应,达到平衡时放出的热量_____
A.大于92.4 kJ B.等于92.4 kJ C.小于92.4 kJ
(3)一定条件下,上述反应达到化学平衡状态的标志是_______ ;
A.N2、H2、NH3的浓度相等
B.容器内压强不再变化
C.单位时间内消耗amol N2,同时生成2amol NH3
(4)25℃时,上述反应平衡常数的表达式为:K=_______ 。
(1)其他条件不变时,升高温度,化学反应速率
(2)25℃时,取1mol N2和3mol H2置于2L的密闭容器中,在催化剂存在下进行反应,达到平衡时放出的热量
A.大于92.4 kJ B.等于92.4 kJ C.小于92.4 kJ
(3)一定条件下,上述反应达到化学平衡状态的标志是
A.N2、H2、NH3的浓度相等
B.容器内压强不再变化
C.单位时间内消耗amol N2,同时生成2amol NH3
(4)25℃时,上述反应平衡常数的表达式为:K=
您最近半年使用:0次



