在T℃下,分别在三个容积为10L的恒容绝热密闭容器中,发生反应:2CO(g)+SO2(g) S(g)+2CO2(g) ΔH>0,测得相关数据如下表所示。
S(g)+2CO2(g) ΔH>0,测得相关数据如下表所示。
下列说法正确的是
 S(g)+2CO2(g) ΔH>0,测得相关数据如下表所示。
S(g)+2CO2(g) ΔH>0,测得相关数据如下表所示。容器 | 起始时物质的量/mol | 平衡时CO2(g)的物质的量/mol | |||
CO(g) | SO2(g) | S(g) | CO2(g) | ||
甲 | 1 | 0.5 | 0.5 | 0 | a |
乙 | 1 | 0.5 | 0 | 0 | 0.8 |
丙 | 2 | 1 | 0 | 0 | b |
| A.其他条件不变,容器乙达到平衡后,再充入体系中四种气体各1mol,平衡逆向移动 |
| B.b=1.6 |
| C.平衡常数:K甲>K乙 |
| D.其他条件不变,向容器甲再充入1mol CO,平衡常数(K)不变 |
更新时间:2018/01/03 15:00:56
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】某温度下,将2molSO2和1molO2置于10L密闭容器中发生反应:2SO2(g)+O2(g)  2SO3(g);ΔH<0,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是
2SO3(g);ΔH<0,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是

 2SO3(g);ΔH<0,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是
2SO3(g);ΔH<0,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是
| A.由图甲推断,B点SO2的平衡浓度为0.3 mol·L-1 |
| B.由图甲推断,A点对应温度下该反应的平衡常数为800L·mol-1 |
| C.压强为0.50 MPa时不同温度下SO2转化率与温度关系如乙图,则T2>T1 |
| D.达平衡后,若增大容器容积,则反应速率变化图象可以用图丙表示 |
您最近一年使用:0次
单选题
|
较难
(0.4)
真题
【推荐2】各可逆反应达平衡后,改变反应条件,其变化趋势正确的是
A. 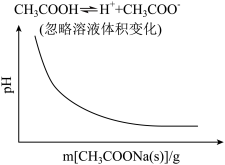 | B. 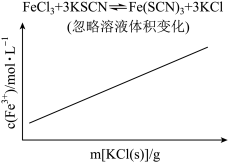 |
C.  | D.  |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】一定温度时,向2.0 L恒容密闭容器中充入2 mol SO2和1 mol O2,发生反应:2SO2(g)+O2(g) 2SO3(g)。经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
2SO3(g)。经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
| t / s | 0 | 2 | 4 | 6 | 8 |
| n(SO3) / mol | 0 | 0.8 | 1.4 | 1.8 | 1.8 |
下列说法正确的是
| A.反应在前2 s 的平均速率v(O2) = 0.4 mol·L-1·s-1 |
| B.保持其他条件不变,体积压缩到1.0 L,平衡常数将增大 |
| C.相同温度下,起始时向容器中充入4 mol SO3,达到平衡时,SO3的转化率小于10% |
D.保持温度不变,向该容器中再充入2 mol SO2、1 mol O2,反应达到新平衡时 减小 减小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】在温度相同、容积均为2L的3个恒容密闭容器中,按不同方式投入反应物发生反应A2(g)+3B2(g) 2AB3(g)保持恒温,测得反应达到平衡时的有关数据如下,下列说法正确的是
2AB3(g)保持恒温,测得反应达到平衡时的有关数据如下,下列说法正确的是
(已知A2(g)+3B2(g) 2AB3(g) ΔH=﹣92.4kJ•mol﹣1)
2AB3(g) ΔH=﹣92.4kJ•mol﹣1)
 2AB3(g)保持恒温,测得反应达到平衡时的有关数据如下,下列说法正确的是
2AB3(g)保持恒温,测得反应达到平衡时的有关数据如下,下列说法正确的是| 甲 | 乙 | 丙 | |
| 反应物投入量 | 1molA2、3mol B2 | 4mol AB3 | 2mol AB3 |
| AB3浓度(mol•L﹣1) | c1 | c2 | c3 |
| 反应的能量变化 | 放出Q1kJ | 吸收Q2kJ | 吸收Q3kJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | α1 | α2 | α3 |
 2AB3(g) ΔH=﹣92.4kJ•mol﹣1)
2AB3(g) ΔH=﹣92.4kJ•mol﹣1)| A.2p1=2p3<p2 | B.α1+α2<1 |
| C.达到平衡时丙容器中AB3的体积分数最大 | D.Q1+Q3<92.4 |
您最近一年使用:0次
【推荐3】一定温度下,在一个容积为1 L的密闭容器中,充入1 mol X(g)和1 mol Y(g),发生反应X(g)+Y(g)  2Z(g),经充分反应达到平衡后,生成的Z(g)占气体体积的50%,该温度下,在另一个容积为2 L的密闭容器中充入1 mol Z(g)发生反应Z(g)
2Z(g),经充分反应达到平衡后,生成的Z(g)占气体体积的50%,该温度下,在另一个容积为2 L的密闭容器中充入1 mol Z(g)发生反应Z(g)
 X(g)+
X(g)+ Y(g),则下列判断正确的是
Y(g),则下列判断正确的是
 2Z(g),经充分反应达到平衡后,生成的Z(g)占气体体积的50%,该温度下,在另一个容积为2 L的密闭容器中充入1 mol Z(g)发生反应Z(g)
2Z(g),经充分反应达到平衡后,生成的Z(g)占气体体积的50%,该温度下,在另一个容积为2 L的密闭容器中充入1 mol Z(g)发生反应Z(g)
 X(g)+
X(g)+ Y(g),则下列判断正确的是
Y(g),则下列判断正确的是| A.后一反应的平衡常数为1 |
| B.后一反应的平衡常数为0.5 |
| C.后一反应达到平衡时,X的平衡浓度为0.25 mol·L-1 |
| D.后一反应达到平衡时,Z的分解率为25% |
您最近一年使用:0次
【推荐1】900℃时,向2.0L恒容密闭容器中充入0.40mol乙苯,发生反应: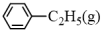

 ,经一段时间后达到平衡,反应过程中测定的部分数据如下表所示:
,经一段时间后达到平衡,反应过程中测定的部分数据如下表所示:
下列说法正确的是
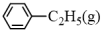

 ,经一段时间后达到平衡,反应过程中测定的部分数据如下表所示:
,经一段时间后达到平衡,反应过程中测定的部分数据如下表所示:| 时间/min | 0 | 10 | 20 | 30 | 40 |
| n(乙苯)/mol | 0.40 | 0.30 | 0.24 | n2 | n3 |
| n(苯乙烯)/mol | 0.00 | 0.10 | n1 | 0.20 | 0.20 |
| A.保持其他条件不变,向容器中充入不参与反应的水蒸气作为稀释剂,则乙苯的转化率大于50.0% |
| B.反应在前20分钟的平均速率为v(H2)=0.008mol/(L•min) |
| C.若混合气体的平均摩尔质量不再变化,则说明反应已达到平衡状态 |
| D.相同温度下,起始时向容器中充入0.10mol乙苯、0.10mol苯乙烯和0.30molH2,达到平衡前v正>v逆 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】某同学设计实验方案,利用沉淀滴定法测定“Ag++Fe2+ Fe3++Ag↓”的平衡常数K。一定温度下,先将0.0100mol·L-1Ag2SO4溶液与0.0400mol·L-1FeSO4溶液(pH=1)等体积混合,待反应达到平衡时,过滤,取vmL滤液用c1mol·L-1KSCN标准溶液滴定Ag+,至出现稳定的浅红色时消耗KSCN标准溶液v1mL。
Fe3++Ag↓”的平衡常数K。一定温度下,先将0.0100mol·L-1Ag2SO4溶液与0.0400mol·L-1FeSO4溶液(pH=1)等体积混合,待反应达到平衡时,过滤,取vmL滤液用c1mol·L-1KSCN标准溶液滴定Ag+,至出现稳定的浅红色时消耗KSCN标准溶液v1mL。
已知:Ag++SCN- AgSCN↓(白色) K1
AgSCN↓(白色) K1
Fe3++SCN- FeSCN2+(红色) K2
FeSCN2+(红色) K2
下列说法正确的是
 Fe3++Ag↓”的平衡常数K。一定温度下,先将0.0100mol·L-1Ag2SO4溶液与0.0400mol·L-1FeSO4溶液(pH=1)等体积混合,待反应达到平衡时,过滤,取vmL滤液用c1mol·L-1KSCN标准溶液滴定Ag+,至出现稳定的浅红色时消耗KSCN标准溶液v1mL。
Fe3++Ag↓”的平衡常数K。一定温度下,先将0.0100mol·L-1Ag2SO4溶液与0.0400mol·L-1FeSO4溶液(pH=1)等体积混合,待反应达到平衡时,过滤,取vmL滤液用c1mol·L-1KSCN标准溶液滴定Ag+,至出现稳定的浅红色时消耗KSCN标准溶液v1mL。已知:Ag++SCN-
 AgSCN↓(白色) K1
AgSCN↓(白色) K1Fe3++SCN-
 FeSCN2+(红色) K2
FeSCN2+(红色) K2下列说法正确的是
| A.Ag2SO4溶液和FeSO4溶液(pH=1)可替换为AgNO3溶液和Fe(NO3)2溶液(pH=1) |
| B.K1>>K2,Fe3+是滴定终点的指示剂 |
| C.若不过滤,直接用浊液做滴定实验测定c(Ag+),则所测K值偏大 |
| D.若改为测定滤液中c(Fe3+),选择合适的滴定方法直接滴定滤液,也能达到目的 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】一定条件下存在反应:CO(g)+H2O(g) CO2(g)+H2(g),其正反应放热。现有三个相同的2 L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1 mol CO和1 mol H2O,在Ⅱ中充入1 mol CO2和1 mol H2,在Ⅲ中充入2 mol CO和2 mol H2O,700 ℃条件下开始反应。达到平衡时,下列说法正确的是( )
CO2(g)+H2(g),其正反应放热。现有三个相同的2 L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1 mol CO和1 mol H2O,在Ⅱ中充入1 mol CO2和1 mol H2,在Ⅲ中充入2 mol CO和2 mol H2O,700 ℃条件下开始反应。达到平衡时,下列说法正确的是( )
 CO2(g)+H2(g),其正反应放热。现有三个相同的2 L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1 mol CO和1 mol H2O,在Ⅱ中充入1 mol CO2和1 mol H2,在Ⅲ中充入2 mol CO和2 mol H2O,700 ℃条件下开始反应。达到平衡时,下列说法正确的是( )
CO2(g)+H2(g),其正反应放热。现有三个相同的2 L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1 mol CO和1 mol H2O,在Ⅱ中充入1 mol CO2和1 mol H2,在Ⅲ中充入2 mol CO和2 mol H2O,700 ℃条件下开始反应。达到平衡时,下列说法正确的是( )| A.容器Ⅰ、Ⅱ中正反应速率相同 | B.容器Ⅰ、Ⅲ中反应的平衡常数相同 |
| C.容器Ⅰ中CO的物质的量比容器Ⅱ中的少 | D.容器Ⅰ中CO的转化率与容器Ⅱ中CO2的转化率之和小于1 |
您最近一年使用:0次




