某同学取海带灰加蒸馏水煮沸2~3 min,冷却,过滤,获得含I−的溶液,并设计以下实验方案,从中提取I2。

已知:3I2 + 6NaOH == 5NaI + NaIO3 + 3H2O
(1)试剂a的作用是________ 。
(2)试剂b应选择________ (填序号)。
A.CCl4 B.苯 C.酒精 D.植物油
(3)操作1的名称是________ 。
(4)反应3的离子方程式是________ 。

已知:3I2 + 6NaOH == 5NaI + NaIO3 + 3H2O
(1)试剂a的作用是
(2)试剂b应选择
A.CCl4 B.苯 C.酒精 D.植物油
(3)操作1的名称是
(4)反应3的离子方程式是
更新时间:2018-01-25 12:48:44
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】碘是人体不可缺乏的元素,为了防止碘缺乏,现在市场上流行一种加碘盐,就是在精盐中添加一定量的KIO3进去。某研究小组为了检测某加碘盐中是否含有碘,查阅了有关的资料,发现其检测原理是: KIO3+5KI+3H2SO4=3I2+3H2O+3K2SO4
(1)先取少量的加碘盐加蒸馏水溶解,然后加入稀硫酸和KI溶液,最后加入一定量的CCl4,振荡,这时候,观察到的现象是___________________________ ;
(2) 某学生在一次分液操作中发现溶液都是无色液体,无法知道分液漏斗中的液体哪一层是有机层,哪一层是水层,请你用简单的方法帮他鉴别出来,写出有关步骤及判断依据:_________________________ 。
(3)上面实验中用到一定物质的量浓度的稀硫酸,现用浓硫酸配制该稀硫酸,下面操作造成所配稀硫酸溶液浓度偏高的是_____________
A.溶解的时候溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.用量筒量取浓硫酸后洗涤量筒并把洗涤液转移到容量瓶
E.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
(1)先取少量的加碘盐加蒸馏水溶解,然后加入稀硫酸和KI溶液,最后加入一定量的CCl4,振荡,这时候,观察到的现象是
(2) 某学生在一次分液操作中发现溶液都是无色液体,无法知道分液漏斗中的液体哪一层是有机层,哪一层是水层,请你用简单的方法帮他鉴别出来,写出有关步骤及判断依据:
(3)上面实验中用到一定物质的量浓度的稀硫酸,现用浓硫酸配制该稀硫酸,下面操作造成所配稀硫酸溶液浓度偏高的是
A.溶解的时候溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.用量筒量取浓硫酸后洗涤量筒并把洗涤液转移到容量瓶
E.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】某化学兴趣小组通过查阅文献,设计了从某厂阳极泥(成分为Cu、Ag2Se、Au、Pt)中回收贵重金属的工艺,其流程如图所示。

回答下列问题:
(1)写出“焙烧”时,生成 的化学反应方程式
的化学反应方程式_______ 。
(2)“滤液”中的金属阳离子有_______ ;“酸浸氧化”中通入氧气的目的是_______ 、_______ 。
(3)“酸溶”时Pt、Au分别转化为 和
和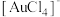 ,写出Au溶解的离子方程式
,写出Au溶解的离子方程式_______ 。
(4)可从“有机层”回收的金属是_______ 。实验室“萃取分液”的玻璃仪器有_______ 、_______ 。

回答下列问题:
(1)写出“焙烧”时,生成
 的化学反应方程式
的化学反应方程式(2)“滤液”中的金属阳离子有
(3)“酸溶”时Pt、Au分别转化为
 和
和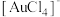 ,写出Au溶解的离子方程式
,写出Au溶解的离子方程式(4)可从“有机层”回收的金属是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】海洋是一个巨大的资源宝库。在海洋中生长的海带,富含碘元素。某同学设计以下实验方案,从海带中提取 。
。
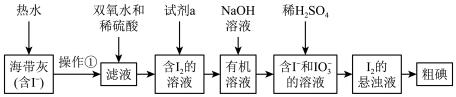
(1)灼烧海带时,需要用到的瓷质实验仪器是___________ 。
(2)如将加双氧水改为加二氧化锰也可达到实验目的,写出向滤液中加入 和稀硫酸发生反应的离子方程式:
和稀硫酸发生反应的离子方程式:___________ 。
(3)试剂a可以是___________ (填字母)。
a.乙醇 b.裂化汽油 c.四氯化碳
(4) 和
和 生成
生成 的离子方程式是
的离子方程式是___________ 。
(5)上图中,含 的溶液经3步转化为
的溶液经3步转化为 的悬浊液,其目的是
的悬浊液,其目的是___________ 。
(6)请设计一种检验提取碘后的水溶液中是否还有单质碘的简单方法:___________ 。
 。
。
(1)灼烧海带时,需要用到的瓷质实验仪器是
(2)如将加双氧水改为加二氧化锰也可达到实验目的,写出向滤液中加入
 和稀硫酸发生反应的离子方程式:
和稀硫酸发生反应的离子方程式:(3)试剂a可以是
a.乙醇 b.裂化汽油 c.四氯化碳
(4)
 和
和 生成
生成 的离子方程式是
的离子方程式是(5)上图中,含
 的溶液经3步转化为
的溶液经3步转化为 的悬浊液,其目的是
的悬浊液,其目的是(6)请设计一种检验提取碘后的水溶液中是否还有单质碘的简单方法:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】实验室设计了如下实验方案测定含有NaCl杂质的 样品含量
样品含量
(1)【方案一】:用如图装置测定生成 气体的质量已确定含量你认为该方法测定结果将比真实值
气体的质量已确定含量你认为该方法测定结果将比真实值___________ (填“偏大”或“偏小”),理由: ___________

(2)【方案二】:用加热分解的方法测定碳酸氢钠的质量分数,样品中碳酸氢钠的质量分数可表示为:_____ (注意你的表达式中所用的有关符号的含义)
 样品含量
样品含量(1)【方案一】:用如图装置测定生成
 气体的质量已确定含量你认为该方法测定结果将比真实值
气体的质量已确定含量你认为该方法测定结果将比真实值
(2)【方案二】:用加热分解的方法测定碳酸氢钠的质量分数,样品中碳酸氢钠的质量分数可表示为:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
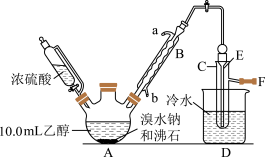
【推荐2】实验室用乙醇、浓磷酸和溴化钠反应来制备溴乙烷,其反应原理和实验的装置如下(反应需要加热,图中省去了加热装置):
H3PO4(浓)+NaBr NaH2PO4+HBr、CH3CH2OH+HBr
NaH2PO4+HBr、CH3CH2OH+HBr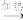 CH3CH2Br+H2O
CH3CH2Br+H2O
有关数据见下表:
(1)A中放入沸石的作用是___ 。
(2)仪器B的名称为___ ,B中进水口为___ (填“a”或“b”)口。
(3)实验中用滴液漏斗代替分液漏斗的优点为:___ 。
(4)制取氢溴酸时,为什么不能用浓H2SO4代替浓磷酸?___ (用化学方程式表示)。
(5)将C中的馏出液转入三角烧瓶中,边振荡边逐滴滴入浓H2SO4以除去水等杂质,滴加浓硫酸约1~2mL,使溶液明显分层,再用分液漏斗分去硫酸层,将经硫酸处理后的溴乙烷转入蒸馏瓶,水浴加热蒸馏,收集到35~40℃馏分约10.0g,从乙醇的角度考虑,本实验所得溴乙烷的产率是___ 。
H3PO4(浓)+NaBr
 NaH2PO4+HBr、CH3CH2OH+HBr
NaH2PO4+HBr、CH3CH2OH+HBr CH3CH2Br+H2O
CH3CH2Br+H2O
有关数据见下表:
| 乙醇 | 溴乙烷 | 溴 | |
| 状态 | 无色液体 | 无色液体 | 深红色液体 |
| 密度g/mL | 0.79 | 1.44 | 3.1 |
| 沸点/℃ | 78.5 | 38.4 | 59 |
(1)A中放入沸石的作用是
(2)仪器B的名称为
(3)实验中用滴液漏斗代替分液漏斗的优点为:
(4)制取氢溴酸时,为什么不能用浓H2SO4代替浓磷酸?
(5)将C中的馏出液转入三角烧瓶中,边振荡边逐滴滴入浓H2SO4以除去水等杂质,滴加浓硫酸约1~2mL,使溶液明显分层,再用分液漏斗分去硫酸层,将经硫酸处理后的溴乙烷转入蒸馏瓶,水浴加热蒸馏,收集到35~40℃馏分约10.0g,从乙醇的角度考虑,本实验所得溴乙烷的产率是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】氮化铝是一种新型的无机非金属材料,被广泛应用于集成电路生产领域。其 制备反应原理为Al2O3+N2+3C
制备反应原理为Al2O3+N2+3C 2AlN+3CO。制备过程中,原料配比不当或反应不完全等因素都会造成产品中含有碳或Al2O3等杂质。为测定产品中AlN的质量分数,某同学按下图装置进行相关实验。可选用的化学试剂:m g氮化铝片状固体、NaOH饱和溶液、水、煤油、医用酒精。
2AlN+3CO。制备过程中,原料配比不当或反应不完全等因素都会造成产品中含有碳或Al2O3等杂质。为测定产品中AlN的质量分数,某同学按下图装置进行相关实验。可选用的化学试剂:m g氮化铝片状固体、NaOH饱和溶液、水、煤油、医用酒精。
回答下列问题:
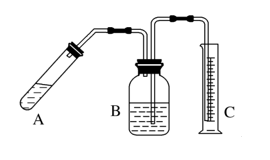
(1)简 述检查该套装置气密性的方法:
述检查该套装置气密性的方法:____________________________________ 。
(2)上图B中试剂最好选用:__________ (填序号)。
①水 ②煤油 ③医用酒精
已知A 中有NaAlO2生成,并放出有刺激性气味的气体,写出A中发生反应的化学方程式:______________________________________________________ 。
(3)读取C(量筒)中液体体积时,应注意__________ (填字母)。
a.C中液面不再上升时立即读数
b.上下移动C,使之液面与B中液面相平
c.A中不再有气泡逸出
d.视线与凹液面最低处相平
(4)m g氮化铝与足量NaOH饱和溶液反应,实验结束后,C中收集到液体的体积为V L(已折算成标准状况),则AlN样品的纯度为__________ (写计算表达式)。
(5)上述实验方案,可能因气体体积测量不准,导致误差较大。有人建议改用下列A、B两个装置中的一种(在通风橱内进行),只需进行简单而又必要的数据测量,用差量法就可比较准确确定样品中AlN的质量分数。较合理的装置是_________ (填字母)。
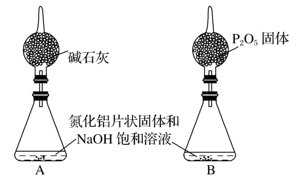
 制备反应原理为Al2O3+N2+3C
制备反应原理为Al2O3+N2+3C 2AlN+3CO。制备过程中,原料配比不当或反应不完全等因素都会造成产品中含有碳或Al2O3等杂质。为测定产品中AlN的质量分数,某同学按下图装置进行相关实验。可选用的化学试剂:m g氮化铝片状固体、NaOH饱和溶液、水、煤油、医用酒精。
2AlN+3CO。制备过程中,原料配比不当或反应不完全等因素都会造成产品中含有碳或Al2O3等杂质。为测定产品中AlN的质量分数,某同学按下图装置进行相关实验。可选用的化学试剂:m g氮化铝片状固体、NaOH饱和溶液、水、煤油、医用酒精。回答下列问题:

(1)简
 述检查该套装置气密性的方法:
述检查该套装置气密性的方法:(2)上图B中试剂最好选用:
①水 ②煤油 ③医用酒精
已知A 中有NaAlO2生成,并放出有刺激性气味的气体,写出A中发生反应的化学方程式:
(3)读取C(量筒)中液体体积时,应注意
a.C中液面不再上升时立即读数
b.上下移动C,使之液面与B中液面相平
c.A中不再有气泡逸出
d.视线与凹液面最低处相平
(4)m g氮化铝与足量NaOH饱和溶液反应,实验结束后,C中收集到液体的体积为V L(已折算成标准状况),则AlN样品的纯度为
(5)上述实验方案,可能因气体体积测量不准,导致误差较大。有人建议改用下列A、B两个装置中的一种(在通风橱内进行),只需进行简单而又必要的数据测量,用差量法就可比较准确确定样品中AlN的质量分数。较合理的装置是

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】碘元素是人体必需的微量元素之一。某小组设计以下实验从海带中提取碘并测定食盐中碘元素的含量。
Ⅰ.海带提碘
(1)同学们称取一定量干海带,将海带先剪碎,然后用水浸泡、洗净、晾干,放入__________ (填仪器名称)中灼烧至海带完全成灰烬,然后继续进行下列流程。 溶液,然后再加入0.5mL
溶液,然后再加入0.5mL ,振荡后静置,若观察到
,振荡后静置,若观察到_________ (填实验现象),则证明海带中含有碘元素,上述过程中涉及的离子反应方程式为______________ 。
(3)萃取实验中,若要使碘尽可能地完全转移到 中,可采取的操作是
中,可采取的操作是______________ 。
Ⅱ.人体碘的重要来源之一是食用加碘食盐(含 )。为测定加碘食盐中的碘含量,学习小组设计如下实验:
)。为测定加碘食盐中的碘含量,学习小组设计如下实验:
①配制1L 硫代硫酸钠(
硫代硫酸钠( )标准溶液;
)标准溶液;
②用天平准确称取wg食盐样品,加适量蒸馏水使其完全溶解;
③用稀硫酸酸化所得溶液,加入足量KI溶液,使 与KI反应完全生成
与KI反应完全生成 ;
;
④向③中混合液逐滴加入浓度为 的
的 溶液,恰好反应完全时,消耗
溶液,恰好反应完全时,消耗 溶液6.00mL。(已知:
溶液6.00mL。(已知: )
)
已知: 易溶于水,具有强还原性。
易溶于水,具有强还原性。
(4)配制硫代硫酸钠溶液时用分析天平准确称量 固体的质量为
固体的质量为______ g。(保留小数点后2位)
(5)配制前蒸馏水需先煮沸再冷却,其目的是__________ 。
(6)下列情况中,导致所配溶液的物质的量浓度偏低的是________.(填标号)。
(7)上述食盐样品中碘元素的含量为__________ mg/kg(用含w的代数式表示)。
Ⅰ.海带提碘
(1)同学们称取一定量干海带,将海带先剪碎,然后用水浸泡、洗净、晾干,放入

 溶液,然后再加入0.5mL
溶液,然后再加入0.5mL ,振荡后静置,若观察到
,振荡后静置,若观察到(3)萃取实验中,若要使碘尽可能地完全转移到
 中,可采取的操作是
中,可采取的操作是Ⅱ.人体碘的重要来源之一是食用加碘食盐(含
 )。为测定加碘食盐中的碘含量,学习小组设计如下实验:
)。为测定加碘食盐中的碘含量,学习小组设计如下实验:①配制1L
 硫代硫酸钠(
硫代硫酸钠( )标准溶液;
)标准溶液;②用天平准确称取wg食盐样品,加适量蒸馏水使其完全溶解;
③用稀硫酸酸化所得溶液,加入足量KI溶液,使
 与KI反应完全生成
与KI反应完全生成 ;
;④向③中混合液逐滴加入浓度为
 的
的 溶液,恰好反应完全时,消耗
溶液,恰好反应完全时,消耗 溶液6.00mL。(已知:
溶液6.00mL。(已知: )
)已知:
 易溶于水,具有强还原性。
易溶于水,具有强还原性。(4)配制硫代硫酸钠溶液时用分析天平准确称量
 固体的质量为
固体的质量为(5)配制前蒸馏水需先煮沸再冷却,其目的是
(6)下列情况中,导致所配溶液的物质的量浓度偏低的是________.(填标号)。
| A.容量瓶在使用前未干燥,里面有少量蒸馏水 |
| B.转移溶液至容量瓶过程中,有少量溶液溅出 |
| C.定容时俯视刻度线读数 |
| D.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线 |
(7)上述食盐样品中碘元素的含量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某学习小组按如下实验流程探究海带中碘含量的测定和碘的制取。
实验(一) 碘含量的测定
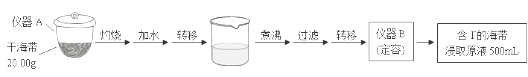
取0.0100 mol·Lˉ1的AgNO3标准溶液装入滴定管,取100.00 mL海带浸取原液至滴定池,用电势滴定法测定碘含量。测得的电动势(E) 反映溶液中c(Iˉ)的变化,部分数据如下表:
实验(二) 碘的制取
另制海带浸取原液,甲、乙两种实验方案如下:
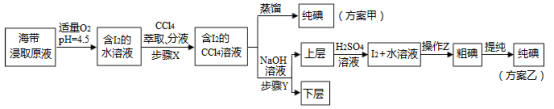
已知:3I2+6NaOH=5NaI+NaIO3+3H2O。
请回答:
(1)①实验(一) 中的仪器名称:仪器A_________ , 仪器 B_________ 。
②该次滴定终点时用去AgNO3溶液的体积为_____ mL,计算得海带中碘的百分含量为_______ %。
(2)①步骤X中,萃取后分液漏斗内观察到的现象是_______________ 。
②下列有关步骤Y的说法,正确的是___________________ 。
A.应控制NaOH溶液的浓度和体积
B.将碘转化成离子进入水层
C.主要是除去海带浸取原液中的有机杂质
D.NaOH溶液可以由乙醇代替
③实验(二) 中操作Z的名称是______________________ 。
(3)方案甲中采用蒸馏不合理,理由是_____________________ 。
实验(一) 碘含量的测定

取0.0100 mol·Lˉ1的AgNO3标准溶液装入滴定管,取100.00 mL海带浸取原液至滴定池,用电势滴定法测定碘含量。测得的电动势(E) 反映溶液中c(Iˉ)的变化,部分数据如下表:
| V(AgNO3)/mL | 15.00 | 19.00 | 19.80 | 19.98 | 20.00 | 20.02 | 21.00 | 23.00 | 25.00 |
| E/mV | -225 | -200 | -150 | -100 | 50.0 | 175 | 275 | 300 | 325 |
实验(二) 碘的制取
另制海带浸取原液,甲、乙两种实验方案如下:

已知:3I2+6NaOH=5NaI+NaIO3+3H2O。
请回答:
(1)①实验(一) 中的仪器名称:仪器A
②该次滴定终点时用去AgNO3溶液的体积为
(2)①步骤X中,萃取后分液漏斗内观察到的现象是
②下列有关步骤Y的说法,正确的是
A.应控制NaOH溶液的浓度和体积
B.将碘转化成离子进入水层
C.主要是除去海带浸取原液中的有机杂质
D.NaOH溶液可以由乙醇代替
③实验(二) 中操作Z的名称是
(3)方案甲中采用蒸馏不合理,理由是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】食品添加剂的常见类别有:着色剂、增味剂、膨松剂、凝固剂、防腐剂、营养强化剂等。
(1)碘酸钾为___________ (填食品添加剂的类别)。
(2)从海带中提取碘的主要实验过程如下图所示:

①干海带的“灼烧”需在___________ (填仪器名称)中进行。
②操作1为___________ (填操作名称)。
③在“氧化”步骤中,最符合绿色化学思想的氧化剂是下列物质中的___________ (填选项字母),酸性条件下该反应的离子方程式为___________ 。
A. 溶液 B.浓硝酸 C.
溶液 B.浓硝酸 C.
④检验操作2后水层中是否含有碘单质的方法为___________ 。
(3)在加热条件下,将 通入到
通入到 和
和 的混合溶液中制备
的混合溶液中制备 ,该反应的化学方程式为
,该反应的化学方程式为___________ ;若要制备500g的加碘食盐(碘含量为2.54%),至少需要
___________ g。
(1)碘酸钾为
(2)从海带中提取碘的主要实验过程如下图所示:

①干海带的“灼烧”需在
②操作1为
③在“氧化”步骤中,最符合绿色化学思想的氧化剂是下列物质中的
A.
 溶液 B.浓硝酸 C.
溶液 B.浓硝酸 C.
④检验操作2后水层中是否含有碘单质的方法为
(3)在加热条件下,将
 通入到
通入到 和
和 的混合溶液中制备
的混合溶液中制备 ,该反应的化学方程式为
,该反应的化学方程式为
您最近一年使用:0次



