Ⅰ、实 验室可以用KMnO4固体和浓盐酸反应制取少量Cl2,反应的化学方程式为:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O回答下列问题:
验室可以用KMnO4固体和浓盐酸反应制取少量Cl2,反应的化学方程式为:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O回答下列问题:
(1)该反应中被氧化的元素是__________ .
(2)氧化性:KMnO4__________ Cl2(填“>”、“<”或“= ”)
”)
(3)该反应中氧化 剂和氧化产物的物质的量之比为
剂和氧化产物的物质的量之比为__________ .
(4)用双线桥法表示该反应中电子转移的方向和数目:_________
2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O
(5)每生成标准状况下2.24L Cl2,反应中转移电子的物质的量为__________ .
Ⅱ、实验室常用以下方法制取氯气:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O请你根据所学知识回答下列问题:
MnCl2+Cl2↑+2H2O请你根据所学知识回答下列问题:
(1)把氯气通入紫色石蕊试液中,可以观察到的现象是:________________ ,请你解释其中的原因 __________________________________________________
(2)为保证实验安全,常用NaOH溶液吸收多余的氯气。写出反应的化学方程式__________________________________ ;
 验室可以用KMnO4固体和浓盐酸反应制取少量Cl2,反应的化学方程式为:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O回答下列问题:
验室可以用KMnO4固体和浓盐酸反应制取少量Cl2,反应的化学方程式为:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O回答下列问题:(1)该反应中被氧化的元素是
(2)氧化性:KMnO4
 ”)
”)(3)该反应中氧化
 剂和氧化产物的物质的量之比为
剂和氧化产物的物质的量之比为(4)用双线桥法表示该反应中电子转移的方向和数目:
2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O
(5)每生成标准状况下2.24L Cl2,反应中转移电子的物质的量为
Ⅱ、实验室常用以下方法制取氯气:MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O请你根据所学知识回答下列问题:
MnCl2+Cl2↑+2H2O请你根据所学知识回答下列问题:(1)把氯气通入紫色石蕊试液中,可以观察到的现象是:
(2)为保证实验安全,常用NaOH溶液吸收多余的氯气。写出反应的化学方程式
17-18高一上·山东淄博·期末 查看更多[5]
山东省桓台县2017-2018学年高一上学期期末考试化学试题山东省桓台第二中学2017-2018学年高一上学期期末考试化学试题辽宁省抚顺中学2017-2018学年高一上学期期末考试化学试题黑龙江省牡丹江中学2017-2018学年高一上学期期末考试化学试题(已下线)【艺体生百日捷进提升系列-技能方法】专题3.12 卤族方面试题的解题方法与技巧
更新时间:2018-01-25 22:48:37
|
相似题推荐
【推荐1】NaClO2是一种重要的杀菌消毒剂,其一种生产工艺如下:

(1)NaClO2中Cl的化合价为_______ ;
(2)写出“反应”步骤中生成 ClO2的化学方程式_____________ ;
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去 和Ca2+等杂质离子,需加入除杂试剂的先后顺序为
和Ca2+等杂质离子,需加入除杂试剂的先后顺序为_________ 、_________ (填化学式);
(4)已知“尾气吸收”中发生的化学反应如下: 2NaOH+H2O2+2ClO2=2NaClO2+O2+2H2O
①用双线桥表示该反应中电子转移的数目和方向________ ;
②该反应中,还原剂是_______________ ,还原产物是_________________ ;
③标准状况下,当反应中转移1 mol电子时,生成氧气的体积为______________ 。

(1)NaClO2中Cl的化合价为
(2)写出“反应”步骤中生成 ClO2的化学方程式
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去
 和Ca2+等杂质离子,需加入除杂试剂的先后顺序为
和Ca2+等杂质离子,需加入除杂试剂的先后顺序为(4)已知“尾气吸收”中发生的化学反应如下: 2NaOH+H2O2+2ClO2=2NaClO2+O2+2H2O
①用双线桥表示该反应中电子转移的数目和方向
②该反应中,还原剂是
③标准状况下,当反应中转移1 mol电子时,生成氧气的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下列三组物质中,均有一种物质的类别与其他三种不同。
① 、
、 、
、 、
、
② 、
、 、
、 、
、
③ 、
、 、
、 、
、
(1)三种物质依次是(填化学式):A_______ ;B_______ ;C_______ 。
(2)写出物质C的水溶液与足量稀硫酸反应的离子方程式:_______ 。
(3)将少量 通入
通入 溶液中,反应的离子方程式为
溶液中,反应的离子方程式为 ,则
,则 、
、 、
、 三种离子的还原性由强到弱的顺序为
三种离子的还原性由强到弱的顺序为_______ 。
(4)①用双线桥法标出下列反应的电子转移情况:_______ 。
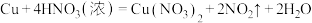
②该反应的还原剂是_______ ,还原产物是_______ 。
①
 、
、 、
、 、
、
②
 、
、 、
、 、
、
③
 、
、 、
、 、
、
(1)三种物质依次是(填化学式):A
(2)写出物质C的水溶液与足量稀硫酸反应的离子方程式:
(3)将少量
 通入
通入 溶液中,反应的离子方程式为
溶液中,反应的离子方程式为 ,则
,则 、
、 、
、 三种离子的还原性由强到弱的顺序为
三种离子的还原性由强到弱的顺序为(4)①用双线桥法标出下列反应的电子转移情况:
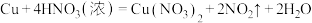
②该反应的还原剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氯化铁是一种重要的化学试剂,其晶体的化学式为FeCl3·6H2O。FeCl3的饱和溶液在实验室和电子工业中都有重要应用。
(1)饱和FeCl3溶液的颜色是______________ 色的,实验室里常用它来制备______________ (化学式)胶体,具体操作方法是:先将烧杯中的水加热至沸腾,再滴入5~6滴____________________ ,______________ 至液体呈______________ 色,停止加热。
(2)电子工业中 ,常用FeCl3的饱和溶液来印刷电路图板,反应的原理是:Cu+2FeCl3=2FeCl2+CuCl2。该反应中______________ 作氧化剂,用单线桥法表示电子转移的方向和数目:____________ 。
(3)将0.5mol·L—1的FeCl3溶液从100mL稀释至500mL,所得溶液中,c(Cl—)为__________ 。【写出计算过程】
(1)饱和FeCl3溶液的颜色是
(2)电子工业中 ,常用FeCl3的饱和溶液来印刷电路图板,反应的原理是:Cu+2FeCl3=2FeCl2+CuCl2。该反应中
(3)将0.5mol·L—1的FeCl3溶液从100mL稀释至500mL,所得溶液中,c(Cl—)为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】根据已经学过的化学知识,回答下列问题。
Ⅰ.金属及其化合物在生产生活中有着广泛的应用。
(1)胃舒平(主要成分为氢氧化铝)可用于治疗胃酸过多,氢氧化铝体现___________ 性;___________ (填“能”或“不能”)用氢氧化钠溶液代替。
(2)NaHSO4是一种酸式盐,写出NaHSO4在水中的电离方程式:___________ 。
Ⅱ.物质的量是学习化学的基础。
(3)在标准状况下8.96 L CO2的分子数为___________ 。
(4)19 g某二价金属的氯化物ACl2中含有0.4 mol Cl-,金属A的相对原子质量是___________ 。
(5)质量分数为24%、密度为1.18g/m3的NaClO溶液的物质的量浓度约为___________ mol·L-1(计算结果保留一位小数)。在用NaClO固体配制100mL  溶液过程中,下列操作中能使所配溶液的浓度偏高的有
溶液过程中,下列操作中能使所配溶液的浓度偏高的有___________ (填序号)。
①用托盘天平称量时物品和砝码放反(托盘天平的最小砝码为1g)
②烧杯中固体溶解后未冷却直接转移定容
③转移前,容量瓶中含有少量蒸馏水
④定容时,加蒸馏水超过标线,又用胶头滴管吸出
⑤定容时,俯视刻度线
(6)根据反应14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,可知当有2.5 mol FeS2参加反应时,被氧化的硫元素的物质的量为___________ mol。
Ⅰ.金属及其化合物在生产生活中有着广泛的应用。
(1)胃舒平(主要成分为氢氧化铝)可用于治疗胃酸过多,氢氧化铝体现
(2)NaHSO4是一种酸式盐,写出NaHSO4在水中的电离方程式:
Ⅱ.物质的量是学习化学的基础。
(3)在标准状况下8.96 L CO2的分子数为
(4)19 g某二价金属的氯化物ACl2中含有0.4 mol Cl-,金属A的相对原子质量是
(5)质量分数为24%、密度为1.18g/m3的NaClO溶液的物质的量浓度约为
 溶液过程中,下列操作中能使所配溶液的浓度偏高的有
溶液过程中,下列操作中能使所配溶液的浓度偏高的有①用托盘天平称量时物品和砝码放反(托盘天平的最小砝码为1g)
②烧杯中固体溶解后未冷却直接转移定容
③转移前,容量瓶中含有少量蒸馏水
④定容时,加蒸馏水超过标线,又用胶头滴管吸出
⑤定容时,俯视刻度线
(6)根据反应14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,可知当有2.5 mol FeS2参加反应时,被氧化的硫元素的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】碳族元素包括碳、硅、锗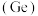 、锡
、锡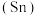 、铅等,它们的单质及化合物广泛应用于我们生活的各个领域。锗和锡曾被用于半导体材料,铅被用来制造蓄电池。碳族元素在化合物中只有铅以低价形式存在时较稳定,其他元素在化合物中都是以高价形式存在比较稳定。
、铅等,它们的单质及化合物广泛应用于我们生活的各个领域。锗和锡曾被用于半导体材料,铅被用来制造蓄电池。碳族元素在化合物中只有铅以低价形式存在时较稳定,其他元素在化合物中都是以高价形式存在比较稳定。
请回答下列问题:
(1)实验室用单质锡粉制取少量二氯化锡溶液,制取和保存的方法是 用文字叙述
用文字叙述
________ 。
(2)铅有多种氧化物,写出四氧化三铅与浓盐酸反应的离子方程式:________ 。
(3)二氧化铅在空气中加强热会得到一系列铅的其他氧化物。若把 二氧化铅加强热,当固体的质量变为
二氧化铅加强热,当固体的质量变为 时,写出反应的化学方程式:
时,写出反应的化学方程式:________ 。
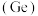 、锡
、锡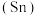 、铅等,它们的单质及化合物广泛应用于我们生活的各个领域。锗和锡曾被用于半导体材料,铅被用来制造蓄电池。碳族元素在化合物中只有铅以低价形式存在时较稳定,其他元素在化合物中都是以高价形式存在比较稳定。
、铅等,它们的单质及化合物广泛应用于我们生活的各个领域。锗和锡曾被用于半导体材料,铅被用来制造蓄电池。碳族元素在化合物中只有铅以低价形式存在时较稳定,其他元素在化合物中都是以高价形式存在比较稳定。请回答下列问题:
(1)实验室用单质锡粉制取少量二氯化锡溶液,制取和保存的方法是
 用文字叙述
用文字叙述
(2)铅有多种氧化物,写出四氧化三铅与浓盐酸反应的离子方程式:
(3)二氧化铅在空气中加强热会得到一系列铅的其他氧化物。若把
 二氧化铅加强热,当固体的质量变为
二氧化铅加强热,当固体的质量变为 时,写出反应的化学方程式:
时,写出反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氯酸钾和浓盐酸之间有下列反应:2KClO3+4HCl(浓)=2KCl+Cl2↑+2ClO2+2H2O
(1)该反应中发生还原反应的物质是___________ 。氧化产物是___________ 。
(2)用双线桥标出方程式中的电子得失。2KClO3+4HCl(浓)=2KCl+Cl2↑+2ClO2+2H2O,___________
(3)当有0.2mol电子发生转移时,生成的氯气的体积为___________ L(标准状况)。被氧化的HCl的物质的量为___________ mol。
(4)若分别用①KMnO4(还原产物是Mn2+);②MnO2(还原产物是Mn2+);③Ca(ClO)2(还原产物是Cl2)氧化浓盐酸制备氯气,当浓盐酸足量且这三种氧化剂的物质的量相同时,生成氯气的物质的量最少的是___________ (填编号)。
(5)有下列6种物质:K2SO4、K2SO3、I2、H2SO4、KIO3、H2O组成一个氧化还原反应,已知在反应中K2SO3失去电子。请回答下列问题:将这6种物质分别填入下面对应的横线上,组成一个配平 的化学方程式:___________+___________+H2SO4→___________+___________+___________(填化学式),___________
(1)该反应中发生还原反应的物质是
(2)用双线桥标出方程式中的电子得失。2KClO3+4HCl(浓)=2KCl+Cl2↑+2ClO2+2H2O,
(3)当有0.2mol电子发生转移时,生成的氯气的体积为
(4)若分别用①KMnO4(还原产物是Mn2+);②MnO2(还原产物是Mn2+);③Ca(ClO)2(还原产物是Cl2)氧化浓盐酸制备氯气,当浓盐酸足量且这三种氧化剂的物质的量相同时,生成氯气的物质的量最少的是
(5)有下列6种物质:K2SO4、K2SO3、I2、H2SO4、KIO3、H2O组成一个氧化还原反应,已知在反应中K2SO3失去电子。请回答下列问题:将这6种物质分别填入下面对应的横线上,组成一个
您最近一年使用:0次
【推荐1】对于数以千万计的化学物质和十分丰富的化学变化,分类法的作用几乎是无可替代的。某化学兴趣小组对下列三组物质进行研究:
A组:CaO、 、
、 、CuO
、CuO
B组: 、
、 、
、 、Cu
、Cu
C组: 、HCl、
、HCl、 、
、
完成下表,并根据所给物质填空。
(1)上表中应该分别填入:①_______ ,②_______ ,③_______ 。
(2)写出实验室制备 的化学反应方程式
的化学反应方程式_______ 。
(3)工业上用 与石灰乳制取漂白粉,漂白粉的有效成分的化学式是
与石灰乳制取漂白粉,漂白粉的有效成分的化学式是_______ 。84消毒液与氯气相比具有贮运方便等优点,工业上是将氯气通入到30%的NaOH溶液中来制备NaClO溶液,若NaClO溶液中NaOH的质量分数为1%,则生产100kg该溶液需消耗氯气的质量为_______ kg(保留整数)。
(4)采用“空气吹出法”可从浓海水吹出 ,并用纯碱吸收。纯碱吸收溴的主要反应是:
,并用纯碱吸收。纯碱吸收溴的主要反应是: (未配平)。该反应的氧化产物是
(未配平)。该反应的氧化产物是_______ ,吸收 时,转移的电子数为
时,转移的电子数为_______ mol。
A组:CaO、
 、
、 、CuO
、CuOB组:
 、
、 、
、 、Cu
、CuC组:
 、HCl、
、HCl、 、
、
完成下表,并根据所给物质填空。
| 组别 | A组 | B组 | C组 |
| 分类标准 | 碱性氧化物 | ② | ③ |
| 不属于该类别的物质 | ① | Cu |  |
(1)上表中应该分别填入:①
(2)写出实验室制备
 的化学反应方程式
的化学反应方程式(3)工业上用
 与石灰乳制取漂白粉,漂白粉的有效成分的化学式是
与石灰乳制取漂白粉,漂白粉的有效成分的化学式是(4)采用“空气吹出法”可从浓海水吹出
 ,并用纯碱吸收。纯碱吸收溴的主要反应是:
,并用纯碱吸收。纯碱吸收溴的主要反应是: (未配平)。该反应的氧化产物是
(未配平)。该反应的氧化产物是 时,转移的电子数为
时,转移的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】有下列物质:①氢氧化钠固体 ②铝丝 ③稀硫酸 ④饱和食盐水 ⑤氨水 ⑥石墨 ⑦酒精 ⑧熔融的KCl ⑨氢氧化铁 ⑩漂白粉
(1)漂白粉的主要成分:________________ ,写出工业上制备漂白粉的方程式:__________________
(2)以上物质中能导电的:_______________ ;属于电解质的:___________________ ;
(3)写出碳的原子结构示意图:_________________  的电离方程式:
的电离方程式:____________________
(4)写出工业上制氯气的化学方程式,并用双线桥法表示出电子的转移和方向:____________________
(5)说明氢氧化铁胶体能净水的原因___________________________
(1)漂白粉的主要成分:
(2)以上物质中能导电的:
(3)写出碳的原子结构示意图:
 的电离方程式:
的电离方程式:(4)写出工业上制氯气的化学方程式,并用双线桥法表示出电子的转移和方向:
(5)说明氢氧化铁胶体能净水的原因
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】人体吸入 会破坏某些酶的活性,使人体的代谢发生紊乱。为了减少危害,人们进行了许多探索和研究,并且在实际应用中取得了一定的成果。回答下列问题:
会破坏某些酶的活性,使人体的代谢发生紊乱。为了减少危害,人们进行了许多探索和研究,并且在实际应用中取得了一定的成果。回答下列问题:
(1) 具有氧化性,
具有氧化性, 与
与 反应会生成淡黄色沉淀,写出反应的化学方程式:
反应会生成淡黄色沉淀,写出反应的化学方程式:_______ 。
(2) 可以使品红溶液褪色,说明二氧化硫具有
可以使品红溶液褪色,说明二氧化硫具有_______ 性。
(3)石灰石——石膏法。该工艺原理利用石灰石加水制成的浆液( )作为吸收剂,吸收二氧化硫,并生成
)作为吸收剂,吸收二氧化硫,并生成 。再向其中通入烟气氧化生成
。再向其中通入烟气氧化生成 ,写出该工艺中生成
,写出该工艺中生成 的化学方程式:
的化学方程式:_______ 。
(4)近年来,有人提出了一种利用电解饱和氯化钠溶液循环治理含二氧化硫的废气并回收二氧化硫的方法。该方法的流程如下:
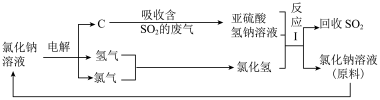
①此种方法中,可以循环利用的物质是_______ (填化学式)。
②写出电解饱和氯化钠溶液的化学方程式:_______ 。
③写出反应I的离子方程式:_______ 。
 会破坏某些酶的活性,使人体的代谢发生紊乱。为了减少危害,人们进行了许多探索和研究,并且在实际应用中取得了一定的成果。回答下列问题:
会破坏某些酶的活性,使人体的代谢发生紊乱。为了减少危害,人们进行了许多探索和研究,并且在实际应用中取得了一定的成果。回答下列问题:(1)
 具有氧化性,
具有氧化性, 与
与 反应会生成淡黄色沉淀,写出反应的化学方程式:
反应会生成淡黄色沉淀,写出反应的化学方程式:(2)
 可以使品红溶液褪色,说明二氧化硫具有
可以使品红溶液褪色,说明二氧化硫具有(3)石灰石——石膏法。该工艺原理利用石灰石加水制成的浆液(
 )作为吸收剂,吸收二氧化硫,并生成
)作为吸收剂,吸收二氧化硫,并生成 。再向其中通入烟气氧化生成
。再向其中通入烟气氧化生成 ,写出该工艺中生成
,写出该工艺中生成 的化学方程式:
的化学方程式:(4)近年来,有人提出了一种利用电解饱和氯化钠溶液循环治理含二氧化硫的废气并回收二氧化硫的方法。该方法的流程如下:

①此种方法中,可以循环利用的物质是
②写出电解饱和氯化钠溶液的化学方程式:
③写出反应I的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】电解饱和食盐水可产生氯气、氢气和氢氧化钠,氯气与石灰乳反应可制得漂白粉。
(1)请写出上述过程中发生反应的化学方程式________ 。
(2)若电解饱和食盐水时消耗NaCl 117g, 试计算理论上最多可得到氯气的体积(标准状况)________ 。
(3)若将2 mol氯气通入足量石灰乳中,理论上可得到次氯酸钙多少克________ ?
(1)请写出上述过程中发生反应的化学方程式
(2)若电解饱和食盐水时消耗NaCl 117g, 试计算理论上最多可得到氯气的体积(标准状况)
(3)若将2 mol氯气通入足量石灰乳中,理论上可得到次氯酸钙多少克
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下图表示在没有通风橱时制取纯净的氯气设计的装置图,图中A、B是可控制的弹簧铁夹。

(1)烧杯中盛放的液体是___________ ,其作用是___________ ,水槽中盛放的液体是___________ 。
(2)简述操作过程:(从氯气已经产生开始)在收集氯气之前,应___________ ;当氯气纯度合乎要求时,应___________ ;当氯气收集完毕时,应___________ 。

(1)烧杯中盛放的液体是
(2)简述操作过程:(从氯气已经产生开始)在收集氯气之前,应
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某漂粉精说明书如下:
(1)从主要成分看,可知生产漂粉精的原料是氯气和石灰乳,请写出制漂粉精的化学方程式:_______ ,漂粉精中有效成分为_______ 。
(2)生活中常有的漂白剂还有“84消毒液”,制备“84消毒液”的反应物是通过氯碱工业制得,请写出电解饱和食盐水的化学方程式:_______ ,并进一步写出制备“84消毒液”的化学方程式_______ 。
(3)为什么家庭中的漂白剂使用漂粉精,而不使用氯水?_______ 。
| 使用说明书 主要成分:次氯酸钙、氯化钙 用途用量:取漂粉精2-3克,水100克,配成溶液,将禽流感病人用具浸泡其中5-10分钟,如需要可延长时间,提高浓度。 注意事项:密封保存于阴凉处,随配随用,有腐蚀性,少与手接触。 |
(2)生活中常有的漂白剂还有“84消毒液”,制备“84消毒液”的反应物是通过氯碱工业制得,请写出电解饱和食盐水的化学方程式:
(3)为什么家庭中的漂白剂使用漂粉精,而不使用氯水?
您最近一年使用:0次



