下列情况与平衡移动无关 的是
| A.CaCO3难溶于水,但易溶于盐酸溶液 |
| B.升温能使醋酸溶液中c(H+)增大 |
| C.用KClO3制O2时常加入少量MnO2 |
| D.在NaHS溶液中加入NaOH固体能使c(S2-)增大 |
更新时间:2018-02-24 09:51:37
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列说法正确的是
| A.NaClO溶液中通入少量CO2,ClO﹣水解程度增大,溶液碱性增强 |
| B.铁片镀锌时,铁片与外电源的正极相连 |
| C.常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s)能自发进行,则ΔH<0 |
D.t℃时,恒容密闭容器中反应:NO2(g)+SO2(g) NO(g)+SO3(g),通入少量O2, NO(g)+SO3(g),通入少量O2, 的值及SO2转化率不变 的值及SO2转化率不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】氢硫酸中存在电离平衡:H2S H++HS-和HS-
H++HS-和HS- H++S2-。已知酸式盐NaHS溶液呈碱性,若向10ml浓度为0.1mol/L的氢硫酸中加入以下物质,下列判断正确的是
H++S2-。已知酸式盐NaHS溶液呈碱性,若向10ml浓度为0.1mol/L的氢硫酸中加入以下物质,下列判断正确的是
 H++HS-和HS-
H++HS-和HS- H++S2-。已知酸式盐NaHS溶液呈碱性,若向10ml浓度为0.1mol/L的氢硫酸中加入以下物质,下列判断正确的是
H++S2-。已知酸式盐NaHS溶液呈碱性,若向10ml浓度为0.1mol/L的氢硫酸中加入以下物质,下列判断正确的是| A.加水,会使平衡向右移动,溶液中氢离子浓度增大 |
| B.加入20ml浓度为0.1mol/L NaOH溶液,则c(Na+)=c(HS-)+c(H2S)+2c(S2-) |
| C.通入过量SO2气体,平衡向左移动,溶液pH值始终增大 |
| D.加入10ml浓度为0.1mol/L NaOH溶液,则c(Na+)>c(HS-)>c(OH-)>c(H+)>c(S2-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】根据下列实验操作与现象得出的结论正确的是
| 选项 | 实验操作与现象 | 结 论 |
| A | 向滴有酚酞的碳酸钠溶液中加入少量氯化钡固体, 红色变浅 | 碳酸钠溶液中存在水解平衡 |
| B | 向某溶液中逐渐通入CO2气体,先出现白色胶状沉淀,继续通入CO2气体,白色胶状沉淀不溶解 | 该溶液中一定含有[Al(OH)4]- |
| C | 将润湿的淀粉碘化钾试纸置于集满某气体的集气瓶口,试纸变蓝 | 该气体为氯气 |
| D | 向10mL 0.5mol·L-1的氯化镁溶液中滴加5mL 2.4mol·L-1氢氧化钠溶液,产生白色沉淀再滴加氯化铜溶液,沉淀变蓝 | Ksp[Cu(OH)2 ]<Ksp[Mg(OH)2 ] |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法不正确的是
| A.放热反应在常温下不一定能够自发进行 |
| B.合成氨反应需使用催化剂,目的是促进该反应平衡向生成氨的方向移动 |
| C.0.1mol·L-1Na2CO3溶液在35°C时碱性比25°C强,说明Na2CO3水解是吸热反应 |
| D.MnS悬浊液中滴加少量CuSO4溶液可生成CuS沉淀,则Ksp(CuS)<Ksp(MnS) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】根据下列实验操作和现象,所得出的结论正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 用铂丝蘸取无色溶液进行焰色反应 | 火焰呈黄色 | 该溶液定是钠盐溶液 |
| B | 向2mL浓度均为0.lmo/L的NaCl和NaI混合溶液中滴加2 滴0.1mol/L的AgNO3溶液 | 出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| C | 向氯化钡溶液中通入少量SO2,再加入稀硝酸 | 先出现白色沉淀,后白色沉淀不溶解 | 亚硫酸钡和硫酸钡都难溶于水 |
| D | 向20mL0.1mol/L的醋酸溶液中加入10mL0.1mo/L的氢氧化钠溶液,加入再滴加2滴石蕊试液 | 溶液变红 | c(CH3COOH)>c(CH3COO-) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】废旧铅蓄电池的铅膏中主要含有 、
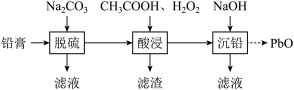
、 。为了保护环境、充分利用铅资源,通过如图流程实现铅的回收。下列说法
。为了保护环境、充分利用铅资源,通过如图流程实现铅的回收。下列说法不正确 的是(已知常温下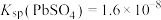 ,
,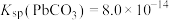 )
)
 、
、 。为了保护环境、充分利用铅资源,通过如图流程实现铅的回收。下列说法
。为了保护环境、充分利用铅资源,通过如图流程实现铅的回收。下列说法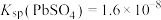 ,
,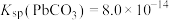 )
)
A.“铅膏”中 主要来源于该电池的正极材料 主要来源于该电池的正极材料 |
B.“脱硫”利用了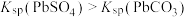 |
C.“酸浸”后溶液中的主要阳离子为 和 和 |
D.“沉铅”后的滤液中存在: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】根据实验目的,设计相关实验,下列实验操作、现象解释及结论都正确的是
| 序号 | 操作 | 现象 | 解释或结论 |
| A | 在含0.1mol的AgNO3溶液中依次加入NaCl溶液和KI溶液 | 溶液中先有白色沉淀生成,后来又变成黄色 | Ksp(AgCl)>Ksp(AgI) |
| B | 取FeSO4少许溶于水,加入几滴KSCN溶液 | 溶液变红色 | FeSO4部分氧化 |
| C | 将纯净的乙烯气体通入酸性KMnO4溶液 | 溶液紫色褪去 | 乙烯具有还原性 |
| D | 在Ca(ClO)2溶液中通入SO2气体 | 有沉淀生成 | 酸性:H2SO3>HClO |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】已知:常温下Ka1(H2SO3)=1.4×10-2,Ka2(H2SO3)=6.0×10-8,通过下列实验探究含硫化合物的性质。
实验1:测得0.1mol·L-1H2SO3溶液pH=2.1.
实验2:向10mL0.1mol·L-1NaHSO3溶液中逐滴加入5mL水,用pH计监测过程中pH变化。
实验3:用0.1mol·L-1NaOH溶液滴定10mL0.1mol·L-1H2SO3溶液。
实验4:向10mL0.1mol·L-1Na2S溶液中加入10mL0.1mol·L-1MnSO4溶液,充分混合,产生粉色沉淀,再加几滴0.1mol·L-1CuSO4溶液,产生黑色沉淀。
下列说法不正确的是
实验1:测得0.1mol·L-1H2SO3溶液pH=2.1.
实验2:向10mL0.1mol·L-1NaHSO3溶液中逐滴加入5mL水,用pH计监测过程中pH变化。
实验3:用0.1mol·L-1NaOH溶液滴定10mL0.1mol·L-1H2SO3溶液。
实验4:向10mL0.1mol·L-1Na2S溶液中加入10mL0.1mol·L-1MnSO4溶液,充分混合,产生粉色沉淀,再加几滴0.1mol·L-1CuSO4溶液,产生黑色沉淀。
下列说法不正确的是
A.由实验1可知:0.1mol·L-1H2SO3溶液中c( )>c(OH-) )>c(OH-) |
| B.实验2加水过程中,监测结果为溶液的pH不断减小 |
| C.因实验3可出现两次突跃,指示剂应选用甲基橙和酚酞 |
| D.由实验4可知:Ksp(MnS)>Ksp(CuS) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
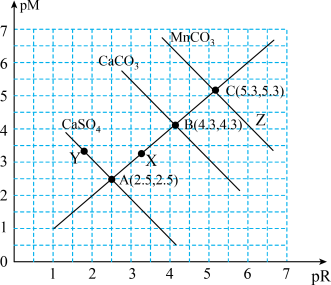
【推荐1】25℃时,难溶盐CaSO4、CaCO3、MnCO3溶液中阳离子浓度的负对数 和阴离子浓度的负对数
和阴离子浓度的负对数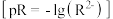 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
 和阴离子浓度的负对数
和阴离子浓度的负对数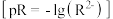 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
A.25℃,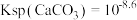 |
| B.向A点对应的溶液中加入固体CaCl2,可得到Y点对应的溶液 |
| C.25℃,三种物质的溶解度:MnCO3<CaCO3<CaSO4 |
| D.25℃,向100mLMnCO3饱和溶液中加入0.01mol CaCl2(s),有CaCO3沉淀生成 |
您最近一年使用:0次
【推荐2】下表是五种银盐的溶度积常数(25℃),下列有关说法错误的是
| 化学式 | AgCl | Ag2SO4 | Ag2S | AgBr | AgI |
| 溶度积 | 1.8×10-10 | 1.4×10-5 | 6.3×10-50 | 5.0×10-13 | 8.3×10-17 |
| A.五种物质在常温下溶解度最大的是Ag2SO4 |
| B.向AgCl的悬浊液中加入0.1mol/LNa2S溶液,则可以生成黑色的Ag2S沉淀 |
| C.外界条件改变时,沉淀溶解平衡也会发生移动 |
| D.常温下,向AgI的悬浊液中加入0.1mol/LNaCl溶液,黄色沉淀变成白色沉淀 |
您最近一年使用:0次






