图1是元素周期表的一部分,已知A、B、C、D、E、F、G都是周期表中的前四周期元素,它们在周期表中的位置如图1所示。
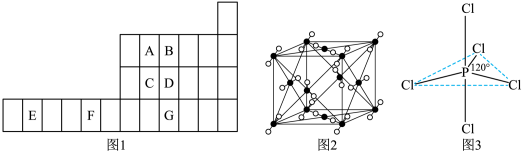
试回答下列问题:
(1)F元素基态原子的核外电子排布式为_________________ 。
(2)ABC的第一电离能由大到小的顺序______________ (用元素符号表示)。
(3)B元素单质分子中的_______ 个π键,与其互为等电子体的阴离子为____________________ 。
(4)图2为A元素某种氧化物的晶胞,其分子中心原子采用________ 杂化,每个分子周围有_____ 个分子与之距离相等且最近。若晶胞棱长为a pm,则该晶体密度的表达式为________ g·cm-3。
(5)G元素的氢化物分子的空间构型为________ ,其沸点与B元素的氢化物相比________ (填高或低),其原因是________ 。
(6)向CuSO4溶液中滴加入B 元素氢化物的水溶液,先生成蓝色沉淀,后沉淀逐渐溶解,得到深蓝色透明溶液,请写出沉淀溶解的离子方程式________ 。
(7)知道B 的电负性大于氯,则B 与F2或Cl2形成的化合物水解,产物是否相同__________ ?(填“相同”或“不同”)。

试回答下列问题:
(1)F元素基态原子的核外电子排布式为
(2)ABC的第一电离能由大到小的顺序
(3)B元素单质分子中的
(4)图2为A元素某种氧化物的晶胞,其分子中心原子采用
(5)G元素的氢化物分子的空间构型为
(6)向CuSO4溶液中滴加入B 元素氢化物的水溶液,先生成蓝色沉淀,后沉淀逐渐溶解,得到深蓝色透明溶液,请写出沉淀溶解的离子方程式
(7)知道B 的电负性大于氯,则B 与F2或Cl2形成的化合物水解,产物是否相同
更新时间:2018-03-23 15:11:16
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】铁被誉为“第一金属”,铁及其化合物在生活中有广泛应用。回答下列问题:
(1)基态Fe3+的电子排布式为___________ 。
(2)实验室用KSCN溶液、苯酚(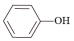 )检验Fe3+。N、O、S的第一电离能由大到小的顺序为
)检验Fe3+。N、O、S的第一电离能由大到小的顺序为___________ (用元素符号表示),苯酚中碳原子的杂化轨道类型为___________ 。
(3)FeSO4常作补铁剂,SO 的立体构型是
的立体构型是___________ 。
(4)氮化铁晶体的晶体结构示意图如图1所示。该晶体中铁、氮的微粒个数之比为___________ 。
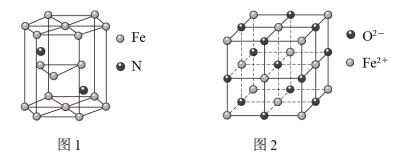
(5)氧化亚铁晶体的晶胞如图2所示。已知:氧化亚铁晶体的密度为ρg·cm-3,NA代表阿伏加德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为___________ ;Fe2+与O2-的最短间距为___________ pm。
(1)基态Fe3+的电子排布式为
(2)实验室用KSCN溶液、苯酚(
 )检验Fe3+。N、O、S的第一电离能由大到小的顺序为
)检验Fe3+。N、O、S的第一电离能由大到小的顺序为(3)FeSO4常作补铁剂,SO
 的立体构型是
的立体构型是(4)氮化铁晶体的晶体结构示意图如图1所示。该晶体中铁、氮的微粒个数之比为

(5)氧化亚铁晶体的晶胞如图2所示。已知:氧化亚铁晶体的密度为ρg·cm-3,NA代表阿伏加德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】“愚人金”的主要成分是 ,它是炼铜的主要矿物,冶炼中的反应之一为
,它是炼铜的主要矿物,冶炼中的反应之一为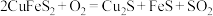 。
。
(1)基态 的核外电子排布式为
的核外电子排布式为___________ ,铜元素的焰色为绿色,产生此焰色过程中电子会___________ (填“吸收”或“释放”)出能量;上述反应涉及的几种元素中,第一电离能由大到小的顺序是___________ 。
(2) (八元环状结构)、
(八元环状结构)、 、
、 、
、 、
、 五种粒子中每个原子均达到8电子稳定结构,则中心原子杂化类型为
五种粒子中每个原子均达到8电子稳定结构,则中心原子杂化类型为 的是
的是___________ , 的立体构型为
的立体构型为___________ ,属于非极性分子的是___________ 。
(3)已知 、
、 的熔点分别为
的熔点分别为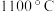 、
、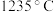 ,导致这种差异的主要原因是
,导致这种差异的主要原因是___________ ,热稳定性: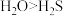 ,从结构角度上看,其原因是
,从结构角度上看,其原因是___________ 。
(4) 的晶胞如图所示,晶胞参数为
的晶胞如图所示,晶胞参数为 、
、 。
。
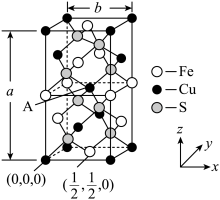
①A原子的原子坐标为___________ , 的晶体中每个Cu原子与
的晶体中每个Cu原子与___________ 个S原子相连。
②若晶体密度为 ,则阿伏加德罗常数
,则阿伏加德罗常数
___________ (用含 、
、 、
、 的式子表示)。
的式子表示)。
 ,它是炼铜的主要矿物,冶炼中的反应之一为
,它是炼铜的主要矿物,冶炼中的反应之一为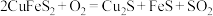 。
。(1)基态
 的核外电子排布式为
的核外电子排布式为(2)
 (八元环状结构)、
(八元环状结构)、 、
、 、
、 、
、 五种粒子中每个原子均达到8电子稳定结构,则中心原子杂化类型为
五种粒子中每个原子均达到8电子稳定结构,则中心原子杂化类型为 的是
的是 的立体构型为
的立体构型为(3)已知
 、
、 的熔点分别为
的熔点分别为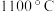 、
、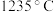 ,导致这种差异的主要原因是
,导致这种差异的主要原因是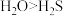 ,从结构角度上看,其原因是
,从结构角度上看,其原因是(4)
 的晶胞如图所示,晶胞参数为
的晶胞如图所示,晶胞参数为 、
、 。
。
①A原子的原子坐标为
 的晶体中每个Cu原子与
的晶体中每个Cu原子与②若晶体密度为
 ,则阿伏加德罗常数
,则阿伏加德罗常数
 、
、 、
、 的式子表示)。
的式子表示)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】我国秦俑彩绘和汉代器物上用的颜料被称为“中国蓝”“中国紫”,直到近年来人们才研究出来其成分为BaCuSi4O10,BaCuSi2O6。
(1)“中国蓝”、“中国紫”中均具有Cun+离子,n=___________ ,基态时该阳离子的价电子排布式为___________ 。
(2)合成“中国蓝”、“中国紫”的原料有BaCO3、孔雀石[Cu2(OH)2CO3]和砂子(SiO2)。现代文物分析发现,“中国蓝”中含有微量硫元素。假若硫元素来源于一种阴离子的立体构型是正四面体的天然钡矿中,则该钡矿主要成分化学式是___________ 。
(3)在5500年前,古代埃及人就已经知道如何合成蓝色颜料——“埃及蓝”CaCuSi4O10,其合成原料中用CaCO3代替了BaCO3,其他和“中国蓝”一致。CO 中键角为
中键角为___________ 。根据所学,从原料分解的角度判断“埃及蓝”的合成温度比“中国蓝”更___________ (填“高”或“低”)。
(4)硝酸铜溶于氨水形成[Cu(NH3)4](NO3)2的深蓝色溶液。
①[Cu(NH3)4](NO3)2中阴离子的立体构型是___________ 。NO 中心原子的轨道杂化类型为
中心原子的轨道杂化类型为___________ 。
②氨气在一定的压强下,测得的密度比该压强下理论密度略大,请解释原因___________ 。
(5)下图为SiO2晶胞中Si原子沿z轴方向在xy平面的投影图(即俯视图),晶胞边长为d nm,其中O原子略去,Si原子旁标注的数字表示每个Si原子位于z轴的高度,则SiA与SiB的距离是___________ 。SiO2晶体的密度为___________ g/cm3。

(1)“中国蓝”、“中国紫”中均具有Cun+离子,n=
(2)合成“中国蓝”、“中国紫”的原料有BaCO3、孔雀石[Cu2(OH)2CO3]和砂子(SiO2)。现代文物分析发现,“中国蓝”中含有微量硫元素。假若硫元素来源于一种阴离子的立体构型是正四面体的天然钡矿中,则该钡矿主要成分化学式是
(3)在5500年前,古代埃及人就已经知道如何合成蓝色颜料——“埃及蓝”CaCuSi4O10,其合成原料中用CaCO3代替了BaCO3,其他和“中国蓝”一致。CO
 中键角为
中键角为(4)硝酸铜溶于氨水形成[Cu(NH3)4](NO3)2的深蓝色溶液。
①[Cu(NH3)4](NO3)2中阴离子的立体构型是
 中心原子的轨道杂化类型为
中心原子的轨道杂化类型为②氨气在一定的压强下,测得的密度比该压强下理论密度略大,请解释原因
(5)下图为SiO2晶胞中Si原子沿z轴方向在xy平面的投影图(即俯视图),晶胞边长为d nm,其中O原子略去,Si原子旁标注的数字表示每个Si原子位于z轴的高度,则SiA与SiB的距离是

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐1】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
试回答下列问题:
(1)元素p为26号元素,请写出其基态原子外围电子排布式:____ 。
(2)c与a形成6个原子组成分子结构简式:__________ ,该分子是:_______ (填“极性”或“非极性”)分子。
(3)表中O、P两元素的部分电离能数据列于下表:
比较两元素的I2、I3可知,气态O2+再失去一个电子比气态P2+再失去一个电子难。对此,你的解释是__________________________ ;
(4)i单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
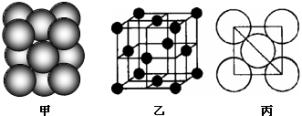
晶胞中i原子的配位数为___________ ,一个晶胞中i原子的数目为____________ 。
| a | |||||||||||||||||
| b | c | d | e | f | |||||||||||||
| g | h | i | j | k | l | m | |||||||||||
| n | o | p | |||||||||||||||
试回答下列问题:
(1)元素p为26号元素,请写出其基态原子外围电子排布式:
(2)c与a形成6个原子组成分子结构简式:
(3)表中O、P两元素的部分电离能数据列于下表:
| 元 素 | O | P | |
| 电离能kJ·mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
比较两元素的I2、I3可知,气态O2+再失去一个电子比气态P2+再失去一个电子难。对此,你的解释是
(4)i单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。

晶胞中i原子的配位数为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】在庆祝中华人民共和国成立70周年的阅兵仪式上,最后亮相的DF- 3IA洲际战略导弹是我国大国地位、国防实力的显著标志。其制作材料中包含了Fe、Cr、 Ni、 Co.、Cu等多种元素。回答下列问题:
(1)与Cr同周期且基态原子最外层电子数相同的元素,可能位于周期表中的_______ 区;
(2)实验室常用KSCN溶液、苯酚(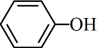 )检验Fe3+,其中C、N、O、K的第一电离能由大到小的顺序为
)检验Fe3+,其中C、N、O、K的第一电离能由大到小的顺序为_______ (用元素符号表示),KSCN和苯酚中碳原子的杂化轨道类型为_______ ;
(3)在周期表中Ir位于第六周期并和Co处于同一纵行,则基态Ir原子价电子轨道表示式为_______ 。
(4)羰基铁[Fe(CO) 5]可溶于汽油等有机物,常温下为黄色油状液体,则Fe(CO)5的晶体类型是_______ ;在lmolFe (CO) 5分子中含_______ molσ键,与CO互为等电子体的一种离子的化学式为_______ ;
(5)碳的一种同素异形体的晶体,在空隙中插入金属离子获得超导体。如图为一种超导体的面心立方晶胞,C60分子占据顶点和面心处,K+占据的是C60分子围成的_______ 空隙和_______ 空隙(填几何空间构型) ;若C60分子的坐标参数分别为A (0, 0, 0),B( ,0,
,0, ),C(1,1,1),则距离A位置最近的阳离子的坐标参数为
),C(1,1,1),则距离A位置最近的阳离子的坐标参数为 _______ ;
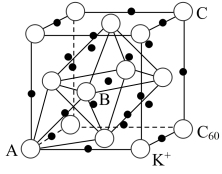
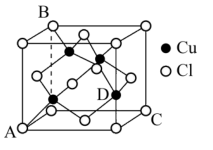
(6)CuCl的晶胞结构如图所示,该结构在实验室可经_______ 方法测得:晶胞中C、D两原子核间距为anm,阿伏加德罗常数的值为NA,CuCl 的相对分子质量为M,则该晶体密度为_______ g·cm-3(列出计算式即可)。
(1)与Cr同周期且基态原子最外层电子数相同的元素,可能位于周期表中的
(2)实验室常用KSCN溶液、苯酚(
 )检验Fe3+,其中C、N、O、K的第一电离能由大到小的顺序为
)检验Fe3+,其中C、N、O、K的第一电离能由大到小的顺序为(3)在周期表中Ir位于第六周期并和Co处于同一纵行,则基态Ir原子价电子轨道表示式为
(4)羰基铁[Fe(CO) 5]可溶于汽油等有机物,常温下为黄色油状液体,则Fe(CO)5的晶体类型是
(5)碳的一种同素异形体的晶体,在空隙中插入金属离子获得超导体。如图为一种超导体的面心立方晶胞,C60分子占据顶点和面心处,K+占据的是C60分子围成的
 ,0,
,0, ),C(1,1,1),则距离A位置最近的阳离子的坐标参数为
),C(1,1,1),则距离A位置最近的阳离子的坐标参数为 
(6)CuCl的晶胞结构如图所示,该结构在实验室可经

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】我国具有悠久的历史,在西汉就有湿法炼铜(Fe+CuSO4=Cu+FeSO4),试回答下列问题。
(1)Cu2+的未成对电子数有______ 个,H、O、S 电负性由大到小的顺序为_______ 。
(2)在硫酸铜溶液中滴加过量氨水可形成[Cu(NH3)4]SO4蓝色溶液。[Cu(NH3)4]SO4中化学键类型有_______ ,阴离子中心原子杂化类型为______ 。
(3)铁铜合金晶体类型为_____ ;铁的第三(I3)和第四(I4)电离能分别为2957kJ/mol、5290kJ/mol,比较数据并分析原因________________ 。
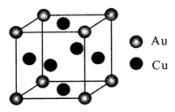
(4)金铜合金的一种晶体结构为立方晶型,如图所示。已知该合金的密度为d g/cm3,阿伏伽德罗常数值为NA,两个金原子间最小间隙为a pm(1pm= 10-10cm)。则铜原子的半径为_______ cm(写出计算表达式)。
(1)Cu2+的未成对电子数有
(2)在硫酸铜溶液中滴加过量氨水可形成[Cu(NH3)4]SO4蓝色溶液。[Cu(NH3)4]SO4中化学键类型有
(3)铁铜合金晶体类型为
(4)金铜合金的一种晶体结构为立方晶型,如图所示。已知该合金的密度为d g/cm3,阿伏伽德罗常数值为NA,两个金原子间最小间隙为a pm(1pm= 10-10cm)。则铜原子的半径为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】SiC纤维单向增强的TixAly基复合材料可作为高超音速飞行器表面的放热材料。回答下列问题:
(1)C元素所在周期中,第一电离能最大的元素是__ (填元素符号),电负性最大的是__ (填元素符号)。
(2)基态Ti原子的价电子排布式为__ ,能量最高的能级有__ 个空轨道。
(3)甲基硅油结构如图所示,其中Si原子的杂化方式为__ 。以甲基硅油为主要成分的硅橡胶能够耐高温的原因是__ 。

(4)Li2CO3、Li2TiO3是锂离子电池中的常用材料,其中CO32-的空间构型为__ ,其含有的共价键类型有__ 。
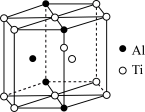
(5)TixAly合金的一种结构单元如图所示(Al、Ti原子各有一个原子在结构单元内部),该合金的化学式为__ 。其结构单元棱长为apm,底面边长为bpm,该合金的密度为___ g·cm-3。
(1)C元素所在周期中,第一电离能最大的元素是
(2)基态Ti原子的价电子排布式为
(3)甲基硅油结构如图所示,其中Si原子的杂化方式为

(4)Li2CO3、Li2TiO3是锂离子电池中的常用材料,其中CO32-的空间构型为
(5)TixAly合金的一种结构单元如图所示(Al、Ti原子各有一个原子在结构单元内部),该合金的化学式为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
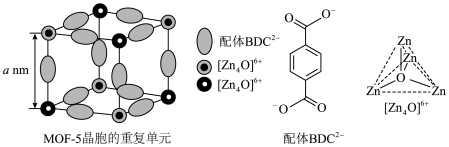
【推荐2】金属有机框架(MOFs)是一类由金属离子与有机配体通过配位键自组装形成的多孔晶体材料。MOF-5是其中最具代表性的材料之一、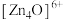 (如图)和有机配体
(如图)和有机配体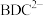 (如图)构成,其中与同一配体相连的两个
(如图)构成,其中与同一配体相连的两个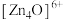 的取向不同。
的取向不同。
①Zn元素在周期表中的位置是第四周期第___________ 族。
②基态O原子的电子排布式为___________ 。
③比较C和O的电负性大小,并从原子结构角度说明理由:___________ 。
(2)MOF-5晶体内部的空腔可以吸附小分子。若要增强MOF-5与 之间的吸附作用,可在配体上引入
之间的吸附作用,可在配体上引入___________ 。(假设MOF-5晶胞形状不变)
A. B.
B. C.
C.
(3)MOF-5晶体属于立方晶系,其晶胞由8个结构相似的重复单元(如图)构成。
①每个重复单元中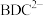 的个数为
的个数为___________ 。
②已知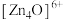 与
与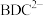 的摩尔质量分别为
的摩尔质量分别为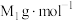 和
和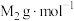 ,阿伏加德罗常数为
,阿伏加德罗常数为 。MOF-5晶体的密度为
。MOF-5晶体的密度为___________  。(
。( )
)
(4)除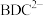 外,下列也可以作为有机配体用于构成金属有机框架的是
外,下列也可以作为有机配体用于构成金属有机框架的是___________ 。
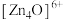 (如图)和有机配体
(如图)和有机配体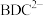 (如图)构成,其中与同一配体相连的两个
(如图)构成,其中与同一配体相连的两个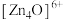 的取向不同。
的取向不同。①Zn元素在周期表中的位置是第四周期第
②基态O原子的电子排布式为
③比较C和O的电负性大小,并从原子结构角度说明理由:
(2)MOF-5晶体内部的空腔可以吸附小分子。若要增强MOF-5与
 之间的吸附作用,可在配体上引入
之间的吸附作用,可在配体上引入A.
 B.
B. C.
C.
(3)MOF-5晶体属于立方晶系,其晶胞由8个结构相似的重复单元(如图)构成。
①每个重复单元中
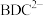 的个数为
的个数为②已知
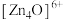 与
与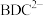 的摩尔质量分别为
的摩尔质量分别为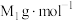 和
和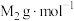 ,阿伏加德罗常数为
,阿伏加德罗常数为 。MOF-5晶体的密度为
。MOF-5晶体的密度为 。(
。( )
)(4)除
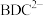 外,下列也可以作为有机配体用于构成金属有机框架的是
外,下列也可以作为有机配体用于构成金属有机框架的是A. 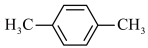 B.
B.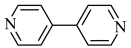 C.
C.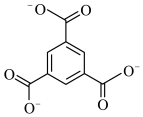
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐3】Fe、Co、Ni、Cu均为第四周期元素,它们的化合物在生产、生活中有着广泛的应用。
(1)基态Fe原子的核外电子中,两种自旋状态的电子数之比为___________ 。在空气中FeO稳定性小于 ,从电子排布的角度分析,其主要原因是
,从电子排布的角度分析,其主要原因是___________ 。
(2) 可形成
可形成 ,其中en代表
,其中en代表 。该化合物分子中,VSEPR模型为四面体的非金属原子共有
。该化合物分子中,VSEPR模型为四面体的非金属原子共有___________ 个;C、N、B的电负性由小到大的顺序为___________ 。
(3)基态 的核外电子排布式为
的核外电子排布式为___________ ; 常温下为无色液体,写出两种与CO互为等电子体离子的化学式
常温下为无色液体,写出两种与CO互为等电子体离子的化学式___________ 、___________ 。
(4)一种由Cu、In、Te组成的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,晶体中Te原子填充在Cu、In围成的四面体空隙中,则四面体空隙的占有率为___________ ;该晶体的化学式为___________ 。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点、B点原子的分数坐标分别为 、
、 ,则c点原子的分数坐标为
,则c点原子的分数坐标为___________ ;晶胞中C、D间距离d=___________ pm。
(1)基态Fe原子的核外电子中,两种自旋状态的电子数之比为
 ,从电子排布的角度分析,其主要原因是
,从电子排布的角度分析,其主要原因是(2)
 可形成
可形成 ,其中en代表
,其中en代表 。该化合物分子中,VSEPR模型为四面体的非金属原子共有
。该化合物分子中,VSEPR模型为四面体的非金属原子共有(3)基态
 的核外电子排布式为
的核外电子排布式为 常温下为无色液体,写出两种与CO互为等电子体离子的化学式
常温下为无色液体,写出两种与CO互为等电子体离子的化学式(4)一种由Cu、In、Te组成的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,晶体中Te原子填充在Cu、In围成的四面体空隙中,则四面体空隙的占有率为
 、
、 ,则c点原子的分数坐标为
,则c点原子的分数坐标为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐1】根据科技日报网报道南开大学科研团队借助镍和苯基硼酸共催化剂,首次实现丙烯醇高效、绿色合成。丙烯醇及其化合物可合成甘油、医药、农药、香料等,合成维生素E及天然抗癌药物紫杉醇中都含有关键的丙烯醇结构。丙烯醇的结构简式为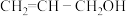 。请回答下列问题:
。请回答下列问题:
(1) 与
与 处于同一周期,且核外最外层电子构型相同,请写出基态钙原子的电子排布式:
处于同一周期,且核外最外层电子构型相同,请写出基态钙原子的电子排布式:_______ ;金属镍能与 形成配合物
形成配合物 ,写出与
,写出与 互为等电子体的一种分子或一种离子的化学式:
互为等电子体的一种分子或一种离子的化学式:_______ 。
(2)
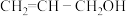 中
中 键和
键和 键的个数比为
键的个数比为_______ ,丙烯醇分子中碳原子的杂化类型为_______ 。
(3)丙醛(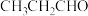 )的沸点为49℃,丙烯醇(
)的沸点为49℃,丙烯醇( )的沸点为91℃,二者相对分子质量相等,沸点相差较大的主要原因是
)的沸点为91℃,二者相对分子质量相等,沸点相差较大的主要原因是_______ 。
(4)羧基镍[ ]用于制备高纯度镍粉,它的熔点为
]用于制备高纯度镍粉,它的熔点为 ℃,沸点为43℃。羧基镍的晶体类型是
℃,沸点为43℃。羧基镍的晶体类型是_______ 。
(5) 与
与 处于同一周期,且核外最外层电子构型相同,但金属
处于同一周期,且核外最外层电子构型相同,但金属 的熔点和沸点都比金属
的熔点和沸点都比金属 高,原因为
高,原因为_______ 。区分晶体 和非晶体
和非晶体 的最可靠的科学方法为
的最可靠的科学方法为_______ 。
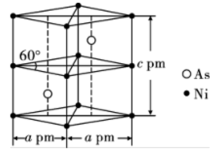
(6)某砷镍合金的晶胞如图所示,设阿伏加德罗常数的值为 ,该晶体的密度
,该晶体的密度
_______  。
。
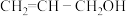 。请回答下列问题:
。请回答下列问题:(1)
 与
与 处于同一周期,且核外最外层电子构型相同,请写出基态钙原子的电子排布式:
处于同一周期,且核外最外层电子构型相同,请写出基态钙原子的电子排布式: 形成配合物
形成配合物 ,写出与
,写出与 互为等电子体的一种分子或一种离子的化学式:
互为等电子体的一种分子或一种离子的化学式:(2)

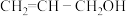 中
中 键和
键和 键的个数比为
键的个数比为(3)丙醛(
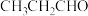 )的沸点为49℃,丙烯醇(
)的沸点为49℃,丙烯醇( )的沸点为91℃,二者相对分子质量相等,沸点相差较大的主要原因是
)的沸点为91℃,二者相对分子质量相等,沸点相差较大的主要原因是(4)羧基镍[
 ]用于制备高纯度镍粉,它的熔点为
]用于制备高纯度镍粉,它的熔点为 ℃,沸点为43℃。羧基镍的晶体类型是
℃,沸点为43℃。羧基镍的晶体类型是(5)
 与
与 处于同一周期,且核外最外层电子构型相同,但金属
处于同一周期,且核外最外层电子构型相同,但金属 的熔点和沸点都比金属
的熔点和沸点都比金属 高,原因为
高,原因为 和非晶体
和非晶体 的最可靠的科学方法为
的最可靠的科学方法为(6)某砷镍合金的晶胞如图所示,设阿伏加德罗常数的值为
 ,该晶体的密度
,该晶体的密度
 。
。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】镍、铬、铜及其化合物在工业上有广泛的应用,从电镀污泥[含有 、
、 、
、 、
、 和
和 等]中回收制备
等]中回收制备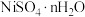 和其它金属及其化合物的工艺流程如图所示。
和其它金属及其化合物的工艺流程如图所示。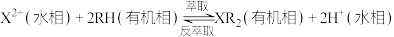 。
。
回答下列问题:
(1)与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有___________ (填元素符号)。
(2)已知NiO与MgO的晶体结构相同,其中 和
和 的离子半径分别为66pm和69pm。则熔点:NiO
的离子半径分别为66pm和69pm。则熔点:NiO___________ MgO(填“>”“<”或“=”),理由是___________ 。
(3)滤渣1的主要成分为___________ (填化学式)。
(4)电解之后加入碳酸钠调节pH的目的是___________ 。
(5)反萃取剂A为___________ 。
(6)“反萃取”得到的 溶液,在碱性条件下可被NaClO氧化生成NiOOH沉淀,该反应的离子方程式为
溶液,在碱性条件下可被NaClO氧化生成NiOOH沉淀,该反应的离子方程式为___________ 。
(7)资料显示,硫酸镍结晶水合物的形态与温度有如表关系:
由 溶液获得
溶液获得 晶体的操作依次是蒸发浓缩、
晶体的操作依次是蒸发浓缩、___________ 、过滤、洗涤、干燥。
(8)铁能形成多种氧化物,其中一种氧化物的晶胞结构如图所示:___________ ,该氧化物的化学式为___________ 。
②设 表示阿伏加德罗常数的值,若该晶胞的参数为anm,则该晶体的密度为
表示阿伏加德罗常数的值,若该晶胞的参数为anm,则该晶体的密度为___________  (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
 、
、 、
、 、
、 和
和 等]中回收制备
等]中回收制备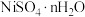 和其它金属及其化合物的工艺流程如图所示。
和其它金属及其化合物的工艺流程如图所示。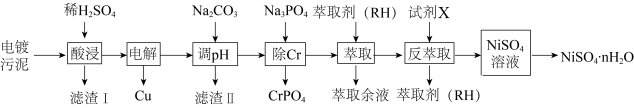
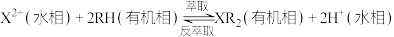 。
。回答下列问题:
(1)与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有
(2)已知NiO与MgO的晶体结构相同,其中
 和
和 的离子半径分别为66pm和69pm。则熔点:NiO
的离子半径分别为66pm和69pm。则熔点:NiO(3)滤渣1的主要成分为
(4)电解之后加入碳酸钠调节pH的目的是
(5)反萃取剂A为
(6)“反萃取”得到的
 溶液,在碱性条件下可被NaClO氧化生成NiOOH沉淀,该反应的离子方程式为
溶液,在碱性条件下可被NaClO氧化生成NiOOH沉淀,该反应的离子方程式为(7)资料显示,硫酸镍结晶水合物的形态与温度有如表关系:
| 温度 | 低于30.8℃ | 30.8℃~53.8℃ | 53.8℃~280℃ | 高于280℃ |
| 晶体形态 |  |  | 多种结晶水合物 |  |
 溶液获得
溶液获得 晶体的操作依次是蒸发浓缩、
晶体的操作依次是蒸发浓缩、(8)铁能形成多种氧化物,其中一种氧化物的晶胞结构如图所示:

②设
 表示阿伏加德罗常数的值,若该晶胞的参数为anm,则该晶体的密度为
表示阿伏加德罗常数的值,若该晶胞的参数为anm,则该晶体的密度为 (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】硫代硫酸盐是一类具有应用前景的浸金试剂。硫代硫酸根(S2O )可看作是SO
)可看作是SO 中的一个O原子被S原子取代的产物。
中的一个O原子被S原子取代的产物。
(1)基态S原子价层电子轨道表示式是______ 。
(2)比较S原子和O原子的第一电离能大小,I1(S)______ I1(O)(填“>”、或“<”)。
(3)S2O 的空间结构是
的空间结构是______ 。
(4)同位素示踪实验可证实S2O 中两个S原子的化学环境不同,实验过程为SO
中两个S原子的化学环境不同,实验过程为SO
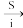 S2O
S2O
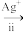 Ag2S+SO
Ag2S+SO ,过程ii中,断裂的只有硫硫键,若过程i所用试剂是Na
,过程ii中,断裂的只有硫硫键,若过程i所用试剂是Na SO3和35S,过程ii含硫产物是
SO3和35S,过程ii含硫产物是______ 。
(5)MgS2O3•6H2O的晶胞形状为长方体,边长分别为anm、bnm。cnm结构如图所示。晶胞中的[Mg(H2O)6]2+个数为______ ;已知MgS2O3•6H2O的摩尔质量是Mg•mol-1,阿伏加德罗常数为NA,该晶体的密度为______ g•cm-3。(1nm=10-7cm)

(6)浸金时,S2O 作为配体可提供孤电子对与Au+形成[Au(S2O3)2]3-。分别判断S2O
作为配体可提供孤电子对与Au+形成[Au(S2O3)2]3-。分别判断S2O 中的中心S原子和端基S原子能否做配位原子并说明理由:
中的中心S原子和端基S原子能否做配位原子并说明理由:______ 。
 )可看作是SO
)可看作是SO 中的一个O原子被S原子取代的产物。
中的一个O原子被S原子取代的产物。(1)基态S原子价层电子轨道表示式是
(2)比较S原子和O原子的第一电离能大小,I1(S)
(3)S2O
 的空间结构是
的空间结构是(4)同位素示踪实验可证实S2O
 中两个S原子的化学环境不同,实验过程为SO
中两个S原子的化学环境不同,实验过程为SO
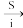 S2O
S2O
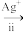 Ag2S+SO
Ag2S+SO ,过程ii中,断裂的只有硫硫键,若过程i所用试剂是Na
,过程ii中,断裂的只有硫硫键,若过程i所用试剂是Na SO3和35S,过程ii含硫产物是
SO3和35S,过程ii含硫产物是(5)MgS2O3•6H2O的晶胞形状为长方体,边长分别为anm、bnm。cnm结构如图所示。晶胞中的[Mg(H2O)6]2+个数为

(6)浸金时,S2O
 作为配体可提供孤电子对与Au+形成[Au(S2O3)2]3-。分别判断S2O
作为配体可提供孤电子对与Au+形成[Au(S2O3)2]3-。分别判断S2O 中的中心S原子和端基S原子能否做配位原子并说明理由:
中的中心S原子和端基S原子能否做配位原子并说明理由:
您最近一年使用:0次



