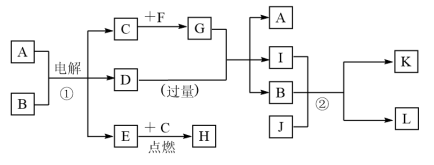
A~L是由6种短周期元素且成的物质,各物质之间有如下转化关系:
已知:
(a)C、E是气体单质,E是一种理想的清洁能源,F是日常生活中的常用金属;
(b)J是能使澄清石灰水变浑浊的无色无味气体;
(c)化合物A、D、I、L的焰色反应显黄色;
(d)白色沉淀K既溶于H溶液,又能溶于D溶液;
(e)反应①是工业上生产D和C的重要方法
请回答下列问题:
(1)写出F的化学式:______ ,D的电子式:______
(2)写出下列有关反应的离子方程:
反应①:______ ;
过量J与I反应:______
(3)G溶液呈______ 性(填“酸”、“碱”或“中”),请用离子方程式表示其原因: ______

已知:
(a)C、E是气体单质,E是一种理想的清洁能源,F是日常生活中的常用金属;
(b)J是能使澄清石灰水变浑浊的无色无味气体;
(c)化合物A、D、I、L的焰色反应显黄色;
(d)白色沉淀K既溶于H溶液,又能溶于D溶液;
(e)反应①是工业上生产D和C的重要方法
请回答下列问题:
(1)写出F的化学式:
(2)写出下列有关反应的离子方程:
反应①:
过量J与I反应:
(3)G溶液呈
2011·江西抚州·一模 查看更多[1]
(已下线)2011届江西省临川二中高三下学期第一次模拟考试(理综)化学部分
更新时间:2016-12-09 01:50:40
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题
(1)已知钴属于铁系元素,其单质与化合物的性质与铁相似,其常见化合价有+2和+3,则Co3O4与浓盐酸反应能生成黄绿色气体的离子方程式_______ 。
(2)碳酸亚铁(FeCO3)是菱镁矿的主要成分,将FeCO3加热到200℃开始分解为FeO和CO2,若在空气中高温煅烧FeCO3生成Fe2O3。
已知25℃,101kPa时: 4Fe(s)+3O2(g)=2Fe2O3(s) ∆H=−1648kJ/mol
C(s)+O2(g)=CO2(g) ∆H =−393kJ/mol
2FeCO3(s)=2Fe(s)+2C(s)+3O2(g) ∆H =+1480kJ/mol
写出FeCO3在空气中煅烧生成Fe2O3的热化学方程式_______ 。
(3)将标准状况下1.344L Cl2通入100mL0.5mol/lFeI2溶液中的离子方程式为_______ 。
(4)1mol·L-1的NaAlO2溶液和3.0mol·L-1的HCl溶液等体积混合的离子方程式为_______
(5)用于驱动潜艇的液氨-液氧燃料电池示意图如图所示:

则电极1的电极反应式为:_______ 。
(1)已知钴属于铁系元素,其单质与化合物的性质与铁相似,其常见化合价有+2和+3,则Co3O4与浓盐酸反应能生成黄绿色气体的离子方程式
(2)碳酸亚铁(FeCO3)是菱镁矿的主要成分,将FeCO3加热到200℃开始分解为FeO和CO2,若在空气中高温煅烧FeCO3生成Fe2O3。
已知25℃,101kPa时: 4Fe(s)+3O2(g)=2Fe2O3(s) ∆H=−1648kJ/mol
C(s)+O2(g)=CO2(g) ∆H =−393kJ/mol
2FeCO3(s)=2Fe(s)+2C(s)+3O2(g) ∆H =+1480kJ/mol
写出FeCO3在空气中煅烧生成Fe2O3的热化学方程式
(3)将标准状况下1.344L Cl2通入100mL0.5mol/lFeI2溶液中的离子方程式为
(4)1mol·L-1的NaAlO2溶液和3.0mol·L-1的HCl溶液等体积混合的离子方程式为
(5)用于驱动潜艇的液氨-液氧燃料电池示意图如图所示:

则电极1的电极反应式为:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某实验小组欲探究 和
和 的性质,发现实验室里盛放两种固体的试剂瓶丢失了标签。于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究。
的性质,发现实验室里盛放两种固体的试剂瓶丢失了标签。于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究。
(1)分别加热固体A、B,发现固体A受热产生的气体能使澄清石灰水变浑浊。A受热分解的化学方程式为_______ 。
(2)称取两种固体各2 g,分别加入两个小烧杯中,再各加10 mL蒸馏水,振荡,测量温度变化;待固体充分溶解,恢复至室温,向所得溶液中各滴入2滴酚酞溶液。
①发现 固体完全溶解,而
固体完全溶解,而 固体有剩余,由此得出结论
固体有剩余,由此得出结论_______ 。
②同学们在两烧杯中还观察到以下现象。其中,盛放 的烧杯中出现的现象是
的烧杯中出现的现象是_______ (填字母序号)。
a.溶液温度升高 b.溶液温度下降
c.滴入酚酞后呈浅红色 d.滴入酚酞后呈红色
(3)同学们将两种固体分别配制成 的溶液,设计如下方案并对反应现象做出预测:
的溶液,设计如下方案并对反应现象做出预测:
实施实验后,发现操作2的现象与预测有差异:产生白色沉淀和气体。则该条件下, 溶液与
溶液与 溶液反应的离子方程式为
溶液反应的离子方程式为_______ 。
 和
和 的性质,发现实验室里盛放两种固体的试剂瓶丢失了标签。于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究。
的性质,发现实验室里盛放两种固体的试剂瓶丢失了标签。于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究。(1)分别加热固体A、B,发现固体A受热产生的气体能使澄清石灰水变浑浊。A受热分解的化学方程式为
(2)称取两种固体各2 g,分别加入两个小烧杯中,再各加10 mL蒸馏水,振荡,测量温度变化;待固体充分溶解,恢复至室温,向所得溶液中各滴入2滴酚酞溶液。
①发现
 固体完全溶解,而
固体完全溶解,而 固体有剩余,由此得出结论
固体有剩余,由此得出结论②同学们在两烧杯中还观察到以下现象。其中,盛放
 的烧杯中出现的现象是
的烧杯中出现的现象是a.溶液温度升高 b.溶液温度下降
c.滴入酚酞后呈浅红色 d.滴入酚酞后呈红色
(3)同学们将两种固体分别配制成
 的溶液,设计如下方案并对反应现象做出预测:
的溶液,设计如下方案并对反应现象做出预测:| 实验方案 | 预测依据 | |
操作1:向2 mL 溶液中滴加1 mL 溶液中滴加1 mL  溶液 溶液 | 有白色沉淀 |  溶液中的 溶液中的 浓度较大,能与 浓度较大,能与 发生反应 发生反应 |
操作2:向2 mL 溶液中滴加1 mL 溶液中滴加1 mL  溶液 溶液 | 无白色沉淀 |  溶液中的 溶液中的 浓度很小,不能与 浓度很小,不能与 反应。 反应。 |
 溶液与
溶液与 溶液反应的离子方程式为
溶液反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】某中学化学兴趣小组为了调查当地某一湖泊的水质污染情况,在注入湖泊的3个主要水源的入口处采集水样,并进行了分析,给出了如下实验信息:其中一处水源含有A、B两种物质,一处含有C、D两种物质,一处含有E物质,A、B、C、D、E为五种强电解质,均由下表中的离子形成,其中C中有两种阳离子:
为了鉴别上述化合物。分别完成以下实验,其结果是:
①将它们溶于水后,C为黄色溶液,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现红褐色沉淀,继续滴加并微热,放出刺激性气味气体;
③进行焰色反应,只有B为紫色(透过蓝色钴玻璃观察);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中都能产生白色沉淀;
⑤分别将B和D溶液、A和足量E溶液混合并微热,均未见沉淀或气体生成。
根据上述实验填空:
(1)写出A、B、C的化学式:A___ ,B___ ,C___ 。
(2)将含1molA的溶液与含lmolE的溶液反应后蒸干,仅得到一种化合物,该化合物的化学式为____ 。
(3)在A溶液中加入足量澄清石灰水,其离子方程式为___ 。
| 阳离子 | K+Na+Cu2+Fe3+NH4+ |
| 阴离子 | SO42-HCO3-NO3-OH- |
①将它们溶于水后,C为黄色溶液,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现红褐色沉淀,继续滴加并微热,放出刺激性气味气体;
③进行焰色反应,只有B为紫色(透过蓝色钴玻璃观察);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中都能产生白色沉淀;
⑤分别将B和D溶液、A和足量E溶液混合并微热,均未见沉淀或气体生成。
根据上述实验填空:
(1)写出A、B、C的化学式:A
(2)将含1molA的溶液与含lmolE的溶液反应后蒸干,仅得到一种化合物,该化合物的化学式为
(3)在A溶液中加入足量澄清石灰水,其离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】为探究某不溶性固体X(仅含四种元素)的成分,设计并完成了如下实验:
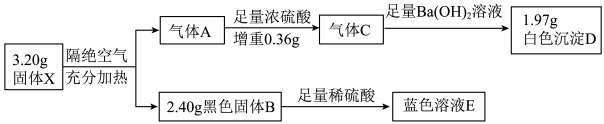
已知气体A是混合物,气体C是纯净物且无色无味.请回答:
(1)盐X中的4种元素是H、O和__________ (填元素符号),黑色固体B的化学式为__________ .
(2)气体C的结构式为__________ .
(3)该流程中X隔绝空气加热分解的化学方程式为__________ .
(4)向蓝色溶液E中加入 溶液,有白色沉淀生成,溶液的颜色则由蓝色变为深黄色,经分析白色沉淀是
溶液,有白色沉淀生成,溶液的颜色则由蓝色变为深黄色,经分析白色沉淀是 ,写出该反应的离子方程式
,写出该反应的离子方程式__________ .

已知气体A是混合物,气体C是纯净物且无色无味.请回答:
(1)盐X中的4种元素是H、O和
(2)气体C的结构式为
(3)该流程中X隔绝空气加热分解的化学方程式为
(4)向蓝色溶液E中加入
 溶液,有白色沉淀生成,溶液的颜色则由蓝色变为深黄色,经分析白色沉淀是
溶液,有白色沉淀生成,溶液的颜色则由蓝色变为深黄色,经分析白色沉淀是 ,写出该反应的离子方程式
,写出该反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】据下图的转化关系及现象回答下列问题:_______ 。
(2)A的化学式为_______ 。
(3)流程图中的金属单质与水反应的化学方程式为_______ 。
(4)反应①的化学方程式并用双线桥法表示电子转移的方向和数目为_______ 。
(5)若澄清石灰水过量,反应②的离子方程式为_______ 。
(6)反应③的化学方程式为_______ 。

(2)A的化学式为
(3)流程图中的金属单质与水反应的化学方程式为
(4)反应①的化学方程式并用双线桥法表示电子转移的方向和数目为
(5)若澄清石灰水过量,反应②的离子方程式为
(6)反应③的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】甲、乙、丙为常见单质,乙、丙两元素在周期表中位于同一主族。X、A、B、C、D、E、F、G均为常见的化合物,其中A和X的摩尔质量相同,A、G的焰色反应为黄色。在一定条件下,各物质相互转化关系如右图。请回答:

(1)写化学式:丙____ ,E________
(2)X的电子式为_____________ 。
(3)写出反应⑥的化学反应方程式:______________________________________ 。
(4)写出B与G溶液反应生成F的离子方程式:____________________________ 。

(1)写化学式:丙
(2)X的电子式为
(3)写出反应⑥的化学反应方程式:
(4)写出B与G溶液反应生成F的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】已知:A、B、C均是由短周期元素组成的单质,其余物质均为化合物。F在常温常压下为液态,I为具有磁性的黑色晶体。它们有下图所示的转化关系:

根据以上转换关系回答:
(1)写出反应①的化学方程式:__________________ ____;
(2)写出反应②的离子方程式:_______ _______________________;
写出H+E反应的离子方程式:____ _______________________;
(3)将I溶于足量盐酸,请分别写出反应后混合溶液中存在的阳离子、检验所需试剂及相应现象(可不填满):

根据以上转换关系回答:
(1)写出反应①的化学方程式:__________________ ____;
(2)写出反应②的离子方程式:_______ _______________________;
写出H+E反应的离子方程式:____ _______________________;
(3)将I溶于足量盐酸,请分别写出反应后混合溶液中存在的阳离子、检验所需试剂及相应现象(可不填满):
| 阳离子 | 检验试剂 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同元素,它们可发生如图所示的转化反应(反应条件和部分产物已略去):甲 乙
乙 丙
丙
(1)若甲为目前使用最为广泛的金属,甲和丁的稀溶液反应生成无色气体。则丁的化学式为_______ , 检验乙溶液中的金属阳离子的方法为:_______ 。
(2)若甲为氯碱工业的产品,含丙的某种药品可用于治疗胃酸过多。则丁的化学式为_______ ,鉴别等浓度的乙溶液和丙溶液,可选用的试剂为_______ (填字母序号)。
A.NaOH溶液 B. CaCl2溶液 C.稀硫酸 D.澄清石灰水
(3)若甲为常用的净水剂,乙具有两性。则丁的化学式为_______ ,乙与丁反应生成丙的离子方程式为_______ 。
(4)若甲为臭鸡蛋气味的气体,丙为有刺激性气味的气体。则丁的化学式为_______ ,丙与甲反应生成乙的化学方程式为_______ 。
 乙
乙 丙
丙(1)若甲为目前使用最为广泛的金属,甲和丁的稀溶液反应生成无色气体。则丁的化学式为
(2)若甲为氯碱工业的产品,含丙的某种药品可用于治疗胃酸过多。则丁的化学式为
A.NaOH溶液 B. CaCl2溶液 C.稀硫酸 D.澄清石灰水
(3)若甲为常用的净水剂,乙具有两性。则丁的化学式为
(4)若甲为臭鸡蛋气味的气体,丙为有刺激性气味的气体。则丁的化学式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】工业上的许多反应工艺来源于实验室里的简单操作,比如用铝土矿(成分为氧化铝、氧化铁)制取铝的过程如图:

请回答下列问题:
(1)写出铝土矿中加入NaOH溶液的反应方程式___ 。
(2)沉淀C的化学式___ ,颜色为___ ,写出它的一种用途___ 。
(3)操作I、操作II、操作III的名称为___ ,这个过程用到的玻璃仪器有烧杯、___ 。
(4)整个生产过程中,除可以循环使用的物质有___ (写出3种,填化学式),用此法制取铝的副产品是___ (写出2种,填化学式)。
(5)氧化铝熔点高,氯化铝熔点低,工业上为什么不用熔点较低的氯化铝而用熔点更高的氧化铝为原料电解制铝?___ 。

请回答下列问题:
(1)写出铝土矿中加入NaOH溶液的反应方程式
(2)沉淀C的化学式
(3)操作I、操作II、操作III的名称为
(4)整个生产过程中,除可以循环使用的物质有
(5)氧化铝熔点高,氯化铝熔点低,工业上为什么不用熔点较低的氯化铝而用熔点更高的氧化铝为原料电解制铝?
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】化学平衡原理是中学化学学习的重要内容,请回答下列问题:
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上可用合成气(主要成分CO、H2)制备甲醇。
(1)已知:CO、H2、CH3OH、的燃烧热(△H)分别为-283.0kJ/mol、-241.8kJ/mol、-192.2 kJ/mol,请写出合成气制备甲醇的热化学方程式。
(2)若在绝热、恒容的密闭容器中充入1 mol CO、2 mol H2,发生CO(g)+2H2(g) CH3OH(g)反应,下列示意图正确且能说明反应在进行到t1时刻为平衡状态的是______(填选项字母)。
CH3OH(g)反应,下列示意图正确且能说明反应在进行到t1时刻为平衡状态的是______(填选项字母)。
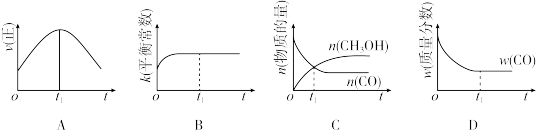
(3)在T1℃时,在体积为5 L的恒容容器中充入3 mol的合成气,反应达到平衡时CH3OH的体积分数与n(H2)/n(CO)的关系如图所示。H2和CO按2:1投入时经过5 min达到平衡,则5 min内用H2表示的反应速率为v(H2)=_______。温度不变,当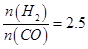 时,达到平衡状态,CH3OH的体积分数可能是图象中的______点。
时,达到平衡状态,CH3OH的体积分数可能是图象中的______点。

(4)含有甲醇的废水随意排放会造成水污染,可用ClO2将其氧化为CO2,然后再加碱中和即可。写出处理甲醇酸性废水过程中,ClO2与甲醇反应的离子方程式:________________________。
(5)水的自偶电离可表示为H2O+H2O H3O++OH-。与水电离相似,甲醇也能发生自偶电离,请写出甲醇的自偶电离方程式_______________________________________,往甲醇中加入少量金属钠反应生成甲醇钠,则反应后的混合液中的电荷守恒式_____________________________。
H3O++OH-。与水电离相似,甲醇也能发生自偶电离,请写出甲醇的自偶电离方程式_______________________________________,往甲醇中加入少量金属钠反应生成甲醇钠,则反应后的混合液中的电荷守恒式_____________________________。
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上可用合成气(主要成分CO、H2)制备甲醇。
(1)已知:CO、H2、CH3OH、的燃烧热(△H)分别为-283.0kJ/mol、-241.8kJ/mol、-192.2 kJ/mol,请写出合成气制备甲醇的热化学方程式。
(2)若在绝热、恒容的密闭容器中充入1 mol CO、2 mol H2,发生CO(g)+2H2(g)
 CH3OH(g)反应,下列示意图正确且能说明反应在进行到t1时刻为平衡状态的是______(填选项字母)。
CH3OH(g)反应,下列示意图正确且能说明反应在进行到t1时刻为平衡状态的是______(填选项字母)。
(3)在T1℃时,在体积为5 L的恒容容器中充入3 mol的合成气,反应达到平衡时CH3OH的体积分数与n(H2)/n(CO)的关系如图所示。H2和CO按2:1投入时经过5 min达到平衡,则5 min内用H2表示的反应速率为v(H2)=_______。温度不变,当
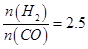 时,达到平衡状态,CH3OH的体积分数可能是图象中的______点。
时,达到平衡状态,CH3OH的体积分数可能是图象中的______点。
(4)含有甲醇的废水随意排放会造成水污染,可用ClO2将其氧化为CO2,然后再加碱中和即可。写出处理甲醇酸性废水过程中,ClO2与甲醇反应的离子方程式:________________________。
(5)水的自偶电离可表示为H2O+H2O
 H3O++OH-。与水电离相似,甲醇也能发生自偶电离,请写出甲醇的自偶电离方程式_______________________________________,往甲醇中加入少量金属钠反应生成甲醇钠,则反应后的混合液中的电荷守恒式_____________________________。
H3O++OH-。与水电离相似,甲醇也能发生自偶电离,请写出甲醇的自偶电离方程式_______________________________________,往甲醇中加入少量金属钠反应生成甲醇钠,则反应后的混合液中的电荷守恒式_____________________________。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】硫的氧化物是形成酸雨的罪魁祸首,含硫烟气(主要成分为SO2)的处理方法备受关注,主要有以下两种方法。请回答下列问题:
I.碱液吸收法
步骤1:用足量氨水吸收SO2
步骤2:再加入熟石灰,发生反应:2NH +Ca2++2OH-+SO
+Ca2++2OH-+SO =CaSO3↓+2NH3•H2O
=CaSO3↓+2NH3•H2O
(1)已知:25℃时,Kb(NH3•H2O)=a;Ksp(CaSO3)=b,该温度下,步骤2中反应的平衡常数K=____ (用含a、b的代数式表示)。
(2)氨水吸收SO2最终也可转化为(NH4)2SO4溶液,则该溶液中离子浓度由大到小依次为____ 。
(3)工业上还可用Na2SO3溶液吸收烟气中的SO2:Na2SO3+SO2+H2O=2NaHSO3。某温度下用1.0mol/LNa2SO3溶液吸收纯净的SO2,当溶液中c(SO )降至0.2mol/L时,吸收能力显著下降,应更换吸收剂。此时溶液的pH=
)降至0.2mol/L时,吸收能力显著下降,应更换吸收剂。此时溶液的pH=____ 。(已知该温度下亚硫酸的电离平衡常数Ka1=1.75×10-2,Ka2=1.25×10-7)
II.水煤气还原法
已知:①2CO(g)+SO2(g) S(l)+2CO2(g) △H1=-37.0kJ•mol-1
S(l)+2CO2(g) △H1=-37.0kJ•mol-1
②2H2(g)+SO2(g) S(l)+2H2O(g) △H2=+45.4kJ•mol-1
S(l)+2H2O(g) △H2=+45.4kJ•mol-1
(4)写出CO(g)与H2O(g)反应生成CO2(g)、H2(g)的热化学方程式:____ 。若该反应在恒温、恒容体系中进行,达到平衡的标志为____ (填选项字母)。
A.单位时间内,生成nmolCO的同时生成nmolCO2
B.混合气体的密度保持不变
C.混合气体的总压强保持不变
D.H2O(g)与H2(g)的体积比保持不变
(5)反应②的正反应的活化能E正____ (填“>”“<”或“=”)逆反应的活化能E逆。
(6)T℃,向10L恒容密闭容器中充入2molCO(g)、2molSO2(g)和2molH2(g),发生反应①和②,5min达到平衡时,CO2(g)和H2O(g)的物质的量分别为1.6mol、1.8mol。T℃时,反应②的平衡常数K=____ 。
I.碱液吸收法
步骤1:用足量氨水吸收SO2
步骤2:再加入熟石灰,发生反应:2NH
 +Ca2++2OH-+SO
+Ca2++2OH-+SO =CaSO3↓+2NH3•H2O
=CaSO3↓+2NH3•H2O(1)已知:25℃时,Kb(NH3•H2O)=a;Ksp(CaSO3)=b,该温度下,步骤2中反应的平衡常数K=
(2)氨水吸收SO2最终也可转化为(NH4)2SO4溶液,则该溶液中离子浓度由大到小依次为
(3)工业上还可用Na2SO3溶液吸收烟气中的SO2:Na2SO3+SO2+H2O=2NaHSO3。某温度下用1.0mol/LNa2SO3溶液吸收纯净的SO2,当溶液中c(SO
 )降至0.2mol/L时,吸收能力显著下降,应更换吸收剂。此时溶液的pH=
)降至0.2mol/L时,吸收能力显著下降,应更换吸收剂。此时溶液的pH=II.水煤气还原法
已知:①2CO(g)+SO2(g)
 S(l)+2CO2(g) △H1=-37.0kJ•mol-1
S(l)+2CO2(g) △H1=-37.0kJ•mol-1②2H2(g)+SO2(g)
 S(l)+2H2O(g) △H2=+45.4kJ•mol-1
S(l)+2H2O(g) △H2=+45.4kJ•mol-1(4)写出CO(g)与H2O(g)反应生成CO2(g)、H2(g)的热化学方程式:
A.单位时间内,生成nmolCO的同时生成nmolCO2
B.混合气体的密度保持不变
C.混合气体的总压强保持不变
D.H2O(g)与H2(g)的体积比保持不变
(5)反应②的正反应的活化能E正
(6)T℃,向10L恒容密闭容器中充入2molCO(g)、2molSO2(g)和2molH2(g),发生反应①和②,5min达到平衡时,CO2(g)和H2O(g)的物质的量分别为1.6mol、1.8mol。T℃时,反应②的平衡常数K=
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D都是中学化学常见的物质,其中A、B、C均含有同一种元素。在一定条件下相互转化的关系如下图所示。

请回答下列问题。
(1)若通常情况下A、B、C、D都是气体,且B和D为空气的主要成分写出反应(Ⅲ)的化学方程式:
___________
(2)若D为氯碱工业的重要产品,A、B、C为均含有同一种金属元素的无机化合物,反应(Ⅲ)的离子方程式为___________
(3)若B为非金属单质,且B所含元素的原子最外层电子数与内层电子数之和的比值为3:5,则反应(Ⅲ)中氧化产物与还原产物的物质的量之比为_______________________ 。0.1 mol A与含O.15 mol NaOH的溶液充分反应后,溶液中所含离子浓度的大小关系为______________________________ 。
(4)若A、B、C的溶液均显碱性,C为焙制糕点的发酵粉的主要成分之一。
①A中所含化学键类型为_________________ ,D的电子式为_____________________ 。
②25℃时,浓度均为O.1 mol/l的B、C溶液,pH较大的是_______ (填溶质的化学式)溶液,写出B 溶液中显电中性的原因:______________________ 。已知,B溶液的PH=a,则其水电离出来的H+的浓度为:______

请回答下列问题。
(1)若通常情况下A、B、C、D都是气体,且B和D为空气的主要成分写出反应(Ⅲ)的化学方程式:
(2)若D为氯碱工业的重要产品,A、B、C为均含有同一种金属元素的无机化合物,反应(Ⅲ)的离子方程式为
(3)若B为非金属单质,且B所含元素的原子最外层电子数与内层电子数之和的比值为3:5,则反应(Ⅲ)中氧化产物与还原产物的物质的量之比为
(4)若A、B、C的溶液均显碱性,C为焙制糕点的发酵粉的主要成分之一。
①A中所含化学键类型为
②25℃时,浓度均为O.1 mol/l的B、C溶液,pH较大的是
您最近一年使用:0次



