Boderlscens研究反应:H2(g)+I2(g) 2HI(g) △H<0.温度T时,在两个体积均为1L的密闭容器中进行实验,测得气体混合物中碘化氢的物质的量分数ω(HI)与反应时间t的关系如下表:
2HI(g) △H<0.温度T时,在两个体积均为1L的密闭容器中进行实验,测得气体混合物中碘化氢的物质的量分数ω(HI)与反应时间t的关系如下表:
研究发现上述反应中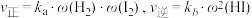 ,其中
,其中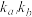 为常数。下列说法正确的是
为常数。下列说法正确的是
 2HI(g) △H<0.温度T时,在两个体积均为1L的密闭容器中进行实验,测得气体混合物中碘化氢的物质的量分数ω(HI)与反应时间t的关系如下表:
2HI(g) △H<0.温度T时,在两个体积均为1L的密闭容器中进行实验,测得气体混合物中碘化氢的物质的量分数ω(HI)与反应时间t的关系如下表:容器编号 | 起始物质 | t/min | 0 | 20 | 40 | 60 | 80 | 100 |
I | 0.5molI2、0.5molH2 | w(HI)/% | 0 | 50 | 68 | 76 | 80 | 80 |
II | xmol HI | w(HI)/% | 100 | 91 | 84 | 81 | 80 | 80 |
研究发现上述反应中
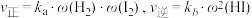 ,其中
,其中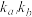 为常数。下列说法正确的是
为常数。下列说法正确的是A.温度为T时该反应的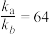 |
| B.容器I中前20 min的平均速率v(HI)=0.0125mol.L-1.min-1 |
| C.若起始时,向容器I中加入物质的量均为0.l mol的H2、I2、HI,反应逆向进行 |
D.若两容器中 且 且 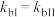 则x的值一定为1 则x的值一定为1 |
更新时间:2018-04-03 14:24:24
|
相似题推荐
多选题
|
适中
(0.65)
【推荐1】对水样中M的分解速率的影响因素进行研究,每次取2L水样进行实验,在相同温度下,M的物质的量[n(M)]随时间(t)变化的有关实验数据如下图所示,下列说法正确的是

| A.由③④得,水样中添加Cu2+,能加快M的分解速率 |
| B.由②③得,反应物浓度越大,M的分解速率越快 |
| C.由②④得,水样的pH越小,M的分解速率越快 |
| D.在0~20min内,②中M的平均分解速率为0.0075mol/(L·min) |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】一定温度下:在 的四氯化碳溶液(100mL)中发生分解反应:
的四氯化碳溶液(100mL)中发生分解反应: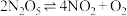 。在不同时刻测量放出的
。在不同时刻测量放出的 体积,换算成
体积,换算成 浓度如下表:
浓度如下表:
下列说法正确的是
 的四氯化碳溶液(100mL)中发生分解反应:
的四氯化碳溶液(100mL)中发生分解反应: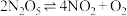 。在不同时刻测量放出的
。在不同时刻测量放出的 体积,换算成
体积,换算成 浓度如下表:
浓度如下表:| t/s | 0 | 600 | 1200 | 1710 | 2220 | 2820 | x |
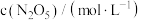 | 1.40 | 0.96 | 0.66 | 0.48 | 0.35 | 0.24 | 0.12 |
A.600~1200s,生成 的平均速率为 的平均速率为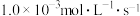 |
B.反应2220s时,放出的 体积为11.8L(标准状况) 体积为11.8L(标准状况) |
C.反应达到平衡时, |
| D.推测上表中的x为3930 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐3】一定温度下,1molX和nmolY在容积为2L的密闭容器中发生反应:X(g)+Y(g) 2Z(g)+M(s),5min后达到平衡状态,此时生成2amolZ,下列说法正确的是
2Z(g)+M(s),5min后达到平衡状态,此时生成2amolZ,下列说法正确的是
 2Z(g)+M(s),5min后达到平衡状态,此时生成2amolZ,下列说法正确的是
2Z(g)+M(s),5min后达到平衡状态,此时生成2amolZ,下列说法正确的是| A.当混合气体的质量不再发生变化时,说明反应达到平衡状态 |
| B.0~5min时间段内,用M表示的平均反应速率是0.1amol·L-1·min-1 |
| C.0~5min时间段内,用X表示的平均反应速率是0.1amol·L-1·min-1 |
| D.当混合气体的压强不再发生变化时;说明反应达到平衡状态 |
您最近一年使用:0次
【推荐1】相同温度下,容积相同的甲,乙两个恒容密闭容器均发生如下反应:N2+3H2 2NH3 ΔH=-92.4kJ/mol,实验测得有关数据如下;下列判断中正确的是
2NH3 ΔH=-92.4kJ/mol,实验测得有关数据如下;下列判断中正确的是
 2NH3 ΔH=-92.4kJ/mol,实验测得有关数据如下;下列判断中正确的是
2NH3 ΔH=-92.4kJ/mol,实验测得有关数据如下;下列判断中正确的是| 容器编号 | 起始时各物质的物质的量/mol | 达到平衡时体系能量的变化/kJ | ||
| N2 | 3H2 | NH3 | ||
| 甲 | 1 | 3 | 0 | 放出热量:Q1 |
| 乙 | 0.9 | 2.7 | 0.2 | 放出热量:Q2 |
| A.Q2<Q1=92.4 | B.容器甲先达平衡 |
| C.两容器中反应的平衡常数相等 | D.达到平衡时NH3的体积分数:甲=乙 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】在体积均为1.0 L的恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1 mol CO2和0.2 mol CO2,在不同温度下反应CO2(g)+C(s) 2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是( )
2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是( )
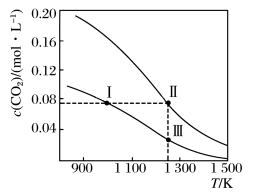
 2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是( )
2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是( )
A.反应CO2(g)+C(s) 2CO(g)△S>0、△H<0 2CO(g)△S>0、△H<0 |
| B.体系的总压强P总:P总(状态Ⅱ)>2P总(状态Ⅰ) |
| C.体系中c(CO):c(CO,状态Ⅱ)<2c(CO,状态Ⅲ) |
| D.逆反应速率V逆:V逆(状态Ⅰ)>V逆(状态Ⅲ) |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐3】一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应2SO2(g)+ O2(g)  2SO3(g) △H = -196.0 KJ/mol,测得反应的相关数据如下,下列说法正确的是
2SO3(g) △H = -196.0 KJ/mol,测得反应的相关数据如下,下列说法正确的是
 2SO3(g) △H = -196.0 KJ/mol,测得反应的相关数据如下,下列说法正确的是
2SO3(g) △H = -196.0 KJ/mol,测得反应的相关数据如下,下列说法正确的是| 容器1 | 容器2 | 容器3 | |
| 应温度T/K | 700 | 700 | 800 |
| 反应物投入量 | 2 mol SO2、1mol O2 | 4mol SO3 | 2 mol SO3 |
平衡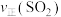 / /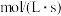 | v1 | v2 | v3 |
平衡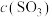 / / | c1 | c2 | c3 |
| 平衡体系总压强p/Pa | p1 | p2 | p3 |
| 反应能量变化 | 放出a KJ | 吸收b KJ | 吸收c KJ |
| 物质的平衡转化率α | α1(SO2) | α2(SO3) | α3(SO3) |
| 平衡常数K | K1 | K2 | K3 |
A. , , | B.K1> K3,p2>2p3 |
C. ,a +b>196.0 ,a +b>196.0 | D. ,α2(SO3 )+α1(SO2 )=1 ,α2(SO3 )+α1(SO2 )=1 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】T℃时,在一固定容积1L的密闭容器中发生反应:A(g)+B(g) C(s),正反应为放热反应,按照不同配比充入
C(s),正反应为放热反应,按照不同配比充入 ,达到平衡时容器中
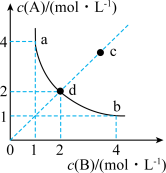
,达到平衡时容器中 浓度变化如图中曲线(实线)所示,下列判断正确的是
浓度变化如图中曲线(实线)所示,下列判断正确的是
 C(s),正反应为放热反应,按照不同配比充入
C(s),正反应为放热反应,按照不同配比充入 ,达到平衡时容器中
,达到平衡时容器中 浓度变化如图中曲线(实线)所示,下列判断正确的是
浓度变化如图中曲线(实线)所示,下列判断正确的是
| A.T℃时,该反应的平衡常数值为4 |
| B.若通入反应物A与B各4mol,则达到平衡点为d点 |
| C.若c点也为平衡点,则平衡从d移动到c改变条件可能为减小压强或升高温度 |
| D.在d点向其中通入A气体,平衡正向移动,达到新平衡可能为a点 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】只改变一个影响因素,平衡常数K与化学平衡移动的关系叙述错误的是
| A.K值不变,平衡可能移动 | B.K值变化,平衡不一定移动 |
| C.平衡移动,K值可能不变 | D.平衡移动,K值一定变化 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】水煤气变换[CO(g)+H2O(g) CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。Shoichi研究了467℃、489℃时水煤气变换中CO和H2分压随时间变化关系(如图甲所示),已知467℃和489℃时反应的平衡常数大于1,催化剂为氧化铁,实验初始时体系中的
CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。Shoichi研究了467℃、489℃时水煤气变换中CO和H2分压随时间变化关系(如图甲所示),已知467℃和489℃时反应的平衡常数大于1,催化剂为氧化铁,实验初始时体系中的 和pCO相等、
和pCO相等、 和
和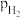 相等。
相等。
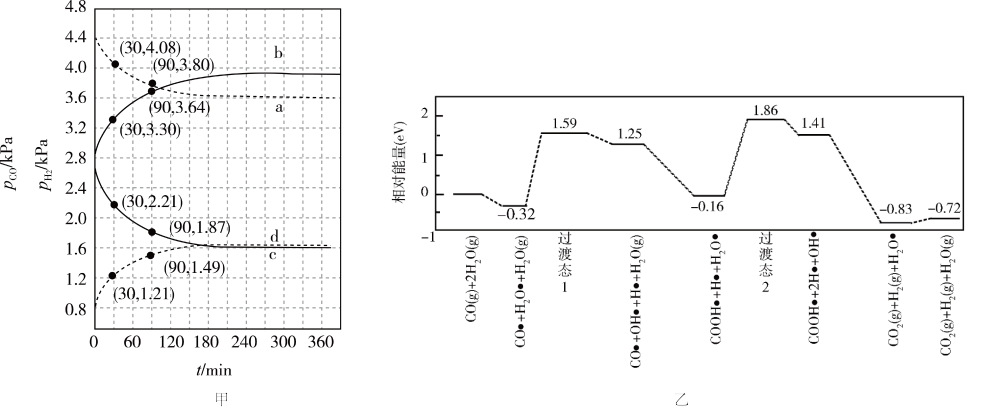
试分析图象判断,下列说法正确的是
 CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。Shoichi研究了467℃、489℃时水煤气变换中CO和H2分压随时间变化关系(如图甲所示),已知467℃和489℃时反应的平衡常数大于1,催化剂为氧化铁,实验初始时体系中的
CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。Shoichi研究了467℃、489℃时水煤气变换中CO和H2分压随时间变化关系(如图甲所示),已知467℃和489℃时反应的平衡常数大于1,催化剂为氧化铁,实验初始时体系中的 和pCO相等、
和pCO相等、 和
和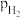 相等。
相等。
试分析图象判断,下列说法正确的是
| A.曲线a的反应在30~90min内的平均速率v(a)=0.0047 kPa·min-1 |
| B.我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图乙所示,其中吸附在金催化剂表面上的物种用*标注,由图象可知水煤气变换的反应是放热反应 |
C.489℃时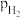 和pCO随时间变化关系的曲线分别是b、c 和pCO随时间变化关系的曲线分别是b、c |
D.467℃时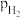 和pCO 和pCO 随时间变化关系的曲线分别是a、d 随时间变化关系的曲线分别是a、d |
您最近一年使用:0次



