镓(31Ga)是一种重要金属元素,镓及其化合物在电子工业、光电子工业、国防工业和超导材料等领域有着广泛的应用。回答下列问题:
(1)基态Ga原子占据最高能级电子的电子云轮廓图形状为__________ ,未成对电子数为________________ 。
(2)Ga(NO3)3中阴离子的立体构型是_____________ ,写出一个与该阴离子的立体构型相同的分子的化学式___________ 。
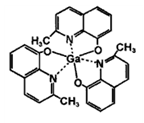
(3)2-甲基-8-羟基喹啉镓(如图)应用于分子印迹技术,2-甲基-8-羟基喹啉镓中五种元素电负性由大到小的顺序是____________________________ (填元素符号),提供孤电子对的成键原子是_____________ 。
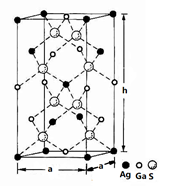
(4)一种硅镓半导体材料的晶胞结构如图所示由硫、镓、银形成的化合物的晶胞是底面为正方形的长方体,结构如下图所示,则该晶体中硫的配位数为___________ ,晶胞底面的边长a=5.75 nm,高h=10.30nm,该晶体密度为__________________ g·cm-3(列出计算式即可)。
(1)基态Ga原子占据最高能级电子的电子云轮廓图形状为
(2)Ga(NO3)3中阴离子的立体构型是
(3)2-甲基-8-羟基喹啉镓(如图)应用于分子印迹技术,2-甲基-8-羟基喹啉镓中五种元素电负性由大到小的顺序是

(4)一种硅镓半导体材料的晶胞结构如图所示由硫、镓、银形成的化合物的晶胞是底面为正方形的长方体,结构如下图所示,则该晶体中硫的配位数为

更新时间:2018/04/28 15:22:05
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】材料是人类文明进步的阶梯,第IIIA、IVA、VA族元素是组成特殊材料的重要元素。请回答下列问题:
(1)基态As原子核外能量最高能级的电子云形状为___________ 。
(2)M与 位于同周期,
位于同周期, 的一种配合物组成为
的一种配合物组成为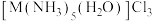 。
。
①下列有关 、
、 的说法正确的是
的说法正确的是___________ (填字母)。
a.分子空间构型相同 b.中心原子杂化类型相同 c.键角大小相同
② 含
含___________ molσ键。
③配合物T与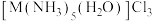 组成元素相同,中心离子的配位数相同。
组成元素相同,中心离子的配位数相同。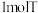 溶于水,加入足量
溶于水,加入足量 溶液可生成
溶液可生成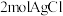 ;且T溶于水加强碱再加热不产生氨气。则T的化学式为
;且T溶于水加强碱再加热不产生氨气。则T的化学式为___________ 。
(3)常压、180℃时, 升华形成的二聚体
升华形成的二聚体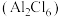 的结构如图所示。
的结构如图所示。___________ 。 的配位数为
的配位数为___________ 。
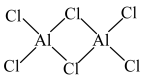
(4)磷化硼(BP)是一种超硬耐磨涂层材料,其晶胞结构如右图所示,该晶胞中B原子填在P原子所围成的___________ (填“立方体”“正四面体”或“正八面体”)空隙中;若该晶体的密度为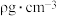 ,
, 是阿伏伽德罗常数的值。BP晶胞中面心上6个P原子相连构成正八面体,该正八面体的边长为
是阿伏伽德罗常数的值。BP晶胞中面心上6个P原子相连构成正八面体,该正八面体的边长为___________  (列式即可)。
(列式即可)。
(1)基态As原子核外能量最高能级的电子云形状为
(2)M与
 位于同周期,
位于同周期, 的一种配合物组成为
的一种配合物组成为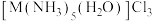 。
。①下列有关
 、
、 的说法正确的是
的说法正确的是a.分子空间构型相同 b.中心原子杂化类型相同 c.键角大小相同
②
 含
含③配合物T与
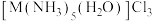 组成元素相同,中心离子的配位数相同。
组成元素相同,中心离子的配位数相同。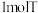 溶于水,加入足量
溶于水,加入足量 溶液可生成
溶液可生成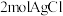 ;且T溶于水加强碱再加热不产生氨气。则T的化学式为
;且T溶于水加强碱再加热不产生氨气。则T的化学式为(3)常压、180℃时,
 升华形成的二聚体
升华形成的二聚体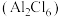 的结构如图所示。
的结构如图所示。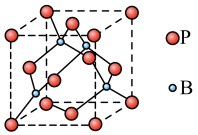
 的配位数为
的配位数为(4)磷化硼(BP)是一种超硬耐磨涂层材料,其晶胞结构如右图所示,该晶胞中B原子填在P原子所围成的
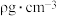 ,
, 是阿伏伽德罗常数的值。BP晶胞中面心上6个P原子相连构成正八面体,该正八面体的边长为
是阿伏伽德罗常数的值。BP晶胞中面心上6个P原子相连构成正八面体,该正八面体的边长为 (列式即可)。
(列式即可)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】太阳能电池一共可分为三代,请回答下列问题:
(1)第一代太阳能电池为硅基太阳能电池,其中以单晶硅太阳能电池的转化效率最高,技术最为成熟,应用最为广泛。
①在基态Si原子中,电子占据的最高能层符号为___________ ,电子占据的最高能级的电子云轮廓图为___________ 。
②根据对角线规则,Si的一些化学性质与___________ (填短周期元素名称)相似。
(2)第二代太阳能电池是薄膜太阳能电池,如砷化镓电池。
①原子半径:Ga___________ As(填“大于”或“小于”,下同),第一电离能:Ga___________ As。
② 分子含有
分子含有___________ (填“ 键”或“
键”或“ 键”),As的最高价氧化物的化学式为
键”),As的最高价氧化物的化学式为___________ 。
③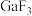 的熔点约为1000℃,
的熔点约为1000℃, 的熔点为77.9℃,其原因是
的熔点为77.9℃,其原因是___________ 。
④Ga、F、Cl的电负性由大到小的顺序为___________ 。
(3)第三代太阳能电池—钙钛矿型太阳能电池,它利用有机金属卤化物(组成为 、
、 和有机碱离子
和有机碱离子 )作为吸光材料,其晶胞结构如图所示。
)作为吸光材料,其晶胞结构如图所示。

①该有机碱离子中,C、N原子的杂化轨道类型分别为___________ 、___________ 。
②若晶胞参数为apm,则晶体密度为___________  。(阿伏加德罗常数的值为
。(阿伏加德罗常数的值为 ,列出计算式)
,列出计算式)
(1)第一代太阳能电池为硅基太阳能电池,其中以单晶硅太阳能电池的转化效率最高,技术最为成熟,应用最为广泛。
①在基态Si原子中,电子占据的最高能层符号为
②根据对角线规则,Si的一些化学性质与
(2)第二代太阳能电池是薄膜太阳能电池,如砷化镓电池。
①原子半径:Ga
②
 分子含有
分子含有 键”或“
键”或“ 键”),As的最高价氧化物的化学式为
键”),As的最高价氧化物的化学式为③
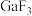 的熔点约为1000℃,
的熔点约为1000℃, 的熔点为77.9℃,其原因是
的熔点为77.9℃,其原因是④Ga、F、Cl的电负性由大到小的顺序为
(3)第三代太阳能电池—钙钛矿型太阳能电池,它利用有机金属卤化物(组成为
 、
、 和有机碱离子
和有机碱离子 )作为吸光材料,其晶胞结构如图所示。
)作为吸光材料,其晶胞结构如图所示。
①该有机碱离子中,C、N原子的杂化轨道类型分别为
②若晶胞参数为apm,则晶体密度为
 。(阿伏加德罗常数的值为
。(阿伏加德罗常数的值为 ,列出计算式)
,列出计算式)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】氮及其化合物应用广泛。回答下列问题:
(1)基态N原子处于最高能级的电子云轮廓图为__________ 形。
(2)胍(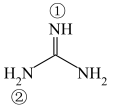 )为平面形分子,存在大π键
)为平面形分子,存在大π键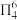 。胍属于
。胍属于__________ 分子(填“极性”或“非极性”),①号N原子H-N-C键角__________ ②号N原子H-N-C键角(填“>”“<”或“=”),胍易吸收空气中H2O和CO2,其原因是____________________________________ 。
(3)氮化钴属于立方晶系,经Cu掺杂得催化剂X,经Li掺杂得催化剂Y。
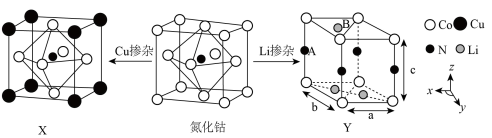
X属于立方晶系,晶胞参数为dpm,距离最近Co原子的核间距为__________ pm,Y属于六方晶系,晶胞参数为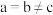 ,
, ,
,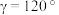 ,如A点原子的分数坐标为
,如A点原子的分数坐标为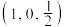 ,则B点Li原子的分数坐标为
,则B点Li原子的分数坐标为____________ ,1个N原子周围距离相等且最近的Li原子数目为_____________ 。
(1)基态N原子处于最高能级的电子云轮廓图为
(2)胍(
 )为平面形分子,存在大π键
)为平面形分子,存在大π键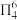 。胍属于
。胍属于(3)氮化钴属于立方晶系,经Cu掺杂得催化剂X,经Li掺杂得催化剂Y。

X属于立方晶系,晶胞参数为dpm,距离最近Co原子的核间距为
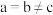 ,
, ,
,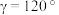 ,如A点原子的分数坐标为
,如A点原子的分数坐标为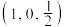 ,则B点Li原子的分数坐标为
,则B点Li原子的分数坐标为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、E分别代表五种短周期元素,且原子序数依次增大,已知:B的最外层电子排布是nsnnpn+1;C的p能级上未成对的电子比B少一个;D的二价阳离子与C的阴离子具有相同的电子层结构;E与D同周期且E在该周期中原子半径最小;B与A的单质能生成具有刺激性气味的气体,该气体极易溶于水。)
(1)B原子核外电子排布式为___________ 。
(2)A与E化合时原子间以___________ 键相结合,D与C化合时原子间以___________ 键相结合。
(3)写出A、C的单质直接化合形成的化合物与E单质反应的离子方程式:___________ 。
(4)A与B形成化合物时,中心原子采取___________ 杂化成键,其立体结构为___________ ,属于___________ (填“极性”或“非极性”)分子。
(5)将白色的无水CuSO4溶解于A2C中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子。请写出生成此配合离子的离子方程式:___________ 。
(6)五种元素中电负性最大的是___________ (填元素名称)。
(1)B原子核外电子排布式为
(2)A与E化合时原子间以
(3)写出A、C的单质直接化合形成的化合物与E单质反应的离子方程式:
(4)A与B形成化合物时,中心原子采取
(5)将白色的无水CuSO4溶解于A2C中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子。请写出生成此配合离子的离子方程式:
(6)五种元素中电负性最大的是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】向 溶液中滴加过量的氨水得到含有
溶液中滴加过量的氨水得到含有 的溶液。
的溶液。
(1)基态 的价层电子排布式为
的价层电子排布式为_______ 。
(2)基态 占据的最高能级的电子云轮廓图的形状是
占据的最高能级的电子云轮廓图的形状是_______ 。
(3)O、N、H的电负性由大到小的顺序是_______ 。
(4)下列状态的氮中,电离最外层一个电子所需能量最小的是_______ (填序号)。 的晶胞结构示意图如下。
的晶胞结构示意图如下。 中一个
中一个 的结构式
的结构式_______ 。
_______  (填“>”“<”或“=”),原因是
(填“>”“<”或“=”),原因是_______ 。
③该立方晶胞的边长为a cm,阿伏加德罗常数为 ,
, 的摩尔质量为M g/mol,则该晶体的密度为
的摩尔质量为M g/mol,则该晶体的密度为_______  。
。
 溶液中滴加过量的氨水得到含有
溶液中滴加过量的氨水得到含有 的溶液。
的溶液。(1)基态
 的价层电子排布式为
的价层电子排布式为(2)基态
 占据的最高能级的电子云轮廓图的形状是
占据的最高能级的电子云轮廓图的形状是(3)O、N、H的电负性由大到小的顺序是
(4)下列状态的氮中,电离最外层一个电子所需能量最小的是
a. b.
b. c.
c.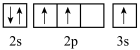
 的晶胞结构示意图如下。
的晶胞结构示意图如下。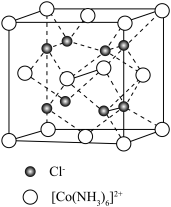
 中一个
中一个 的结构式
的结构式

 (填“>”“<”或“=”),原因是
(填“>”“<”或“=”),原因是③该立方晶胞的边长为a cm,阿伏加德罗常数为
 ,
, 的摩尔质量为M g/mol,则该晶体的密度为
的摩尔质量为M g/mol,则该晶体的密度为 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】硫及其化合物种类繁多,应用广泛。请回答:
(1)基态硫原子的价层电子排布图是_______ 。
(2)下列有关说法正确的是_______。
(3) 中的O-O比H2O2中的更
中的O-O比H2O2中的更_______ (填“难”或“易”)断裂。其原因是_______ 。
(4)锌与硫形成的化合物晶体的晶胞如图所示。_______ 。
②设 为阿伏加德罗常数的值,晶胞参数为anm,则该晶体的密度
为阿伏加德罗常数的值,晶胞参数为anm,则该晶体的密度_______ 。
(1)基态硫原子的价层电子排布图是
(2)下列有关说法正确的是_______。
| A.同周期元素中,第一电离能大于硫元素的有3种 |
| B.SO2的VSEPR模型和空间结构均为V形 |
C.甲基磺酸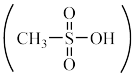 中S原子采取sp杂化 中S原子采取sp杂化 |
D. 的发射光谱不止1条谱线 的发射光谱不止1条谱线 |
(3)
 中的O-O比H2O2中的更
中的O-O比H2O2中的更(4)锌与硫形成的化合物晶体的晶胞如图所示。
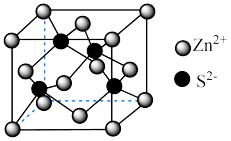
②设
 为阿伏加德罗常数的值,晶胞参数为anm,则该晶体的密度
为阿伏加德罗常数的值,晶胞参数为anm,则该晶体的密度
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态Ge原子的价电子排布式为_______ ,有_______ 个未成对电子。
(2)Ge与C是同主族元素,第一电离能Ge_______ C(填“大于”或“小于”)。
(3)比较下列锗卤化物的熔点和沸点,分析锗卤化物变化原因_______ 。
GeCl4水解可获得高纯GeO2,经H2还原成金属Ge。GeCl4的空间结构为_______ 。
(4)Ge单晶具有金刚石型结构,Ge单晶的熔点比金刚石_______ (填“高”或“低”)。
(5)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为( ,0,
,0, );C为(
);C为( ,
, ,0)。则D原子的坐标参数为
,0)。则D原子的坐标参数为_______ 。

②已知Ge单晶的晶胞参数 a pm,其密度为_______ g∙cm-3(列出计算式即可)。
(1)基态Ge原子的价电子排布式为
(2)Ge与C是同主族元素,第一电离能Ge
(3)比较下列锗卤化物的熔点和沸点,分析锗卤化物变化原因
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | -49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约400 |
(4)Ge单晶具有金刚石型结构,Ge单晶的熔点比金刚石
(5)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(
 ,0,
,0, );C为(
);C为( ,
, ,0)。则D原子的坐标参数为
,0)。则D原子的坐标参数为
②已知Ge单晶的晶胞参数 a pm,其密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】科技前沿科学家利用3D打印技术结合金属合金与陶瓷颗粒开发出新型合金GRX-810,该合金可用于制造飞机和航天器的高温零件。GRX-810主要由镍、钴、铬制成,并掺入一种陶瓷氧化物的纳米颗粒形成氧化物弥散强化合金。回答下列问题:
(1)金属铬基态原子的价层电子排布图为_______ 。
(2)镍可形成Ni(NH3)4(NCS)2、Ni(NH3)4(NO2)2、[Ni(NH3)6]SO4等多种配合物。
①配体 中,电负性最大的元素是
中,电负性最大的元素是_______ 。
②配体 的空间构型为
的空间构型为_______ 形。
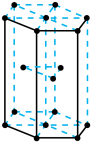
(3)镍的晶胞结构如图所示,则该晶胞中Ni原子个数为_______ 。已知图中六棱柱边长为a pm,高为c pm,该晶胞密度为 ρ g・cm-³,则NA=_______ (用含 a、c和ρ 的式子表示)
①原子坐标参数,表示晶胞内部各原子的相对位置。下图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0); B为(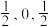 ) ;C为 (
) ;C为 (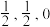 ),则D原子的坐标参数为
),则D原子的坐标参数为_______ 。_______ nm;其密度为_______ g・cm-³(NA为阿伏加德罗常数的值)。
(1)金属铬基态原子的价层电子排布图为
(2)镍可形成Ni(NH3)4(NCS)2、Ni(NH3)4(NO2)2、[Ni(NH3)6]SO4等多种配合物。
①配体
 中,电负性最大的元素是
中,电负性最大的元素是②配体
 的空间构型为
的空间构型为(3)镍的晶胞结构如图所示,则该晶胞中Ni原子个数为
①原子坐标参数,表示晶胞内部各原子的相对位置。下图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0); B为(
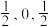 ) ;C为 (
) ;C为 (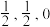 ),则D原子的坐标参数为
),则D原子的坐标参数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】填空
(1)基态Si原子核外电子的空间运动状态有_____ 种,其价层电子排布式为_____ 。
(2)N2F2(二氟氮烯)分子中,氮原子的杂化类型为sp2,则N2F2的结构式为_____ 。
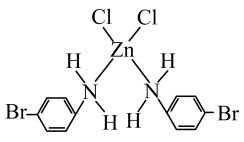
(3)一种锌的配合物结构如图所示。该配合物中H-N-H键角为109.5°,而NH3分子中H-N-H键角为107°,原因是_____ 。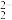 所形成的
所形成的_____ (填“正四面体”或“正八面体”)空隙;若晶胞参数为anm,密度为pg·cm-3,阿伏加德罗常数的值为NA,则FeS2的摩尔质量M=_____ g·mol-1(用含a、p、NA的代数式表示)。
(1)基态Si原子核外电子的空间运动状态有
(2)N2F2(二氟氮烯)分子中,氮原子的杂化类型为sp2,则N2F2的结构式为
(3)一种锌的配合物结构如图所示。该配合物中H-N-H键角为109.5°,而NH3分子中H-N-H键角为107°,原因是
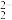 所形成的
所形成的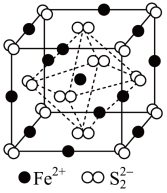
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】很多过渡金属及其化合物在工业上有重要用途。
(1)钛铁合金是钛系储氢合金的代表,该合金具有放氢温度低、价格适中等优点。
①Fe的基态原子价电子排布式为___ 。
②Ti的基态原子共有___ 种不同空间运动状态的电子。
(2)制备CrO2Cl2的反应为K2Cr2O7+3CCl4=2KCl+2CrO2Cl2+3COCl2↑。
①上述化学方程式中非金属元素电负性由小到大的顺序是___ (用元素符号表示)。
②CCl4和COCl2分子中所有原子均满足8电子构型,CCl4和COCl2分子中σ键的个数比为___ ,COCl2分子的中心原子的杂化方式为___ 。
(3)金属铁可导电,导热,具有金属光泽,有延展性,这些性质都可以用___ “理论”解释。
(4)Ni和La的合金也是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在日本和中国已实现了产业化。该合金的晶胞结构如图所示。
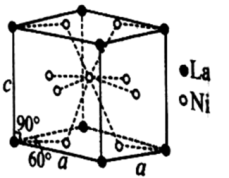
①该晶体的化学式为___ 。
②已知该晶胞的摩尔质量为Mg·mol-1,密度为dg·cm-3。设NA为阿伏加德罗常数的值,则该晶胞的体积是___ cm3(用含M、d、NA的代数式表示)。
(1)钛铁合金是钛系储氢合金的代表,该合金具有放氢温度低、价格适中等优点。
①Fe的基态原子价电子排布式为
②Ti的基态原子共有
(2)制备CrO2Cl2的反应为K2Cr2O7+3CCl4=2KCl+2CrO2Cl2+3COCl2↑。
①上述化学方程式中非金属元素电负性由小到大的顺序是
②CCl4和COCl2分子中所有原子均满足8电子构型,CCl4和COCl2分子中σ键的个数比为
(3)金属铁可导电,导热,具有金属光泽,有延展性,这些性质都可以用
(4)Ni和La的合金也是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在日本和中国已实现了产业化。该合金的晶胞结构如图所示。

①该晶体的化学式为
②已知该晶胞的摩尔质量为Mg·mol-1,密度为dg·cm-3。设NA为阿伏加德罗常数的值,则该晶胞的体积是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】1998年,LiW,Dhandapani B等制备了一种具有良好加氢脱氮性质的催化剂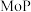 ,开辟了一类全新的催化材料。近年来,过渡金属磷化物(
,开辟了一类全新的催化材料。近年来,过渡金属磷化物(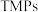 )作为一种新型催化材料,开始广泛应用在电化学、生物学、光学、催化等方面。常见的过渡金属磷化物有
)作为一种新型催化材料,开始广泛应用在电化学、生物学、光学、催化等方面。常见的过渡金属磷化物有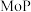 、
、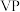 、
、 、
、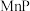 、
、 、
、 等,在金属磷化物中金属原子围绕着非金属原子形成正三棱柱,非金属原子位于正三棱柱的中心。请回答下列问题:
等,在金属磷化物中金属原子围绕着非金属原子形成正三棱柱,非金属原子位于正三棱柱的中心。请回答下列问题:
(1)基态磷原子的价电子排布式为_______ 。基态 与
与 中未成对电子数之比为
中未成对电子数之比为_______ 。
(2) 、P、S三种元素的第一电离能由大到小的顺序是
、P、S三种元素的第一电离能由大到小的顺序是_______ 。电负性:P_______ As(填“>、=或<”),原因是_______ 。
(3) 分子的空间构型为
分子的空间构型为_______ ,其中P的杂化轨道类型为_______ 杂化。
(4)磷化钒(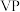 )的晶胞结构如图所示,V作简单六方棱柱体排列,P交替地填入一半的V的正三棱柱中心空隙。与V原子距离相等且最近的P原子有
)的晶胞结构如图所示,V作简单六方棱柱体排列,P交替地填入一半的V的正三棱柱中心空隙。与V原子距离相等且最近的P原子有_______ 个,晶胞的各参数见下图,设阿伏加德罗常数为 ,则
,则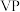 晶体的密度为
晶体的密度为_______  。(列出计算式)
。(列出计算式)
 ,开辟了一类全新的催化材料。近年来,过渡金属磷化物(
,开辟了一类全新的催化材料。近年来,过渡金属磷化物( )作为一种新型催化材料,开始广泛应用在电化学、生物学、光学、催化等方面。常见的过渡金属磷化物有
)作为一种新型催化材料,开始广泛应用在电化学、生物学、光学、催化等方面。常见的过渡金属磷化物有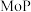 、
、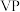 、
、 、
、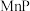 、
、 、
、 等,在金属磷化物中金属原子围绕着非金属原子形成正三棱柱,非金属原子位于正三棱柱的中心。请回答下列问题:
等,在金属磷化物中金属原子围绕着非金属原子形成正三棱柱,非金属原子位于正三棱柱的中心。请回答下列问题:(1)基态磷原子的价电子排布式为
 与
与 中未成对电子数之比为
中未成对电子数之比为(2)
 、P、S三种元素的第一电离能由大到小的顺序是
、P、S三种元素的第一电离能由大到小的顺序是(3)
 分子的空间构型为
分子的空间构型为(4)磷化钒(
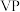 )的晶胞结构如图所示,V作简单六方棱柱体排列,P交替地填入一半的V的正三棱柱中心空隙。与V原子距离相等且最近的P原子有
)的晶胞结构如图所示,V作简单六方棱柱体排列,P交替地填入一半的V的正三棱柱中心空隙。与V原子距离相等且最近的P原子有 ,则
,则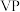 晶体的密度为
晶体的密度为 。(列出计算式)
。(列出计算式)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】我国在新材料领域有重大突破,研发的新材料含有B、C、N、 、
、 、
、 等元素。回答下列问题:
等元素。回答下列问题:
(1)基态 原子的价电子排布式为
原子的价电子排布式为_______ ,电子占据的最高能层的电子云轮廓图形状为_______ 。
(2)B、C、N三种元素中电负性最大的是_______ (填元素符号),C在形成化合物时,其键型以共价键为主,原因是_______ 。
(3)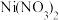 中阴离子的空间构型是
中阴离子的空间构型是_______ ,写出与该阴离子互为等电子体的一种分子的化学式:_______ 。
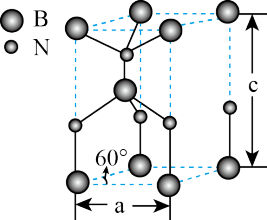
(4)某种含B和N两种元素的功能陶瓷,其原子在晶胞中所处的位置如图所示,该功能陶瓷的化学式为_______ 。若晶胞底边的边长为 ,高为
,高为 ,
, 为阿伏加德罗常数的值,则晶体密度为
为阿伏加德罗常数的值,则晶体密度为_______  (用含a、c的代数式表示)。
(用含a、c的代数式表示)。
 、
、 、
、 等元素。回答下列问题:
等元素。回答下列问题:(1)基态
 原子的价电子排布式为
原子的价电子排布式为(2)B、C、N三种元素中电负性最大的是
(3)
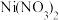 中阴离子的空间构型是
中阴离子的空间构型是(4)某种含B和N两种元素的功能陶瓷,其原子在晶胞中所处的位置如图所示,该功能陶瓷的化学式为
 ,高为
,高为 ,
, 为阿伏加德罗常数的值,则晶体密度为
为阿伏加德罗常数的值,则晶体密度为 (用含a、c的代数式表示)。
(用含a、c的代数式表示)。
您最近一年使用:0次



