室温下将1mol的CuSO4·5H2O(s)溶于水会使溶液温度降低,热效应为△H1, 将1mol的CuSO4(s)溶于水会使溶液温度升高,热效应为△H2;CuSO4·5H2O受热分解的化学方程式为:CuSO4·5H2O(s)═CuSO4(s)+5H2O(l),热效应为△H3 . 则下列判断正确的是
A.△H2>△H3  | B.△H1>△H3  | C.△H1=△H2+△H3  | D.△H1+△H2>△H3 |
更新时间:2018-10-03 16:41:46
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】已知(1)H2O(g) = H2O(l) ΔH1=-Q1 kJ·mol-1
(2)CH3OH(g) = CH3OH(l) △H2=-Q2 kJ·mol-1
(3)2CH3OH(g) +3O2(g) = 2CO2(g)+4H2O(g) △H3=-Q3 kJ·mol-1(Q1、Q2、Q3均大于0)若要使1mol液态甲醇完全燃烧,最后恢复到室温,其△H为
(2)CH3OH(g) = CH3OH(l) △H2=-Q2 kJ·mol-1
(3)2CH3OH(g) +3O2(g) = 2CO2(g)+4H2O(g) △H3=-Q3 kJ·mol-1(Q1、Q2、Q3均大于0)若要使1mol液态甲醇完全燃烧,最后恢复到室温,其△H为
| A.Q2- 0.5Q3-2Q1 | B.0.5Q3-Q2+2Q1 | C.Q3-2Q2+4Q1 | D.0.5(Q1+Q2+Q3) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】十氢萘是具有高储氢密度的氢能载体,经历“十氢萘(C10H18)→四氢萘(C10H12)→萘(C10H8)”的脱氢过程释放氢气。已知:
Ⅰ C10H18(l)==C10H12(l)+3H2(g) ΔH1 Ⅱ C10H12(l)==C10H8(l)+2H2(g) ΔH2
假设某温度下, ΔH1>ΔH2>0。在下图中绘制下列“C10H18→C10H12→C10H8”的“能量~反应过程” 示意图正确的是:
Ⅰ C10H18(l)==C10H12(l)+3H2(g) ΔH1 Ⅱ C10H12(l)==C10H8(l)+2H2(g) ΔH2
假设某温度下, ΔH1>ΔH2>0。在下图中绘制下列“C10H18→C10H12→C10H8”的“能量~反应过程” 示意图正确的是:
A.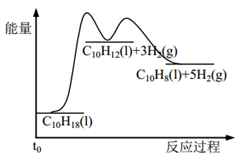 | B. |
C.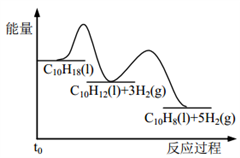 | D.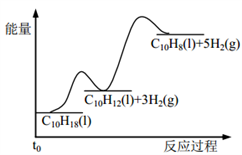 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列有关反应热的叙述中正确的是 ( )
①已知2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ· mol-1,则氢气的燃烧热ΔH=-241.8 kJ· mol-1
②由单质A转化为单质B是一个吸热过程,由此可知单质B比单质A稳定
③X(g)+Y(g) Z(g)+W(s) ΔH>0,恒温恒容条件下达到平衡后加入X,上述反应的ΔH增大
Z(g)+W(s) ΔH>0,恒温恒容条件下达到平衡后加入X,上述反应的ΔH增大
④已知:下表数据可以计算出 (g)+3H2(g)
(g)+3H2(g)
 (g)的焓变
(g)的焓变
⑤根据盖斯定律可推知在相同条件下,金刚石或石墨燃烧生成1 mol CO2(g)时,放出的热量相等
⑥25 ℃、101 kPa时,1 mol碳完全燃烧生成CO2(g)所放出的热量为碳的燃烧热
①已知2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ· mol-1,则氢气的燃烧热ΔH=-241.8 kJ· mol-1
②由单质A转化为单质B是一个吸热过程,由此可知单质B比单质A稳定
③X(g)+Y(g)
 Z(g)+W(s) ΔH>0,恒温恒容条件下达到平衡后加入X,上述反应的ΔH增大
Z(g)+W(s) ΔH>0,恒温恒容条件下达到平衡后加入X,上述反应的ΔH增大④已知:下表数据可以计算出
 (g)+3H2(g)
(g)+3H2(g)
 (g)的焓变
(g)的焓变| 共价键 | C—C | C=C | C—H | H—H |
| 键能/(kJ·mol-1) | 348 | 610 | 413 | 436 |
⑤根据盖斯定律可推知在相同条件下,金刚石或石墨燃烧生成1 mol CO2(g)时,放出的热量相等
⑥25 ℃、101 kPa时,1 mol碳完全燃烧生成CO2(g)所放出的热量为碳的燃烧热
| A.①②③④ | B.③④⑤ | C.④⑤ | D.⑥ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
A.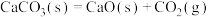 室温下不能自发进行,说明该反应的 室温下不能自发进行,说明该反应的 |
B.一定条件下  , ,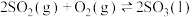  ,则 ,则 |
C.500℃、30MPa下,0.5mol (g)和1.5mol (g)和1.5mol (g)反应生成 (g)反应生成 (g)放热QkJ,其热化学方程式为 (g)放热QkJ,其热化学方程式为  |
D.已知两个平衡体系: 、 、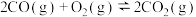 的平衡常数分别为 的平衡常数分别为 和 和 ,可推知平衡 ,可推知平衡 的平衡常数为 的平衡常数为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】用H2O2和H2SO4的混合溶液可腐蚀印刷电路板上的铜,其热化学方程式为Cu(s)+H2O2(l)+2H+(aq)=Cu2+(aq)+2H2O(l) ΔH
已知①Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) ΔH1=64kJ·mol-1
②2H2O2(l)=2H2O(l)+O2(g) ΔH2=-196kJ·mol-1
③H2(g)+ O2(g)=H2O(l) ΔH3=-286kJ·mol-1
O2(g)=H2O(l) ΔH3=-286kJ·mol-1
下列说法不正确的是( )
已知①Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) ΔH1=64kJ·mol-1
②2H2O2(l)=2H2O(l)+O2(g) ΔH2=-196kJ·mol-1
③H2(g)+
 O2(g)=H2O(l) ΔH3=-286kJ·mol-1
O2(g)=H2O(l) ΔH3=-286kJ·mol-1下列说法不正确的是( )
| A.反应①可通过铜作电极电解稀的H2SO4方法实现 |
| B.反应②在任何条件下都能自发进行 |
C.若H2(g)+ O2(g)=H2O(g) ΔH4,则ΔH4<ΔH3 O2(g)=H2O(g) ΔH4,则ΔH4<ΔH3 |
| D.ΔH=-320kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】N2H4(肼)可作制药的原料,也可作火箭的燃料。已知热化学方程式:
反应I:N2H4(g) N2(g)+2H2(g) △H1>0;
N2(g)+2H2(g) △H1>0;
反应II:N2(g)+3H2(g) 2NH3(g) △H2<0;
2NH3(g) △H2<0;
反应III:N2H4(g)+H2(g) 2NH3(g) △H。
2NH3(g) △H。
下列推断不正确的是( )
反应I:N2H4(g)
 N2(g)+2H2(g) △H1>0;
N2(g)+2H2(g) △H1>0;反应II:N2(g)+3H2(g)
 2NH3(g) △H2<0;
2NH3(g) △H2<0;反应III:N2H4(g)+H2(g)
 2NH3(g) △H。
2NH3(g) △H。下列推断不正确的是( )
| A.N2H4断裂共价键需要吸收能量 |
| B.反应I中1molN2H4(g)的能量小于1molN2(g)和2molH2(g)的总能量 |
| C.反应II中正反应的活化能大于逆反应的活化能 |
| D.△H=△H1+△H2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在298K、1.01×105Pa下,将0.5molCO2通入750mL1mol·L-1NaOH溶液中充分反应,测得反应放出xkJ的热量。已知在该条件下,1molCO2通入1L2mol·L-1NaOH溶液中充分反应放出ykJ的热量,则CO2与NaOH溶液反应生成NaHCO3的热化学方程式正确的是( )
| A.CO2(g)+NaOH(aq)=NaHCO3(aq) ΔH=-(4x-y) kJ·mol-1 |
| B.CO2(g)+NaOH(aq)=NaHCO3(aq) ΔH=-(2x-y) kJ·mol-1 |
| C.CO2(g)+NaOH(aq)=NaHCO3(aq) ΔH=-(2y-x) kJ·mol-1 |
| D.2CO2(g)+2NaOH(aq)=2NaHCO3(aq) ΔH=-(8y-2x) kJ·mol-1 |
您最近一年使用:0次

 O2(g)=H2O(g)
O2(g)=H2O(g)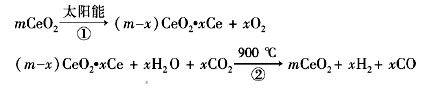
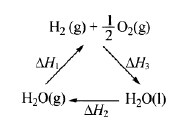
 +2H2O
+2H2O

