下列说法不正确 的是
| A.在恒容下充入惰性气体,容器压强增大,活化分子的百分数不变 |
| B.因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应自发性的判据 |
| C.NH4HCO3(s)=NH3(g)+H2O(g)+CO2(g) ΔH=+185.57kJ·mol-1能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 |
| D.ΔH<0、ΔS>0的反应在任何温度下都能自发进行 |
更新时间:2018-11-15 13:40:50
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】能增加反应物分子中活化分子的百分数的是
| A.升高温度 | B.固体粉碎 | C.增大压强 | D.增加浓度 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】甲烷与氯气在光照条件下存在如下反应历程(”·”表示电子):
①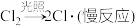 ②
②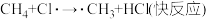
③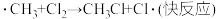 ④
④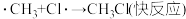
已知在一个分步反应中,较慢的一步反应控制总反应的速率。下列说法不正确的是
①
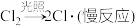 ②
②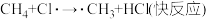
③
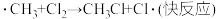 ④
④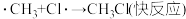
已知在一个分步反应中,较慢的一步反应控制总反应的速率。下列说法不正确的是
A.上述过程的总反应方程式为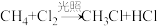 |
| B.光照的主要作用是促进反应①的进行从而使总反应速率加快 |
| C.反应②~④都是由微粒通过碰撞而发生的反应 |
| D.反应①是释放能量的反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列事实不能用勒夏特列原理解释的是
| A.在合成氨实际生产中,使气态氨变成液氨后及时从平衡混合物中分离出去,以提高原料的利用率 |
B. 、 、 、 、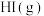 组成的平衡体系,加压后体系颜色变深 组成的平衡体系,加压后体系颜色变深 |
C.向重铬酸钾( )溶液中滴加少量NaOH溶液,溶液颜色由橙色变为黄色 )溶液中滴加少量NaOH溶液,溶液颜色由橙色变为黄色 |
| D.实验室中常用排饱和食盐水的方法收集氯气 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】在密闭容器中发生下列反应aA(g) cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.5倍,下列叙述正确的是
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.5倍,下列叙述正确的是
 cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.5倍,下列叙述正确的是
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.5倍,下列叙述正确的是| A.A的转化率变大 | B.平衡向正反应方向移动 |
| C.D的体积分数变大 | D.a<c+d |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列说法正确的是
| A.自发过程就是自发反应 |
| B.自发反应在任何条件下都能发生 |
| C.自发过程可能是物理变化 |
| D.煤的燃烧是非自发过程 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列说法错误的是
A.1mol 在不同状态时的熵值: 在不同状态时的熵值: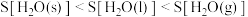 |
| B.凡是放热反应都是自发的,吸热反应都是非自发的 |
C.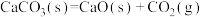  能否自发进行与温度有关 能否自发进行与温度有关 |
D.常温下反应 能自发进行,则 能自发进行,则 |
您最近一年使用:0次

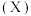 转化为产物
转化为产物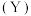 时,能量变化与反应历程的关系如图所示,下列说法正确的是
时,能量变化与反应历程的关系如图所示,下列说法正确的是
 比
比 稳定
稳定 是催化剂,可降低反应所需的活化能
是催化剂,可降低反应所需的活化能
 CO(g) +Cl2(g) △H>0,当反应达到平衡时,下列措施:①升温;②恒容通入惰性气体;③增加CO浓度;④减压;⑤加催化剂;⑥恒压通入惰性气体,能提高COCl2转化率的是
CO(g) +Cl2(g) △H>0,当反应达到平衡时,下列措施:①升温;②恒容通入惰性气体;③增加CO浓度;④减压;⑤加催化剂;⑥恒压通入惰性气体,能提高COCl2转化率的是 C(g)+3D(g)在高温时能自发进行,在低温下不能自发进行,则该反应的正反应的△H、△S应为
C(g)+3D(g)在高温时能自发进行,在低温下不能自发进行,则该反应的正反应的△H、△S应为

